A,B两种液态有机物均由碳、氢、氧三种元素组成。A能溶于水,它的相对分子质量是60,分子中有8个原子,其中氧原子数与碳原子数相等,且A与碳酸钠溶液混合时冒气泡。B分子中有9个原子,分子内所有原子的核电荷数之和为26,且B只能跟钠反应放出氢气,不能与碳酸钠溶液反应。
(1)A的结构简式为__________________ ,B的结构简式为 ________________ 。
(2)写出A与碳酸钠溶液反应的化学方程式________________________________ 。
(3)写出B与钠反应的化学方程式_____________________________ 。
(4)写出A与B反应的化学方程式_____________________________ 。
(1)A的结构简式为
(2)写出A与碳酸钠溶液反应的化学方程式
(3)写出B与钠反应的化学方程式
(4)写出A与B反应的化学方程式
更新时间:2018-06-27 11:53:55
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】某品牌小苏打粉中含有杂质NaCl,化学兴趣小组的同学进行了如下实验探究:称取10g样品放入烧杯中,加入稀盐酸至不再产生气泡为止,并绘制出加入稀盐酸的质量与放出气体质量的关系如图:

(1)反应的化学方程式为_______ 。
(2)计算该样品的纯度_______ (写出计算过程)。
(3)计算当盐酸与小苏打恰好完全反应时,所得溶液的溶质质量分数是_______ (写出计算过程,结果保留一位小数)

(1)反应的化学方程式为
(2)计算该样品的纯度
(3)计算当盐酸与小苏打恰好完全反应时,所得溶液的溶质质量分数是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Na2CO3、NaHCO3走进千家万户,在食品加工方面有着广泛的用途。
(1)下列关于Na2CO3的认识正确的是___________。
(2)传统蒸馒头常采用酵头发面,再用Na2CO3调节面团酸度。查阅资料得知,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。等质量的碳酸钠和碳酸氢钠,消耗酸更多的是___________ 。
(3)若面团发得不好,面团内的气孔少,略有酸味。可不用Na2CO3而用NaHCO3,继续揉面,上锅蒸后也能蒸出松软的馒头。解释NaHCO3的作用___________ 。
(4)某品牌复合膨松剂的说明书如图所示。其中葡萄糖酸-δ-内酯和淀粉是助剂,其作用是防止膨松剂吸潮结块而失效。焦磷酸二氢二钠的作用是___________ 。
(1)下列关于Na2CO3的认识正确的是___________。
| A.受热易分解 | B.俗称纯碱、苏打 |
| C.属于碱 | D.可与酸反应 |
(3)若面团发得不好,面团内的气孔少,略有酸味。可不用Na2CO3而用NaHCO3,继续揉面,上锅蒸后也能蒸出松软的馒头。解释NaHCO3的作用
(4)某品牌复合膨松剂的说明书如图所示。其中葡萄糖酸-δ-内酯和淀粉是助剂,其作用是防止膨松剂吸潮结块而失效。焦磷酸二氢二钠的作用是
| 【名称】xx复合膨松剂 【保质期】24个月 【净含量】1kg 【使用量】面粉用量的0.5%-2.5% 【配料】碳酸氢钠、焦磷酸二氢二钠、碳酸钙、葡萄糖酸-  -内酯、淀粉 -内酯、淀粉【适用范围】适用于各类馒头、包子等发酵面制品以及面包、糕点等的制作 【储存方法】阴凉干燥处存储 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】请回答下列问题。
(1)碳酸氢钠俗称小苏打,其水溶液显____________ 性(填“酸”、“碱”或“中”) ;
(2)等物质的量的碳酸钠和碳酸氢钠与足量盐酸反应时生成CO2的量,前者____________ 后者(填“>”、“<”或“=”) ;
(3)除去碳酸钠固体中碳酸氢钠的方法是____________ (填“加热”或“溶解过滤”) ;
(4)若金属钠长时间在潮湿的空气中放置,最后生成的物质是_________ ;
(5)将一小块金属钠投入水中,发生反应的离子方程式为_________________________ ;
(6)铝是一种比较活泼的金属,在空气中极易被氧化而生成一种致密的氧化膜,从而保护内部的铝不再被氧化。请写出此反应的化学方程式________________ 。
(1)碳酸氢钠俗称小苏打,其水溶液显
(2)等物质的量的碳酸钠和碳酸氢钠与足量盐酸反应时生成CO2的量,前者
(3)除去碳酸钠固体中碳酸氢钠的方法是
(4)若金属钠长时间在潮湿的空气中放置,最后生成的物质是
(5)将一小块金属钠投入水中,发生反应的离子方程式为
(6)铝是一种比较活泼的金属,在空气中极易被氧化而生成一种致密的氧化膜,从而保护内部的铝不再被氧化。请写出此反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题。
(1)酯化反应反应中浓硫酸的作用是_______ ,碎瓷片的作用是___________ 。
(2)酯化反应为什么反应物都必须是无水液体?___________ 。
(3)酯化反应为什么要用饱和Na2CO3溶液吸收产物?___________ 。
(4)酯化反应为什么导气管不能伸入饱和Na2CO3溶液中?___________ 。
(1)酯化反应反应中浓硫酸的作用是
(2)酯化反应为什么反应物都必须是无水液体?
(3)酯化反应为什么要用饱和Na2CO3溶液吸收产物?
(4)酯化反应为什么导气管不能伸入饱和Na2CO3溶液中?
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下列实验操作正确的是_______ 。
A.用量热计测定中和热时,为了操作方便,可用温度计直接搅拌
B.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,重复几次,完成乙醇氧化为乙醛的实验
C.试管中先加入一定量浓硫酸,再依次加入适量冰醋酸、无水乙醇,再加热制取乙酸乙酯
D.实验室制取乙烯时,放入几片碎瓷片,以避免混合液在受热沸腾时剧烈跳动
E.配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
F.验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合加热,充分振荡溶液、静置、待液体冷却后,滴加硝酸银溶液
G.向甲苯中加入酸性高锰酸钾溶液振荡,紫色不能退去
A.用量热计测定中和热时,为了操作方便,可用温度计直接搅拌
B.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,重复几次,完成乙醇氧化为乙醛的实验
C.试管中先加入一定量浓硫酸,再依次加入适量冰醋酸、无水乙醇,再加热制取乙酸乙酯
D.实验室制取乙烯时,放入几片碎瓷片,以避免混合液在受热沸腾时剧烈跳动
E.配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
F.验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合加热,充分振荡溶液、静置、待液体冷却后,滴加硝酸银溶液
G.向甲苯中加入酸性高锰酸钾溶液振荡,紫色不能退去
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ、体育比赛中当运动员肌肉挫伤或扭伤时,队医常用药剂氯乙烷(CH3CH2Cl)(沸点为12.27 ℃)对受伤部位进行局部冷却麻醉处理,工业上制取氯乙烷有两种方案:
a.CH3CH3+Cl2 CH3CH2Cl+HCl b.CH2=CH2+HCl
CH3CH2Cl+HCl b.CH2=CH2+HCl CH3—CH2Cl
CH3—CH2Cl
(1)你认为制备氯乙烷的最好方案为___________ (填“a”或“b”)。
Ⅱ、乙醇和乙酸是生活中常见的有机物。
(2)如图所示为乙醇的___________ (“空间充填”或“球棍”)模型。
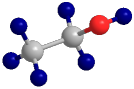
(3)乙醇中所含有的官能团的名称为___________ ,乙酸属于___________ (填“电解质”或“非电解质”)。
(4)用结构简式补全如图所示装置中乙醇和乙酸反应的化学方程式:CH3CH2OH+CH3COOH
___________ +H2O,该反应的类型为___________ 反应(填“取代”或“加成”),右侧小试管中应装有___________ 溶液(填“饱和Na2CO3”或“饱和NaOH”)。

a.CH3CH3+Cl2
 CH3CH2Cl+HCl b.CH2=CH2+HCl
CH3CH2Cl+HCl b.CH2=CH2+HCl CH3—CH2Cl
CH3—CH2Cl(1)你认为制备氯乙烷的最好方案为
Ⅱ、乙醇和乙酸是生活中常见的有机物。
(2)如图所示为乙醇的

(3)乙醇中所含有的官能团的名称为
(4)用结构简式补全如图所示装置中乙醇和乙酸反应的化学方程式:CH3CH2OH+CH3COOH


您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】乙醇在能源、生产及日常生活等许多方面都有十分广泛的应用。请回答下列问题:
(1)乙醇分子的官能团名称为_______ ,小铭将足量乙醇与4.6g金属钠充分反应,则标准状况下生成气体的体积是_______ L。
(2)小铭向一支试管中加3~5mL乙醇,再将下端绕成螺旋状的铜丝在酒精灯上灼烧至红热,插入乙醇中,反复几次。可观察到的现象是_______ ,该过程中发生的化学反应方程式为_______ 。
(1)乙醇分子的官能团名称为
(2)小铭向一支试管中加3~5mL乙醇,再将下端绕成螺旋状的铜丝在酒精灯上灼烧至红热,插入乙醇中,反复几次。可观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】乙醇在能源、生产及日常生活等许多方面都有十分广泛的应用。请计算:
(1)将足量乙醇与9.2 g金属钠充分反应,则标准状况下生成气体的体积是_______ L
(2)若一定量的乙醇和O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g)。产物依次经过浓硫酸和碱石灰使其被充分吸收,浓硫酸增重10.8 g,碱石灰增重13.2 g。则氧气的物质的量是_______________ mol,燃烧产物的平均摩尔质量是____________ g/mol。
(1)将足量乙醇与9.2 g金属钠充分反应,则标准状况下生成气体的体积是
(2)若一定量的乙醇和O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g)。产物依次经过浓硫酸和碱石灰使其被充分吸收,浓硫酸增重10.8 g,碱石灰增重13.2 g。则氧气的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】一定条件下,纤维素与乙酸酐反应可以制取醋酸纤维,同时还有乙酸生成,请写出化学方程式__________________________ ,化学反应类型_________________ 。已知某纤维乙酸酯的平均相对分子质量为311040,则对应的纤维素分子中平均含有的葡萄糖结构单元数(即聚合度n)是___________ 。
您最近一年使用:0次
【推荐2】醇的化学性质(以乙醇为例)
(1)醇的化学性质主要由_______ 官能团决定。在醇分子中由于氧原子吸引电子能力比氢原子和碳原子强,使O-H和C-O的电子对都向氧原子偏移,使O-H和C-O易断裂,即 。
。
(2)置换反应
与活泼金属(如Na)发生置换反应,其反应方程式为_______ ,反应时乙醇分子断裂的化学键为_______ 。
(3)取代反应
①酯化反应
与乙酸发生反应的方程式为_______ 。
②与氢卤酸反应
与HBr反应的化学方程式为_______ ,反应时,乙醇分子断裂的键为_______ 。
③分子间脱水生成醚
乙醇在浓硫酸作用下加热至140 ℃时,生成乙醚,其反应方程式为_______ 。
注意:①乙醚是一种无色、易_______ 的液体,沸点34.5 ℃,有特殊气味,具有_______ 作用。乙醚_______ 于水,易溶于有机溶剂,它本身是一种优良溶剂,能溶解多种有机物。
②醚的官能团叫_______ ,表示为 ,醚的结构可用
,醚的结构可用_______ 表示,R、R′都是_______ ,可以相同也可以不同。
(4)消去反应
乙醇在浓硫酸的作用下,加热至_______ 时生成乙烯,反应方程式为_______ ,浓硫酸的作用是_______ 。反应时乙醇分子断的键是_______ 与_______ 。
(5)氧化反应
①燃烧:_______ (淡蓝色火焰)。
②催化氧化:_______ 。
③被强氧化剂氧化。
④有机反应中的氧化、还原反应
氧化反应:有机物分子中_______ 氢原子或_______ 氧原子的反应叫氧化反应。
还原反应:有机物分子中_______ 氢原子或_______ 氧原子的反应叫还原反应。
(1)醇的化学性质主要由
 。
。(2)置换反应
与活泼金属(如Na)发生置换反应,其反应方程式为
(3)取代反应
①酯化反应
与乙酸发生反应的方程式为
②与氢卤酸反应
与HBr反应的化学方程式为
③分子间脱水生成醚
乙醇在浓硫酸作用下加热至140 ℃时,生成乙醚,其反应方程式为
注意:①乙醚是一种无色、易
②醚的官能团叫
 ,醚的结构可用
,醚的结构可用(4)消去反应
乙醇在浓硫酸的作用下,加热至
(5)氧化反应
①燃烧:
②催化氧化:
③被强氧化剂氧化。
④有机反应中的氧化、还原反应
氧化反应:有机物分子中
还原反应:有机物分子中
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】目前,在自然界和人工合成的上亿种物质中,绝大多数是有机化合物。有机化学已成为当代化学研究和应用的主要方向,我们的衣食住行都离不开有机化合物。请回答下列问题:
(1)下列可以清除水壶中少量水垢(主要成分是碳酸钙)的物质是
(2)为了延长果实或花朵的成熟期,需用浸泡过高锰酸钾溶液的硅土来吸收果实或花朵产生的乙烯。下列关于乙烯的叙述错误的是
(3)在一定条件下,下列物质可与甲烷发生化学反应的是
(4)下列关于乙酸乙酯的叙述错误的是
(5)下列关于乙醇的叙述错误的是
(6)正丁烷和异丁烷的分子结构模型如图所示,二者关系正确的是

(1)下列可以清除水壶中少量水垢(主要成分是碳酸钙)的物质是
| A.食醋 | B.酒精 | C.水 | D.汽油 |
| A.乙烯是一种植物生长调节剂 | B.乙烯的结构简式为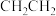 |
| C.乙烯可用于生产聚乙烯塑料 | D.乙烯可使酸性高锰酸钾溶液褪色 |
| A.NaOH溶液 | B.稀硫酸 |
| C.酸性高锰酸钾溶液 | D. |
| A.密度比水大 | B.难溶于水 |
| C.可用作化妆品中的香料 | D.可用作有机溶剂 |
| A.可用作燃料 |
B.能与金属钠反应生成 |
| C.可使紫色石蕊溶液变红 |
| D.医疗上常用75%(体积分数)的乙醇溶液作消毒剂 |

| A.同系物 | B.同分异构体 | C.同种物质 | D.同素异形体 |
您最近一年使用:0次



