醇脱水是合成烯烃的常用方法,实验室合成己烯的反应和实验装置如下:
合成反应: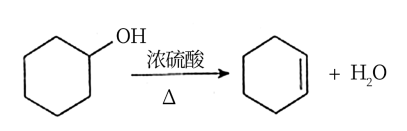
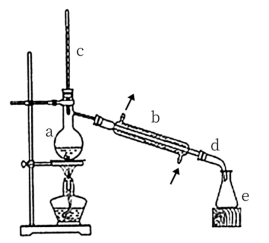
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓硫酸。b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃。
分离提纯:反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净环己烯10g。
请回答下列问题:
(1)装置b的名称是_________________ 。
(2)加入碎瓷片的作用是__________________ ,如果加热一段时间后发现忘记加碎瓷片,应该采取的正确操作是(填正确答案标号)__________ 。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为______________ 。
(4)分液漏斗在使用前须清洗干净并___________ ;在本实验分离过程中,产物应该从分液漏斗的__________ (填“上口倒出”或“下口放出”)
(5)分离提纯过程中加入无水氯化钙的目的是______________________________ 。
(6)在环己烯粗产物蒸馏过程中,不可能用到的仪器有________ (填正确答案标号)。
A.蒸馏烧瓶 B.温度计 C.玻璃棒 D.锥形瓶
(7)本实验所得到的环己烯产率是有________ (填正确答案标号)。
A.41% B.50% C.61% D.70%
合成反应:

| 相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
分离提纯:反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净环己烯10g。
请回答下列问题:
(1)装置b的名称是
(2)加入碎瓷片的作用是
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为
(4)分液漏斗在使用前须清洗干净并
(5)分离提纯过程中加入无水氯化钙的目的是
(6)在环己烯粗产物蒸馏过程中,不可能用到的仪器有
A.蒸馏烧瓶 B.温度计 C.玻璃棒 D.锥形瓶
(7)本实验所得到的环己烯产率是有
A.41% B.50% C.61% D.70%
更新时间:2018-07-03 11:23:11
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐1】药物颠茄酸酯(J)常用于胃肠道平滑肌痉挛及溃疡病的辅助治疗,其合成路线如下:

回答下列问题:
(1)芳香烃B的相对分子质量在100-110之间,1molB充分燃烧可生成72g的水,且反应1为加成反应,则B的化学名称为____ ,X的分子式为____ 。
(2)G→H的反应类型为____ 。
(3)D的结构简式为___ ,G的分子式为____ 。
(4)反应3的化学方程式为___ 。
(5)化合物I有多种同分异构体,同时满足下列条件的结构有___ 种,写出其中任意一种同分异构体结构简式___ 。
①能发生水解反应和银镜反应
②能与FeCl3溶液发生显色反应
③苯环上有四个取代基,且苯环上一卤代物只有一种

回答下列问题:
(1)芳香烃B的相对分子质量在100-110之间,1molB充分燃烧可生成72g的水,且反应1为加成反应,则B的化学名称为
(2)G→H的反应类型为
(3)D的结构简式为
(4)反应3的化学方程式为
(5)化合物I有多种同分异构体,同时满足下列条件的结构有
①能发生水解反应和银镜反应
②能与FeCl3溶液发生显色反应
③苯环上有四个取代基,且苯环上一卤代物只有一种
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐2】为测定某有机物A的结构,进行如下实验。
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成9.0g H2O和17.6g CO2,消耗氧气13.44L(标准状况下),则该有机物的分子式为___________ 。
(2)根据价键理论,属于醇类的A的结构有___________ 种(不考虑立体异构)。
(3)经测定,有机物A分子内有2种不同环境的氢原子,且A能与金属钠反应放出气体,则A的结构简式为___________ 。
(4)A在一定条件下脱水可生成B,B可发生加聚反应生成C,请写出B转化为C的化学反应方程式:___________ 。
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成9.0g H2O和17.6g CO2,消耗氧气13.44L(标准状况下),则该有机物的分子式为
(2)根据价键理论,属于醇类的A的结构有
(3)经测定,有机物A分子内有2种不同环境的氢原子,且A能与金属钠反应放出气体,则A的结构简式为
(4)A在一定条件下脱水可生成B,B可发生加聚反应生成C,请写出B转化为C的化学反应方程式:
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
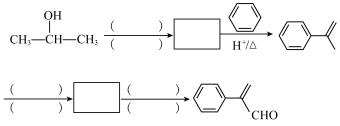
【推荐3】化合物H是一种合成药物中间体,一种合成化合物H的人工合成路线如下:
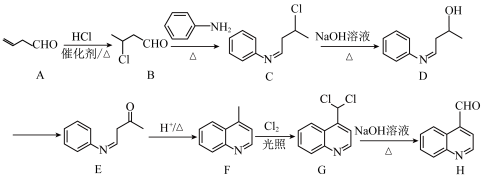
(1)A中官能团的名称为___________ ,B的化学名称为___________ ,H的分子式为___________ ;
(2)B→C的过程经历两步反应。反应类型依次为加成反应、___________ 。
(3)C→D的化学方程式为___________ ;
(4)F与足量稀盐酸反应,所得生成物的结构简式为___________ ;
(5)E满足下列条件的同分异构体有___________ 种(不考虑立体异构)。
苯环上有两个对位的取代基,其中一个取代基为-CONH2。
写出其中所有含有5种不同化学环境的氢原子的结构简式:___________ 。
(6)写出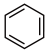 和
和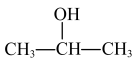 为原料制备
为原料制备 的合成路线图,(无机试剂和有机溶剂任用,箭头上方写所需试剂,下方写条件,方框内写结构简式)
的合成路线图,(无机试剂和有机溶剂任用,箭头上方写所需试剂,下方写条件,方框内写结构简式)___________ 。

(1)A中官能团的名称为
(2)B→C的过程经历两步反应。反应类型依次为加成反应、
(3)C→D的化学方程式为
(4)F与足量稀盐酸反应,所得生成物的结构简式为
(5)E满足下列条件的同分异构体有
苯环上有两个对位的取代基,其中一个取代基为-CONH2。
写出其中所有含有5种不同化学环境的氢原子的结构简式:
(6)写出
 和
和 为原料制备
为原料制备 的合成路线图,(无机试剂和有机溶剂任用,箭头上方写所需试剂,下方写条件,方框内写结构简式)
的合成路线图,(无机试剂和有机溶剂任用,箭头上方写所需试剂,下方写条件,方框内写结构简式)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室常用环己醇脱水合成环己烯。实验装置如图:
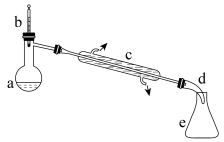
有关实验数据如 表:
合成反应:在a中加入20 g环己醇,冷却搅动下慢慢加入1mL浓硫酸。c中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃.当烧瓶中只剩下很少量的残渣并出现阵阵白雾时停止蒸馏。
分离提纯:将e中粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯10g。
(1)仪器c的名称为_____ 。
(2)该合成反应的化学方程式是__________________________________ ,实验中最容易产生的副产物结构简式为______ 。
(3)控制馏出物的温度不超过90℃的目的是_____________________________ 。
(4)分离提纯过程中加入5% Na2CO3溶液的作用是_____ ,蒸馏过程中除去的杂质主要是_____ 。
(5)本实验所得到的环己烯产率是_____ 。

有关实验数据如 表:
| 相对分子质量 | 密度/(g·cm3) | 沸点℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
分离提纯:将e中粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯10g。
(1)仪器c的名称为
(2)该合成反应的化学方程式是
(3)控制馏出物的温度不超过90℃的目的是
(4)分离提纯过程中加入5% Na2CO3溶液的作用是
(5)本实验所得到的环己烯产率是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐2】3,4-二羟基肉桂酸乙酯( )具有抗炎作用和治疗自身免疫性疾病的潜力。由气体A制备该物质的合成路线如下:
)具有抗炎作用和治疗自身免疫性疾病的潜力。由气体A制备该物质的合成路线如下:
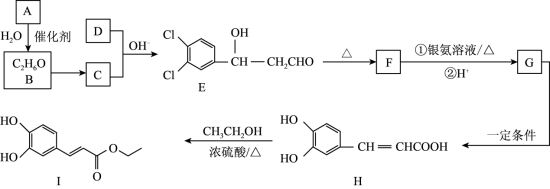
已知: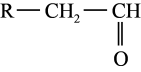 +
+
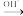
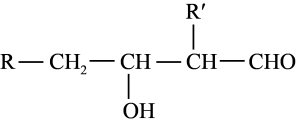
回答下列问题:
(1)已知:气体A对氢气的相对密度为14,A的化学名称是_______ 。
(2)B中含有的官能团的名称为_______ 。
(3)D的结构简式为_______ 。
(4)H→I的反应类型是_______ 。
(5)反应E→F的化学方程式为_______ ;E中含有_______ 个手性碳原子(连有四个不同基团的碳原子)。
(6)芳香族化合物X是H的同分异构体,1molX与足量NaHCO3溶液反应可生成2molCO2,符合条件的X有_______ 种,其中核磁共振氢谱的峰面积比为3:2:2:1的结构简式为_______ (写出一种)。
 )具有抗炎作用和治疗自身免疫性疾病的潜力。由气体A制备该物质的合成路线如下:
)具有抗炎作用和治疗自身免疫性疾病的潜力。由气体A制备该物质的合成路线如下:
已知:
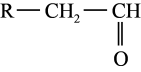 +
+

回答下列问题:
(1)已知:气体A对氢气的相对密度为14,A的化学名称是
(2)B中含有的官能团的名称为
(3)D的结构简式为
(4)H→I的反应类型是
(5)反应E→F的化学方程式为
(6)芳香族化合物X是H的同分异构体,1molX与足量NaHCO3溶液反应可生成2molCO2,符合条件的X有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】实验室中以2-丁醇[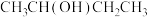 ]为原料制备2-氯丁烷,其装置如图所示(夹持、加热装置已略去):
]为原料制备2-氯丁烷,其装置如图所示(夹持、加热装置已略去):

相关信息见下表:
实验步骤如下:
步骤1:甲装置的圆底烧瓶中加入少量无水 和
和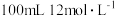 浓盐酸,充分溶解、冷却,再加入
浓盐酸,充分溶解、冷却,再加入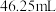 2-丁醇加热一段时间。
2-丁醇加热一段时间。
步骤2:将反应混合物移至乙装置的蒸馏烧瓶内,蒸馏并收集115℃以下的馏分。
步骤3:对馏分进行系列操作,分离出粗产品。
步骤4:经过进一步精制得产品37.0g。
步骤5:测定实验生成2-氯丁烷的产率。
回答下列问题:
(1)甲装置中圆底烧瓶的容积可选择___________ (填标号)。
A.150mL B.250mL C.1000mL D.1500mL
(2)甲装置中Ⅰ处仪器的作用是___________ ,乙装置中Ⅱ处的仪器是___________ (填“A”或“B”)。
(3)“步骤1”中无水氯化锌的作用是___________ 。
(4)“步骤3”中先用蒸馏水洗涤,是为了除去___________ ;再用10% 溶液洗涤,该操作要迅速,原因是
溶液洗涤,该操作要迅速,原因是___________ ;最后加入 固体干燥并过滤。上述步骤中除过滤外,还涉及的操作有
固体干燥并过滤。上述步骤中除过滤外,还涉及的操作有___________ 。
(5)2-氯丁烷的产率是___________ 。
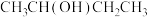 ]为原料制备2-氯丁烷,其装置如图所示(夹持、加热装置已略去):
]为原料制备2-氯丁烷,其装置如图所示(夹持、加热装置已略去):
相关信息见下表:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/( ) ) | 性质 |
| 2-丁醇 | -114.7 | 99.5 | 0.80 | 与水互溶 |
| 2-氯丁烷 | -131.3 | 68.2 | 0.87 | 微溶于水,碱性条件下水解 |
步骤1:甲装置的圆底烧瓶中加入少量无水
 和
和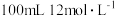 浓盐酸,充分溶解、冷却,再加入
浓盐酸,充分溶解、冷却,再加入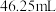 2-丁醇加热一段时间。
2-丁醇加热一段时间。步骤2:将反应混合物移至乙装置的蒸馏烧瓶内,蒸馏并收集115℃以下的馏分。
步骤3:对馏分进行系列操作,分离出粗产品。
步骤4:经过进一步精制得产品37.0g。
步骤5:测定实验生成2-氯丁烷的产率。
回答下列问题:
(1)甲装置中圆底烧瓶的容积可选择
A.150mL B.250mL C.1000mL D.1500mL
(2)甲装置中Ⅰ处仪器的作用是
(3)“步骤1”中无水氯化锌的作用是
(4)“步骤3”中先用蒸馏水洗涤,是为了除去
 溶液洗涤,该操作要迅速,原因是
溶液洗涤,该操作要迅速,原因是 固体干燥并过滤。上述步骤中除过滤外,还涉及的操作有
固体干燥并过滤。上述步骤中除过滤外,还涉及的操作有(5)2-氯丁烷的产率是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
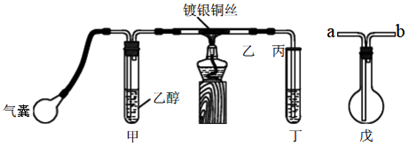
【推荐1】某课外活动小组利用下图装置进行乙醇的催化氧化实验并制取乙醛,图中铁架台等装置已略去,粗黑线表示乳胶管。请填写下列空白:
(1)甲装置常常浸在70~80℃的水浴中,目的是__________________ 。
(2)实验时,先加热玻璃管乙中的镀银铜丝,约1分钟后鼓入空气,此时铜丝即呈红热状态。若把酒精灯撤走,控制一定的鼓气速度,铜丝能长时间保持红热直到实验结束。 乙醇的催化氧化反应是________ 反应(填“放热”或“吸热”)
(3)若试管丁中用水吸收产物,则要在导管乙、丙之间接上戊装置,其连接方法是(填戊装置中导管代号):乙接_____ 、_____ 接丙;若产物不用水吸收而是直接冷却,应将试管丁浸在_____ 中。

(1)甲装置常常浸在70~80℃的水浴中,目的是
(2)实验时,先加热玻璃管乙中的镀银铜丝,约1分钟后鼓入空气,此时铜丝即呈红热状态。若把酒精灯撤走,控制一定的鼓气速度,铜丝能长时间保持红热直到实验结束。 乙醇的催化氧化反应是
(3)若试管丁中用水吸收产物,则要在导管乙、丙之间接上戊装置,其连接方法是(填戊装置中导管代号):乙接
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】3,5-二甲氧基苯酚是重要的有机合成中间体,一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
(1)1mol间苯三酚完全燃烧需要______ molO2。
(2)反应结束后,先分离出甲醇,再加入乙醚进行萃取。
①分离出甲醇的操作是的__________ 。
②萃取用到的分液漏斗使用前需____________ 并洗净,分液时有机层在分液漏斗的______ 填(“上”或“下”)层。
(3)分离得到的有机层依次用饱和NaHCO3溶液、少量蒸馏水进行洗涤。用饱和NaHCO3溶液洗涤的目的是_________________________________________ ;
(4)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是_____________ (填字母)。
a.蒸馏除去乙醚 b.冷却结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(5)反应可能出现的副产物的结构简式为___________________ 。

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
| 物质 | 沸点/℃ | 熔点/℃ | 密度(20℃) / g·cm-3 | 溶解性 |
| 甲醇 | 64. 7 |  | 0. 7915 | 易溶于水 |
| 乙醚 | 34. 5 |  | 0. 7138 | 微溶于水 |
| 3,5-二甲氧基苯酚 |  | 33 ~36 |  | 易溶于甲醇、乙醚,微溶于水 |
(2)反应结束后,先分离出甲醇,再加入乙醚进行萃取。
①分离出甲醇的操作是的
②萃取用到的分液漏斗使用前需
(3)分离得到的有机层依次用饱和NaHCO3溶液、少量蒸馏水进行洗涤。用饱和NaHCO3溶液洗涤的目的是
(4)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是
a.蒸馏除去乙醚 b.冷却结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(5)反应可能出现的副产物的结构简式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】苯甲酸广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸。反应原理:
已知:甲苯的熔点为﹣95℃,沸点为110.6℃,易挥发,密度为0.866g/cm3;
苯甲酸的熔点为122.4℃,在25℃和95℃下在水中溶解度分别为0.344g和6.8g。
Ⅰ.【制备产品】将30.0mL甲苯和25.0mL 1mol/L高锰酸钾溶液在100℃下反应30min,装置如图1所示:

(1)仪器A的名称为________ ,A的进水口为___ (填“a”或“b”)。支管的作用是____________ 。
(2)在本实验中,三颈烧瓶最合适的容积是____ (填字母).
A.50mL B.100mL C.250mL D.500mL
Ⅱ.【分离产品】该同学设计如图2流程分离粗产品苯甲酸和回收甲苯。

(3)操作Ⅰ的名称是________ ;含有杂质的产物经操作Ⅱ进一步提纯得无色液体甲苯,则操作Ⅱ的名称是_________ 。
Ⅲ.【纯度测定】称取1.220g白色固体,配成100mL甲醇溶液,取25.00mL溶液,用0.1000mol/LKOH标准溶液滴定,重复滴定四次,每次消耗的体积如表所示.
(4)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则测定结果______ (填“偏大”、“偏小”或“不变”).计算样品中苯甲酸纯度为_________ 。
(5)从白色固体B中得到纯净的苯甲酸的实验方法是:____________________ 。

已知:甲苯的熔点为﹣95℃,沸点为110.6℃,易挥发,密度为0.866g/cm3;
苯甲酸的熔点为122.4℃,在25℃和95℃下在水中溶解度分别为0.344g和6.8g。
Ⅰ.【制备产品】将30.0mL甲苯和25.0mL 1mol/L高锰酸钾溶液在100℃下反应30min,装置如图1所示:

(1)仪器A的名称为
(2)在本实验中,三颈烧瓶最合适的容积是
A.50mL B.100mL C.250mL D.500mL
Ⅱ.【分离产品】该同学设计如图2流程分离粗产品苯甲酸和回收甲苯。

(3)操作Ⅰ的名称是
Ⅲ.【纯度测定】称取1.220g白色固体,配成100mL甲醇溶液,取25.00mL溶液,用0.1000mol/LKOH标准溶液滴定,重复滴定四次,每次消耗的体积如表所示.
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 体积(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
(5)从白色固体B中得到纯净的苯甲酸的实验方法是:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用a装置来制备。

完成下列填空:
(1)a装置中玻璃仪器除导管和试管外还有___ 仪器。
(2)实验时,通常加入过量的乙醇,原因是:___ 。加入数滴浓硫酸即能起催化作用,但实际用量多于此量,原因是:___ 。浓硫酸用量又不能过多,原因是___ 。
(3)饱和Na2CO3溶液的作用是___ 。
(4)反应结束后,将试管中收集到的产品倒入分液漏斗中,___ 、__ ,然后分液。这样得到的乙酸乙酯是粗产品,要进一步提纯精制,通常先用饱和食盐水洗涤除去少量Na2CO3溶液,再用饱和CaCl2溶液除去少量__ 。
(5)若用b装置制备乙酸乙酯,其缺点有___ 、___ 。

完成下列填空:
(1)a装置中玻璃仪器除导管和试管外还有
(2)实验时,通常加入过量的乙醇,原因是:
(3)饱和Na2CO3溶液的作用是
(4)反应结束后,将试管中收集到的产品倒入分液漏斗中,
(5)若用b装置制备乙酸乙酯,其缺点有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,该厂用上述废金属屑制取新型高效水处理剂Na2FeO4(高铁酸钠)等产品,过程如下:
Ⅰ.向废金属屑中加入过量的NaOH溶液,充分反应后过滤;
Ⅱ.向Ⅰ所得固体中加入过量稀H2SO4,充分反应后过滤;
Ⅲ.向Ⅱ所得固体中继续加入热的稀H2SO4,同时不断鼓入空气,固体溶解得CuSO4溶液;
Ⅳ.……
(1)步骤Ⅰ中发生反应的化学方程式为_________ 。
(2)步骤Ⅱ所得的滤液中一定含有的阳离子为________ 。
(3)步骤Ⅲ获得CuSO4溶液的离子方程式为________ 。
(4)步骤Ⅱ所得滤液经进一步处理可制得Na2FeO4,流程如图:
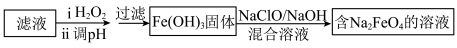
①测得滤液中c(Fe2+)为amol•L-1,若要处理1m3滤液,理论上需要消耗25%的H2O2溶液________ kg(用含a的代数式表示)。
②写出由Fe(OH)3制取Na2FeO4的化学方程式________ 。
Ⅰ.向废金属屑中加入过量的NaOH溶液,充分反应后过滤;
Ⅱ.向Ⅰ所得固体中加入过量稀H2SO4,充分反应后过滤;
Ⅲ.向Ⅱ所得固体中继续加入热的稀H2SO4,同时不断鼓入空气,固体溶解得CuSO4溶液;
Ⅳ.……
(1)步骤Ⅰ中发生反应的化学方程式为
(2)步骤Ⅱ所得的滤液中一定含有的阳离子为
(3)步骤Ⅲ获得CuSO4溶液的离子方程式为
(4)步骤Ⅱ所得滤液经进一步处理可制得Na2FeO4,流程如图:

①测得滤液中c(Fe2+)为amol•L-1,若要处理1m3滤液,理论上需要消耗25%的H2O2溶液
②写出由Fe(OH)3制取Na2FeO4的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】五氧化二氮(N2O5)是一种绿色硝化剂,在军用炸药、火箭推进剂、医药等工业中得到广泛应用。常温下N2O5为白色固体,可溶于二氯甲烷等氯代烃溶剂,微溶于水且与水反应生成硝酸,高于室温时不稳定。回答下列问题:
(1)1840年,Devill将干燥的氯气通入无水硝酸银中,首次制得了固体N2O5。该反应的氧化产物为空气中的主要成分之一,写出反应的化学方程式:_______ 。
(2)某化学兴趣小组设计用臭氧(O3)氧化法制备N2O5,反应原理为 N2O4+O3→N2O5+O2。实验装置如下图:
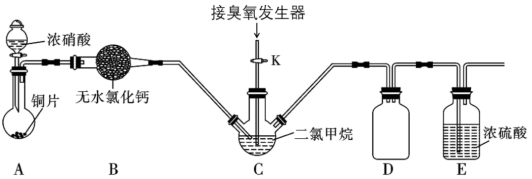
装置B的仪器名称是_______ ;装置E的作用是_______ 。实验时,先将三口烧瓶C浸入_______ (填字母编号)中,打开装置A中分液漏斗的活塞,随即关闭。一段时间后C中液体变为红棕色。然后打开活塞K,通过臭氧发生器向三口烧瓶中通入含有臭氧的氧气。
a.热水 b.冰水 c.自来水 d.饱和食盐水
(3)C中二氯甲烷(CH2Cl2)的作用是_______ (填字母编号)。判断C中反应已结束的简单方法是_______ 。
a.溶解反应物NO2 b.充分混合反应物使其反应更加充分 c.控制O3的通入速度 d.溶解生成物N2O5
(4)该装置存在一处明显缺陷,请指出_______ 。
(5)N2O5粗产品中常含有N2O4。该兴趣小组用滴定法测定N2O5粗产品的纯度。取2.0g粗产品,加入20.00mL 0.1250mol·L-1酸性高锰酸钾溶液。充分反应后,用0.1000mol·L-1 H2O2溶液滴定剩余的高锰酸钾,达到滴定终点时,消耗H2O2溶液17.50mL。已知:N2O4与KMnO4发生反应的离子方程式为5N2O4+2MnO +2H2O→Mn2++10NO
+2H2O→Mn2++10NO +4H+,H2O2与KMnO4发生反应的离子方程式为5H2O2+2MnO
+4H+,H2O2与KMnO4发生反应的离子方程式为5H2O2+2MnO +6H+→2Mn2++5O2↑+8H2O,H2O2与HNO3不反应且不考虑其分解。判断滴定到达终点的方法是
+6H+→2Mn2++5O2↑+8H2O,H2O2与HNO3不反应且不考虑其分解。判断滴定到达终点的方法是_______ 。粗产品的纯度为_______ (结果保留三位有效数字)。
(1)1840年,Devill将干燥的氯气通入无水硝酸银中,首次制得了固体N2O5。该反应的氧化产物为空气中的主要成分之一,写出反应的化学方程式:
(2)某化学兴趣小组设计用臭氧(O3)氧化法制备N2O5,反应原理为 N2O4+O3→N2O5+O2。实验装置如下图:

装置B的仪器名称是
a.热水 b.冰水 c.自来水 d.饱和食盐水
(3)C中二氯甲烷(CH2Cl2)的作用是
a.溶解反应物NO2 b.充分混合反应物使其反应更加充分 c.控制O3的通入速度 d.溶解生成物N2O5
(4)该装置存在一处明显缺陷,请指出
(5)N2O5粗产品中常含有N2O4。该兴趣小组用滴定法测定N2O5粗产品的纯度。取2.0g粗产品,加入20.00mL 0.1250mol·L-1酸性高锰酸钾溶液。充分反应后,用0.1000mol·L-1 H2O2溶液滴定剩余的高锰酸钾,达到滴定终点时,消耗H2O2溶液17.50mL。已知:N2O4与KMnO4发生反应的离子方程式为5N2O4+2MnO
 +2H2O→Mn2++10NO
+2H2O→Mn2++10NO +4H+,H2O2与KMnO4发生反应的离子方程式为5H2O2+2MnO
+4H+,H2O2与KMnO4发生反应的离子方程式为5H2O2+2MnO +6H+→2Mn2++5O2↑+8H2O,H2O2与HNO3不反应且不考虑其分解。判断滴定到达终点的方法是
+6H+→2Mn2++5O2↑+8H2O,H2O2与HNO3不反应且不考虑其分解。判断滴定到达终点的方法是
您最近一年使用:0次



