海洋资源的利用具有广阔前景.
(1)如图是从海水中提取镁的简单流程.

工业上常用于沉淀Mg2+的试剂A是______ (填物质名称),Mg(OH)2转化为MgCl2的离子方程式是______ .
(2)海带灰中富含以I﹣形式存在的碘元素。实验室提取I2的途径如下所示:
干海带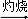 海带灰
海带灰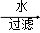 滤液
滤液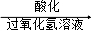
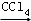
 I2
I2
①灼烧海带至灰烬时所用的主要仪器名称是______ .
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式______ .
③反应结束后,加入CCl4作萃取剂,采用萃取﹣分液的方法从碘水中提取碘,主要操作步骤如图:
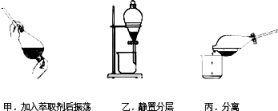
甲、乙、丙3步实验操作中,不正确的是______ (填“甲”、“乙”或“丙”).
(1)如图是从海水中提取镁的简单流程.

工业上常用于沉淀Mg2+的试剂A是
(2)海带灰中富含以I﹣形式存在的碘元素。实验室提取I2的途径如下所示:
干海带
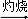 海带灰
海带灰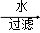 滤液
滤液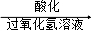
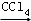
 I2
I2①灼烧海带至灰烬时所用的主要仪器名称是
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
③反应结束后,加入CCl4作萃取剂,采用萃取﹣分液的方法从碘水中提取碘,主要操作步骤如图:

甲、乙、丙3步实验操作中,不正确的是
更新时间:2018-07-07 21:51:14
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】钛酸钡( )是电子陶瓷中使用最广泛的材料之一,一种以富钛渣(主要成分为
)是电子陶瓷中使用最广泛的材料之一,一种以富钛渣(主要成分为 ,含少量Si和Al的氧化物杂质)和重晶石(主要成分是
,含少量Si和Al的氧化物杂质)和重晶石(主要成分是 )为原料,制备钛酸钡的工艺流程如图所示。
)为原料,制备钛酸钡的工艺流程如图所示。 中含有的几种物质的沸点:
中含有的几种物质的沸点:
②草酸氧钛钡晶体的化学式为 。
。
回答下列问题:
(1)沸腾氯化时气体与矿料逆流而行,目的是_______ ;若沸腾氯化时生成 的反应中氧化产物为CO,则氧化剂和还原剂的物质的量之比为
的反应中氧化产物为CO,则氧化剂和还原剂的物质的量之比为_______ 。
(2)除硅、铝过程中,分离 中含Si、Al杂质的方法是
中含Si、Al杂质的方法是_______ ;高温还原时, 和碳粉的投料比(物质的量之比)要大于
和碳粉的投料比(物质的量之比)要大于 ,目的是
,目的是_______ ;生产过程中应避免氧气进入,主要原因是_______ 。
(3)转化过程中溶液中的钛元素在不同pH时主要以 、
、 、
、 这三种形式存在(变化曲线如图所示)。
这三种形式存在(变化曲线如图所示)。_______ ,再进行转化,写出该条件生成草酸氧钛钡晶体的离子方程式:_______ 。
②滤液2的主要成分为_______ (填化学式)。
(4)常温下,用 溶液浸泡
溶液浸泡 固体,也能将
固体,也能将 转化为
转化为 。不考虑
。不考虑 的水解,向340 mL 3.0
的水解,向340 mL 3.0
 溶液中加入4.66 g
溶液中加入4.66 g ,恰好完全转化为
,恰好完全转化为 ,则
,则
_______ 。[已知: ;溶液体积变化忽略不计]
;溶液体积变化忽略不计]
 )是电子陶瓷中使用最广泛的材料之一,一种以富钛渣(主要成分为
)是电子陶瓷中使用最广泛的材料之一,一种以富钛渣(主要成分为 ,含少量Si和Al的氧化物杂质)和重晶石(主要成分是
,含少量Si和Al的氧化物杂质)和重晶石(主要成分是 )为原料,制备钛酸钡的工艺流程如图所示。
)为原料,制备钛酸钡的工艺流程如图所示。
 中含有的几种物质的沸点:
中含有的几种物质的沸点:| 物质 |  |  |  |
| 沸点/℃ | 136 | 57 | 180 |
 。
。回答下列问题:
(1)沸腾氯化时气体与矿料逆流而行,目的是
 的反应中氧化产物为CO,则氧化剂和还原剂的物质的量之比为
的反应中氧化产物为CO,则氧化剂和还原剂的物质的量之比为(2)除硅、铝过程中,分离
 中含Si、Al杂质的方法是
中含Si、Al杂质的方法是 和碳粉的投料比(物质的量之比)要大于
和碳粉的投料比(物质的量之比)要大于 ,目的是
,目的是(3)转化过程中溶液中的钛元素在不同pH时主要以
 、
、 、
、 这三种形式存在(变化曲线如图所示)。
这三种形式存在(变化曲线如图所示)。
②滤液2的主要成分为
(4)常温下,用
 溶液浸泡
溶液浸泡 固体,也能将
固体,也能将 转化为
转化为 。不考虑
。不考虑 的水解,向340 mL 3.0
的水解,向340 mL 3.0
 溶液中加入4.66 g
溶液中加入4.66 g ,恰好完全转化为
,恰好完全转化为 ,则
,则
 ;溶液体积变化忽略不计]
;溶液体积变化忽略不计]
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室以一种工业废渣(主要成分为MgCO3、MgSO4,含有少量Fe、Al的氧化物)为原料制备MgCO3·3H2O。实验过程如下:
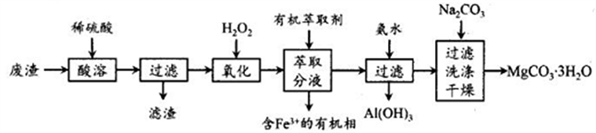
(1)为加快酸溶速率,可采取的办法有______ ,写出酸溶时废渣中主要成分发生反应的化学方程式为_________________ 。
(2)加入H2O2氧化时发生发应的离子方程式为_________________ 。
(3)用萃取分液的方法除去溶液中的Fe3+。
①检验溶液中是否含有Fe3+的最佳试剂是_________________ 。
②为使Fe3+ 尽可能多地从水相转移至有机相,采取的操作:向水溶液中加入一定量的萃取剂,_______ 、静置、分液,并重复多次。
③萃取时,向混合溶液(含Fe2+、Al3+、Mg2+)中加入适量盐酸,使Fe2+ 与Cl-生成[FeCl4]-,再用足量的乙醚(Et2O)进行萃取,乙醚与H+结合,生成了离子Et2O·H+,由于[FeCl4]-与Et2O·H+离子容易形成缔合物Et2O·H+·[FeCl4]-。该缔合物中,Cl-和Et2O分别取代了Fe2+和H+的配位水分子,并且中和了电荷,具有疏水性,能够溶于乙醚中。因此,就从水相转移到有机相中。该萃取剂不能萃取Al3+、Mg2+的原因是_________ 。
(4)已知:Ksp[Al(OH)3]=1.0×10-33,Ksp[(Mg(OH)2)=1.0×10-12.pH=8.5时Mg(OH)2开始沉淀。室温下,除去MgSO4溶液中的Al3+(使其浓度小于1×10-6mol·L-1),需加入氨水调节溶液pH的范围为____________ 。
(5)向滤液中加入Na2CO3溶液生成MgCO3 沉淀并用蒸馏水洗涤,检验沉淀是否洗净的操作是________________ 。
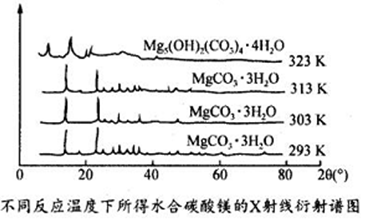
(6)干燥时需低温干燥,温度较高时发生副反应,写出MgCO3·3H2O在323K温度时发生转化的化学方程式________________ 。

(1)为加快酸溶速率,可采取的办法有
(2)加入H2O2氧化时发生发应的离子方程式为
(3)用萃取分液的方法除去溶液中的Fe3+。
①检验溶液中是否含有Fe3+的最佳试剂是
②为使Fe3+ 尽可能多地从水相转移至有机相,采取的操作:向水溶液中加入一定量的萃取剂,
③萃取时,向混合溶液(含Fe2+、Al3+、Mg2+)中加入适量盐酸,使Fe2+ 与Cl-生成[FeCl4]-,再用足量的乙醚(Et2O)进行萃取,乙醚与H+结合,生成了离子Et2O·H+,由于[FeCl4]-与Et2O·H+离子容易形成缔合物Et2O·H+·[FeCl4]-。该缔合物中,Cl-和Et2O分别取代了Fe2+和H+的配位水分子,并且中和了电荷,具有疏水性,能够溶于乙醚中。因此,就从水相转移到有机相中。该萃取剂不能萃取Al3+、Mg2+的原因是
(4)已知:Ksp[Al(OH)3]=1.0×10-33,Ksp[(Mg(OH)2)=1.0×10-12.pH=8.5时Mg(OH)2开始沉淀。室温下,除去MgSO4溶液中的Al3+(使其浓度小于1×10-6mol·L-1),需加入氨水调节溶液pH的范围为
(5)向滤液中加入Na2CO3溶液生成MgCO3 沉淀并用蒸馏水洗涤,检验沉淀是否洗净的操作是
(6)干燥时需低温干燥,温度较高时发生副反应,写出MgCO3·3H2O在323K温度时发生转化的化学方程式

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】乙酰乙酸乙酯是重要的有机合成原料,实验室制备乙酰乙酸乙酯的反应原理为:2CH3COOC2H5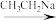 CH3COCH2COOC2H5+CH3CH2OH。
CH3COCH2COOC2H5+CH3CH2OH。

甲是制备装置(烧瓶中物质充分反应后再滴加乙酸溶液),流程图是分离步骤:
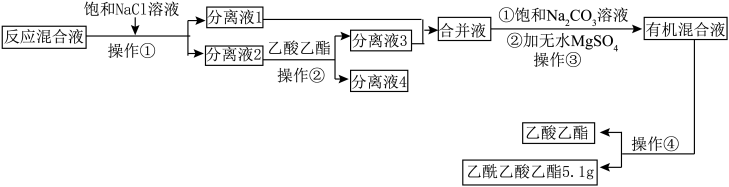
已知:几种物质的部分性质:
回答下列问题:
(1)制备反应需要加热才能发生,装置甲的最适合的加热方式___________。
(2)装置甲中球形冷凝管中冷却水从___________ (填“a”或“b”)口进入;滴加50%乙酸的仪器名称是___________ 。
(3)操作①进行的有关操作中,选出其中正确操作并按顺序排列:涂凡士林→检漏→___________ →清洗干净。
a.打开玻璃塞放气
b.打开旋塞放气
c.将溶液和饱和NaCl移至分液漏斗中,塞上玻璃塞
d.双手托住分液漏斗,右手压住玻璃塞,左手握住旋塞,上下颠倒振荡
e.双手托住分液漏斗,右手压住玻璃塞,左手握住旋塞,将分液漏斗倒转振荡
f.置于铁架台铁圈上静置,打开玻璃塞,将旋塞拧开,放出下层液体
g.从下层放出分离液1
h.从上口倒出分离液1
(4)关于装置甲及流程中的部分步骤,下列说法正确的是___________。
(5)操作④是一个系列过程,先水浴加热蒸出乙酸乙酯,剩余液加入再进行减压蒸条件下蒸馏,减压蒸馏的目的是___________ 。
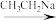 CH3COCH2COOC2H5+CH3CH2OH。
CH3COCH2COOC2H5+CH3CH2OH。
甲是制备装置(烧瓶中物质充分反应后再滴加乙酸溶液),流程图是分离步骤:

已知:几种物质的部分性质:
| 物质 | 沸点/℃ | 相对分子质量 | 水中溶解性 |
| 乙酸乙酯 | 77.2 | 88 | 难溶 |
| 乙酰乙酸乙酯 | 181(温度超过95°C,易分解) | 130 | 微溶 |
| 乙酸 | 118 | 60 | 易溶 |
(1)制备反应需要加热才能发生,装置甲的最适合的加热方式___________。
| A.酒精灯直接加热 | B.垫石棉网用酒精灯加热 |
| C.水浴 | D.油浴 |
(3)操作①进行的有关操作中,选出其中正确操作并按顺序排列:涂凡士林→检漏→
a.打开玻璃塞放气
b.打开旋塞放气
c.将溶液和饱和NaCl移至分液漏斗中,塞上玻璃塞
d.双手托住分液漏斗,右手压住玻璃塞,左手握住旋塞,上下颠倒振荡
e.双手托住分液漏斗,右手压住玻璃塞,左手握住旋塞,将分液漏斗倒转振荡
f.置于铁架台铁圈上静置,打开玻璃塞,将旋塞拧开,放出下层液体
g.从下层放出分离液1
h.从上口倒出分离液1
(4)关于装置甲及流程中的部分步骤,下列说法正确的是___________。
| A.制备钠珠后,迅速投入到三颈烧瓶中 |
| B.去掉干燥管不影响实验结果 |
| C.操作①与操作②相同,所加饱和氯化钠溶液和乙酸乙酯都是为了减小产品溶解,利于分层 |
| D.操作③包括分液和过滤,饱和Na2CO3溶液不能用NaOH溶液代替,但MgSO4固体可用无水Na2SO4代替 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】海带中含有碘元素,从海带中提取碘并验证其性质,提取过程如图所示:
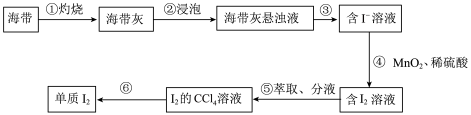
(1)步骤①灼烧的目的__________ 。步骤③和⑤的实验操作名称分别为__________ ,__________ 。
(2)图示步骤④中氧化剂为__________ ,请写出步骤④所发生的离子反应__________ 。
(3) 、稀硫酸可用
、稀硫酸可用______ 代替(填序号)。
a. b.
b. 、稀硫酸 c.
、稀硫酸 c.
请写出所选试剂与 反应的离子反应方程式
反应的离子反应方程式__________ 。
(4)因为海带灰中含有硫酸盐等可溶性杂质,在实验步骤______ (填序号)中实现与碘分离。
(5)某同学制得的粗碘中含有少量 ,对粗碘进行提纯的装置如图所示,采用的分离方法是
,对粗碘进行提纯的装置如图所示,采用的分离方法是__________ ;a、b为冷凝水进出口,其中______ (填“a”或“b”)接水龙头,最终能得到较多较高纯度的单质碘。
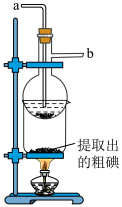

(1)步骤①灼烧的目的
(2)图示步骤④中氧化剂为
(3)
 、稀硫酸可用
、稀硫酸可用a.
 b.
b. 、稀硫酸 c.
、稀硫酸 c.
请写出所选试剂与
 反应的离子反应方程式
反应的离子反应方程式(4)因为海带灰中含有硫酸盐等可溶性杂质,在实验步骤
(5)某同学制得的粗碘中含有少量
 ,对粗碘进行提纯的装置如图所示,采用的分离方法是
,对粗碘进行提纯的装置如图所示,采用的分离方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验(苯,一种不溶于水,密度比水小的液体):
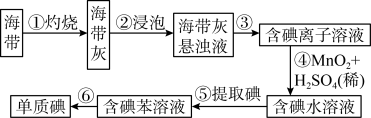
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是_______ (从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是_______ ;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是_______ 。
(3)步骤⑤是萃取、分液,某学生选择用苯来提取碘的理由是_________ ;萃取后,上层液体呈_________ 色,下层液体呈_________ 色。

请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是
(3)步骤⑤是萃取、分液,某学生选择用苯来提取碘的理由是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如图:
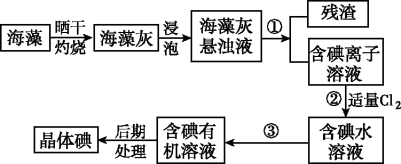
(1)实验室焙烧海带,需要下列仪器中的______ (填字母)。
a.试管 b.烧杯 c.坩埚 d.泥三角 e.铁三脚架 f.酒精灯
(2)指出提取碘的过程中有关的实验操作名称:①______ ,③______ 。
(3)提取碘的过程中,可选择的有机试剂是______ 。
A.甲苯、酒精 B.四氯化碳、苯 C.汽油、乙酸 D.汽油、甘油
(4)为使海藻灰中碘离子转化为碘的有机溶液,实验室有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器有______ 、______ 。
(5)某学习小组用CCl4萃取碘水中的碘,在如图的分液漏斗中,下层液体呈______ 色;他们打开分液漏斗活塞,却未见液体流下,原因可能是___________ 。
(6)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,进行上述蒸馏操作时,使用了水浴加热,使用水浴加热的原因是_________ ,最后晶态碘在______ 里聚集(填仪器名称)。

(1)实验室焙烧海带,需要下列仪器中的
a.试管 b.烧杯 c.坩埚 d.泥三角 e.铁三脚架 f.酒精灯
(2)指出提取碘的过程中有关的实验操作名称:①
(3)提取碘的过程中,可选择的有机试剂是
A.甲苯、酒精 B.四氯化碳、苯 C.汽油、乙酸 D.汽油、甘油
(4)为使海藻灰中碘离子转化为碘的有机溶液,实验室有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器有
(5)某学习小组用CCl4萃取碘水中的碘,在如图的分液漏斗中,下层液体呈

(6)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,进行上述蒸馏操作时,使用了水浴加热,使用水浴加热的原因是
您最近一年使用:0次



