铜的离子除了铜离子(Cu2+)外,自然界中还存在亚铜离子(Cu+)。Cu+在水溶液中没有Cu2+稳定,易在酸性条件下发生反应:2Cu+═Cu2++Cu。+1价铜的化合物通常是难溶物,如Cu2O、CuI、CuCl、Cu2S、等。
回答下列问题:
(1) 在新制Cu(OH)2悬浊液中滴入葡萄糖溶液,加热生成难溶物的颜色为________ ;若继续加热,出现黑色物质,判断这种物质的化学式为________________ 。
(2) 在CuCl2溶液中滴加过量KI溶液,可发生如下反应:
a.2Cu2++4I-═2CuI↓(白色)+I2
b.2Cu2++2Cl-+2I-═2CuCl↓(白色)+I2
为顺利观察到CuI、CuCl白色沉淀,可以加入下列试剂中的________ 。
A.乙醇 B.苯 C.盐酸溶液 D.NaCl溶液
(3) Cu2S在稀H2SO4酸化下与氧气反应生成CuSO4,该反应的化学方程式为________________________________ ;该反应的还原剂为________________ ,当1 mol O2发生反应时,还原剂所失电子的物质的量为________ mol,其中被S元素还原的O2的物质的量为________ mol。
回答下列问题:
(1) 在新制Cu(OH)2悬浊液中滴入葡萄糖溶液,加热生成难溶物的颜色为
(2) 在CuCl2溶液中滴加过量KI溶液,可发生如下反应:
a.2Cu2++4I-═2CuI↓(白色)+I2
b.2Cu2++2Cl-+2I-═2CuCl↓(白色)+I2
为顺利观察到CuI、CuCl白色沉淀,可以加入下列试剂中的
A.乙醇 B.苯 C.盐酸溶液 D.NaCl溶液
(3) Cu2S在稀H2SO4酸化下与氧气反应生成CuSO4,该反应的化学方程式为
更新时间:2018-07-25 21:46:54
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生的反应为2NO+2CO═N2+2CO2。
(1)碳元素的化合价_______ (填“升高”或“降低”),被_______ (填“氧化”或“还原”),CO是_______ 剂(填“氧化”或“还原”),NO是_______ 剂(填“氧化”或“还原”),发生_______ 反应。(填“氧化”或“还原”)
(2)用双线桥表示此反应中的电子得失情况2NO+2CO═N2+2CO2_______ 。
(3)用单线桥表示此反应中的电子转移情况2NO+2CO═N2+2CO2_______ 。
(4)若反应中消耗了2molCO,则生成N2的物质的量为_______ mol,转移电子的物质的量为_______ mol。
(1)碳元素的化合价
(2)用双线桥表示此反应中的电子得失情况2NO+2CO═N2+2CO2
(3)用单线桥表示此反应中的电子转移情况2NO+2CO═N2+2CO2
(4)若反应中消耗了2molCO,则生成N2的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一个氧化还原反应体系,共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质。
(1)该反应中,化合价升高的反应物是__ ,化合价没有发生变化的反应物是__ 。
(2)写出一个包含上述七种物质的氧化还原反应方程式(需配平)__ 。
(3)上述反应中,氧化剂是__ ,1mol氧化剂在反应中__ (填“得到”或“失去”)__ mol电子。
(4)如果在反应后的溶液中加入NaBiO3,溶液又显紫红色。此现象说明NaBiO3具有__ (填“氧化性”或“还原性”)。写出该反应的离子方程式:__ 。
(提示:NaBiO3为黄色或棕色粉末,不溶于冷水,在该反应中转化为Bi3+)
(1)该反应中,化合价升高的反应物是
(2)写出一个包含上述七种物质的氧化还原反应方程式(需配平)
(3)上述反应中,氧化剂是
(4)如果在反应后的溶液中加入NaBiO3,溶液又显紫红色。此现象说明NaBiO3具有
(提示:NaBiO3为黄色或棕色粉末,不溶于冷水,在该反应中转化为Bi3+)
您最近一年使用:0次
【推荐3】把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2
(1)用单线桥表示反应的电子转移方向和数目:______________ 。
(2)反应中发生电子转移的NH3与Cl2的分子数之比为:_______ 。
(3)若反应中有3.4克氨发生氧化反应,则反应中生成氮气的质量为_______ 。
(4)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:Fe(OH)3+NaOH+NaClO—Na2FeO4+NaCl+H2O
①该反应中(用化学式表示,下同),还原产物为_______ ,_______ 元素被氧化。
②配平该反应的方程式:_____________________ 。
(1)用单线桥表示反应的电子转移方向和数目:
(2)反应中发生电子转移的NH3与Cl2的分子数之比为:
(3)若反应中有3.4克氨发生氧化反应,则反应中生成氮气的质量为
(4)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:Fe(OH)3+NaOH+NaClO—Na2FeO4+NaCl+H2O
①该反应中(用化学式表示,下同),还原产物为
②配平该反应的方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下图是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。请根据你所学的知识,按要求填空:
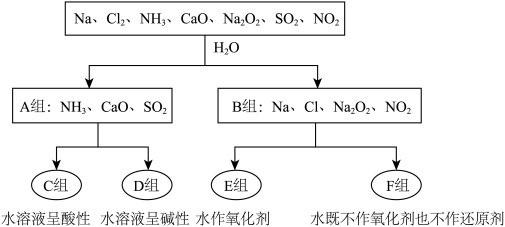
(1)根据物质与水反应的情况,分成A、B组的分类依据是________ 。
(2)A组中的CaO经常用作食品包装袋中的干燥剂,CaO所属的物质类别为________ (填序号)。
①金属氧化物②酸性氧化物③碱性氧化物④两性氧化物
(3)D组中的气体水溶液呈弱碱性,用电离方程式表示其水溶液呈弱碱性的原因:________ 。
(4)F组中与水反应,氧化剂与还原剂的物质的量之比为1∶1的物质是________ 。(填化学式)。
(5)过量的铁粉与Cl2共热时发生反应的化学方程式为____________________ 。

(1)根据物质与水反应的情况,分成A、B组的分类依据是
(2)A组中的CaO经常用作食品包装袋中的干燥剂,CaO所属的物质类别为
①金属氧化物②酸性氧化物③碱性氧化物④两性氧化物
(3)D组中的气体水溶液呈弱碱性,用电离方程式表示其水溶液呈弱碱性的原因:
(4)F组中与水反应,氧化剂与还原剂的物质的量之比为1∶1的物质是
(5)过量的铁粉与Cl2共热时发生反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】页岩气中含有CH4、CO2、H2S等气体,是蕴藏于页岩层可供开采的天然气资源。页岩气的有效利用需要处理其中所含的CO2和H2S。
I. CO2的处理:
(1)CO2和CH4重整可制合成气(主要成分为CO、H2)。已知下列热化学反应方程式:
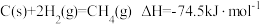
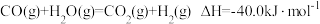

反应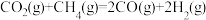 的
的
___________ 
(2)Ni催化CO2加H2形成CH4,其历程如图1所示(吸附在催化剂表面的物种用*标注),反应相同时间,含碳产物中CH4的百分含量及CO2的转化率随温度的变化如图2所示。
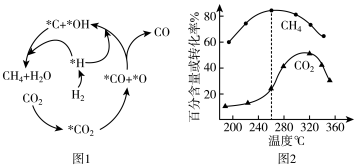
①260℃时生成主要产物所发生反应的化学方程式为___________ 。
②温度高于320℃,CO2的转化率下降的原因是___________ 。
II. H2S的处理:Fe2O3可用作脱除H2S气体的脱硫剂。Fe2O3脱硫和Fe2O3再生的可能反应机理如图3所示。
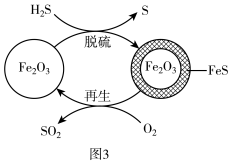
(3) Fe2O3脱硫剂的脱硫和再生过程可以描述为_______ 。
(4)再生时需控制通入O2的浓度和温度。400℃条件下,氧气浓度较大时,会出现脱硫剂再生时质量增大,且所得再生脱硫剂脱硫效果差,原因是_______ 。
(5)脱硫剂再生时可以使用水汽代替O2。700℃条件下用水汽代替O2再生时,生成Fe3O4、H2S和H2,Fe3O4也可作脱硫剂。写出水汽作用条件下脱硫剂再生反应的化学方程式:_____ 。
I. CO2的处理:
(1)CO2和CH4重整可制合成气(主要成分为CO、H2)。已知下列热化学反应方程式:
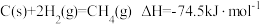
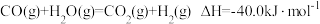

反应
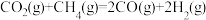 的
的

(2)Ni催化CO2加H2形成CH4,其历程如图1所示(吸附在催化剂表面的物种用*标注),反应相同时间,含碳产物中CH4的百分含量及CO2的转化率随温度的变化如图2所示。

①260℃时生成主要产物所发生反应的化学方程式为
②温度高于320℃,CO2的转化率下降的原因是
II. H2S的处理:Fe2O3可用作脱除H2S气体的脱硫剂。Fe2O3脱硫和Fe2O3再生的可能反应机理如图3所示。

(3) Fe2O3脱硫剂的脱硫和再生过程可以描述为
(4)再生时需控制通入O2的浓度和温度。400℃条件下,氧气浓度较大时,会出现脱硫剂再生时质量增大,且所得再生脱硫剂脱硫效果差,原因是
(5)脱硫剂再生时可以使用水汽代替O2。700℃条件下用水汽代替O2再生时,生成Fe3O4、H2S和H2,Fe3O4也可作脱硫剂。写出水汽作用条件下脱硫剂再生反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】二元化合物A是一种较强的还原剂,可以用次氯酸钠溶液和过量的氨气制得,64gA完全燃烧得到4.48L密度为1.25g·L—1的气体B(体积与密度均在标准状况下测定)。
(1)A的化学式___________________ 。
(2)写出次氯酸钠溶液和过量的氨气制备A的离子方程式_________________________ 。A的制备过程中氨气需要过量的理由是_____________________________________ 。
(3)A可与黑色的CuO反应生成气体B和一种砖红色的物质,写出该化学方程式__________ 。
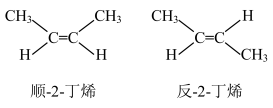
(4)已知2一丁烯存在顺反异构(如下图所示),甲基在双键同一侧的,称为顺式:甲基在双键两侧的,称为反式。现有化合物C,所含元素与A相同,摩尔质量小于A,C可通过A与等物质的量的过氧化氢恰好完全反应得到。实验表明,C可能存在两种结构,请写出它们的结构式_____________ 、_____________ 。
(1)A的化学式
(2)写出次氯酸钠溶液和过量的氨气制备A的离子方程式
(3)A可与黑色的CuO反应生成气体B和一种砖红色的物质,写出该化学方程式
(4)已知2一丁烯存在顺反异构(如下图所示),甲基在双键同一侧的,称为顺式:甲基在双键两侧的,称为反式。现有化合物C,所含元素与A相同,摩尔质量小于A,C可通过A与等物质的量的过氧化氢恰好完全反应得到。实验表明,C可能存在两种结构,请写出它们的结构式

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氢氧化铜悬浊液中存在如下平衡:
Cu(OH)2(s)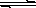 Cu2+(aq)+2OH-(aq),常温下其Ksp=2×10-20则:
Cu2+(aq)+2OH-(aq),常温下其Ksp=2×10-20则:
(1)某硫酸铜溶液里c(Cu2+)=0.02mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH大于______ 。
(2)除去CuCl2溶液中少量的Fe2+,可以按照下面的流程进行:
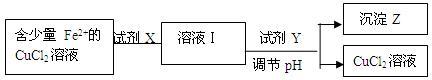
已知Fe2+、Cu2+、Fe3+三种离子开始沉淀和完全沉淀时溶液pH值如下:
①下列物质中适合作为试剂X的是___
A.H2O2 B.KMnO4 C.HNO3 D.Cl2
②加入的Y及调节的pH范围是___
A.CuCO3 3.7~4.3 B.CuO 3.7~6.4
C.NaOH 3.7~4.2 D.NH3·H2O 3.7~4.0
Cu(OH)2(s)
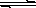 Cu2+(aq)+2OH-(aq),常温下其Ksp=2×10-20则:
Cu2+(aq)+2OH-(aq),常温下其Ksp=2×10-20则:(1)某硫酸铜溶液里c(Cu2+)=0.02mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH大于
(2)除去CuCl2溶液中少量的Fe2+,可以按照下面的流程进行:

已知Fe2+、Cu2+、Fe3+三种离子开始沉淀和完全沉淀时溶液pH值如下:
| 金属离子 | pH | |
| 开始沉淀 | 完全沉淀 | |
| Fe2+ | 7.6 | 9.6 |
| Cu2+ | 4.4 | 6.4 |
| Fe3+ | 2.7 | 3.7 |
①下列物质中适合作为试剂X的是
A.H2O2 B.KMnO4 C.HNO3 D.Cl2
②加入的Y及调节的pH范围是
A.CuCO3 3.7~4.3 B.CuO 3.7~6.4
C.NaOH 3.7~4.2 D.NH3·H2O 3.7~4.0

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求填空
(1)KAl(SO4)2的电离方程式:___________ 。
(2)NaHCO3的电离方程式:___________ 。
(3)铁与盐酸反应的离子方程式:___________ 。
(4)硫酸铜溶液与氢氧化钡溶液反应的离子方程式:___________ 。
(5)实验室制二氧化碳的反应的离子方程式:___________ 。
(6)家中用醋酸除水垢反应的离子方程式:___________ 。
(7)氧化亚铁与盐酸反应的离子方程式:___________ 。
(1)KAl(SO4)2的电离方程式:
(2)NaHCO3的电离方程式:
(3)铁与盐酸反应的离子方程式:
(4)硫酸铜溶液与氢氧化钡溶液反应的离子方程式:
(5)实验室制二氧化碳的反应的离子方程式:
(6)家中用醋酸除水垢反应的离子方程式:
(7)氧化亚铁与盐酸反应的离子方程式:
您最近一年使用:0次



