下图是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。请根据你所学的知识,按要求填空:
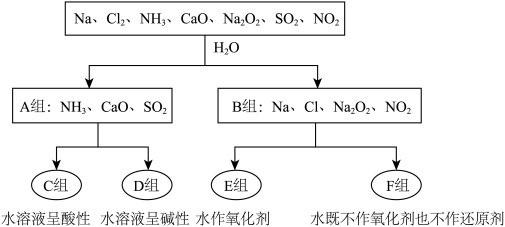
(1)根据物质与水反应的情况,分成A、B组的分类依据是________ 。
(2)A组中的CaO经常用作食品包装袋中的干燥剂,CaO所属的物质类别为________ (填序号)。
①金属氧化物②酸性氧化物③碱性氧化物④两性氧化物
(3)D组中的气体水溶液呈弱碱性,用电离方程式表示其水溶液呈弱碱性的原因:________ 。
(4)F组中与水反应,氧化剂与还原剂的物质的量之比为1∶1的物质是________ 。(填化学式)。
(5)过量的铁粉与Cl2共热时发生反应的化学方程式为____________________ 。

(1)根据物质与水反应的情况,分成A、B组的分类依据是
(2)A组中的CaO经常用作食品包装袋中的干燥剂,CaO所属的物质类别为
①金属氧化物②酸性氧化物③碱性氧化物④两性氧化物
(3)D组中的气体水溶液呈弱碱性,用电离方程式表示其水溶液呈弱碱性的原因:
(4)F组中与水反应,氧化剂与还原剂的物质的量之比为1∶1的物质是
(5)过量的铁粉与Cl2共热时发生反应的化学方程式为
更新时间:2019-02-01 18:01:03
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】W、X、Y、Z、T均是短周期元素,W和X同周期,W和Y同主族;W原子最外层电子数是内层电子数的两倍,X元素族序数是所在周期数的三倍;X的阴离子与Z的阳离子的电子层结构相同;Z的单质与X的单质在不同条件下反应,可生成Z2X或Z2X2;T和Z同周期,且T是所在周期中原子半径最小的元素。请回答:
(1)WX2的结构式是____________ 。
(2)X、Z、T离子半径由大到小的顺序为________ (用离子符号回答)。
(3)X、T的气态氢化物沸点较高的是____________ (用化学式回答),原因是____________ 。
(4)水中锰含量超标,容易使洁具和衣物染色,TX2可以用来除去水中超标的Mn2+,生成黑色沉淀。当消耗13.50g TX2时,共转移了lmol电子,则反应的离子方程式为_____________________ 。
(1)WX2的结构式是
(2)X、Z、T离子半径由大到小的顺序为
(3)X、T的气态氢化物沸点较高的是
(4)水中锰含量超标,容易使洁具和衣物染色,TX2可以用来除去水中超标的Mn2+,生成黑色沉淀。当消耗13.50g TX2时,共转移了lmol电子,则反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铅及其化合物用途非常广泛,已知铅(Pb)与硅同主族且Pb 比Si 多3个电子层。回答下列问题;
(1)铅位于元素周期表的第_________ 周期________ 族。
(2)难溶物PbSO4溶于CH3COONH4 溶液可制得(CH3COO)2Pb[(CH3COO)2Pb 易溶于水],发生的反应为PbSO4+2CH3COONH4=(CH3COO)2Pb+(NH4)2SO4,说明(CH3COO)2Pb是________________ (填“强”或“弱”)电解质。
(3)铅蓄电池充放电原理为Pb+PbO2+2H2SO4 2PbSO4 +2H2O,其中工作“B”为
2PbSO4 +2H2O,其中工作“B”为_________ (填“放电”或“充电”);电解质不能用浓盐酸,否则电池失效并放出大量的氯气,其原因是_______________________________________ (用化学方程式表示)。
(4)将PbO2 加入硝酸酸化的Mn(NO3)2溶液中,搅拌后溶液显紫红色。则每反应1mol Mn(NO3)2转移_________________ mol 电子。
(1)铅位于元素周期表的第
(2)难溶物PbSO4溶于CH3COONH4 溶液可制得(CH3COO)2Pb[(CH3COO)2Pb 易溶于水],发生的反应为PbSO4+2CH3COONH4=(CH3COO)2Pb+(NH4)2SO4,说明(CH3COO)2Pb是
(3)铅蓄电池充放电原理为Pb+PbO2+2H2SO4
 2PbSO4 +2H2O,其中工作“B”为
2PbSO4 +2H2O,其中工作“B”为(4)将PbO2 加入硝酸酸化的Mn(NO3)2溶液中,搅拌后溶液显紫红色。则每反应1mol Mn(NO3)2转移
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”。学习化学应该明白“从生活中来,到生活中去”道理。请填空:
(1)①若金属钠等活泼金属着火时,应该用___________ 来灭火。
②小苏打可治疗胃酸过多,其反应的离子反应方程式为:___________ 。
(2)火药是中国的“四大发明”之一。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑,其中被氧化的元素是___________ ,还原产物是___________ 。
(3)人体内铁元素是以Fe2+和Fe3+的形式存在。 易被人体吸收,服用维生素C,可使Fe3+转化成Fe2+,有利于人体吸收,说明维生素C具有
易被人体吸收,服用维生素C,可使Fe3+转化成Fe2+,有利于人体吸收,说明维生素C具有___________ (填“氧化性”或“还原性”)。
(4)一种测定食用盐中含碘量的化学原理如下: +I-+H+→I2+H2O。请配平:
+I-+H+→I2+H2O。请配平:___________ 。
(1)①若金属钠等活泼金属着火时,应该用
②小苏打可治疗胃酸过多,其反应的离子反应方程式为:
(2)火药是中国的“四大发明”之一。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑,其中被氧化的元素是
(3)人体内铁元素是以Fe2+和Fe3+的形式存在。
 易被人体吸收,服用维生素C,可使Fe3+转化成Fe2+,有利于人体吸收,说明维生素C具有
易被人体吸收,服用维生素C,可使Fe3+转化成Fe2+,有利于人体吸收,说明维生素C具有(4)一种测定食用盐中含碘量的化学原理如下:
 +I-+H+→I2+H2O。请配平:
+I-+H+→I2+H2O。请配平:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
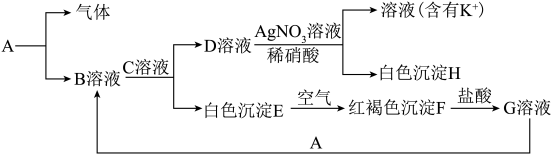
【推荐1】已知存在以下物质之间的相互转化,分别写出下列物质的化学式:A_______ 、B_______ 、C_______ 、D_______ 、E_______ 、F_______ 、G_______ 、H_______ ,并写出每步转化反应的离子方程式_______ 。

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】为探究含结晶水的化合物X(含四种元素,摩尔质量为180 g·mol-1)的组成和性质,某兴趣小组设计并完成如下实验:
请回答:
(1)黑色固体Y的化学式为________ ,气体C的电子式为________________ 。
(2)晶体X隔绝空气受热分解的化学方程式为__________________ 。

请回答:
(1)黑色固体Y的化学式为
(2)晶体X隔绝空气受热分解的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某些化学反应可表示为: A + B → C + D+H2O(未注明反应条件)请回答下列问题:
(1)若A、C、D均含氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式:
_______________________ 。
(2)若A为紫红色金属,D为红棕色气体,请写出该反应的化学方程式:
__________________________________ 。
(3)若A为不含金属元素的盐,B为碱,则检验气体C的方法是:_______________________ 。
(4)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B的组合是____________________ 。
(1)若A、C、D均含氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式:
(2)若A为紫红色金属,D为红棕色气体,请写出该反应的化学方程式:
(3)若A为不含金属元素的盐,B为碱,则检验气体C的方法是:
(4)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B的组合是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】铁酸锌( )是一种重要的磁性材料与催化剂,实验室可以通过前驱固相法制备铁酸锌,具体步骤如下:
)是一种重要的磁性材料与催化剂,实验室可以通过前驱固相法制备铁酸锌,具体步骤如下:
Ⅰ.将 与
与 溶于
溶于 水中,加热至75℃。
水中,加热至75℃。
Ⅱ.加热足量 溶液到75℃与I中溶液混合。
溶液到75℃与I中溶液混合。
Ⅲ.将混合液在90-100℃加热搅拌 ,生成固体前驱物
,生成固体前驱物 。
。
Ⅳ.待混合溶液冷却进行过滤,用冷的蒸馏水洗涤。
Ⅴ.将过滤得到的固体前驱物干燥 ,然后在700℃灼烧
,然后在700℃灼烧 ,得到产品。
,得到产品。
(1) 中铁的价态为
中铁的价态为___________ 价。
(2)步骤Ⅱ中采用的加热方式是___________ 加热。
(3)步骤Ⅳ中检验固体前驱物洗涤干净的操作和现象为___________ 。
(4)步骤Ⅴ中固体前驱物在高温下发生分解生成三种气体,气体的化学式为___________ 。
(5) 可做太阳能制氢的催化剂,过程如图所示。
可做太阳能制氢的催化剂,过程如图所示。
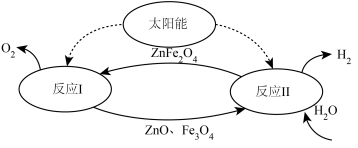
①反应Ⅰ的基本类型为___________ 。
②反应Ⅱ的氧化剂为___________ 。
③该方法制氢气与电解水制氢气相比,有哪些优点___________ 。
 )是一种重要的磁性材料与催化剂,实验室可以通过前驱固相法制备铁酸锌,具体步骤如下:
)是一种重要的磁性材料与催化剂,实验室可以通过前驱固相法制备铁酸锌,具体步骤如下:Ⅰ.将
 与
与 溶于
溶于 水中,加热至75℃。
水中,加热至75℃。Ⅱ.加热足量
 溶液到75℃与I中溶液混合。
溶液到75℃与I中溶液混合。Ⅲ.将混合液在90-100℃加热搅拌
 ,生成固体前驱物
,生成固体前驱物 。
。Ⅳ.待混合溶液冷却进行过滤,用冷的蒸馏水洗涤。
Ⅴ.将过滤得到的固体前驱物干燥
 ,然后在700℃灼烧
,然后在700℃灼烧 ,得到产品。
,得到产品。(1)
 中铁的价态为
中铁的价态为(2)步骤Ⅱ中采用的加热方式是
(3)步骤Ⅳ中检验固体前驱物洗涤干净的操作和现象为
(4)步骤Ⅴ中固体前驱物在高温下发生分解生成三种气体,气体的化学式为
(5)
 可做太阳能制氢的催化剂,过程如图所示。
可做太阳能制氢的催化剂,过程如图所示。
①反应Ⅰ的基本类型为
②反应Ⅱ的氧化剂为
③该方法制氢气与电解水制氢气相比,有哪些优点
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】亚氯酸钠(NaClO2)是一种高效的消毒剂,一种制备NaClO2晶体的流程如下:

已知:高浓度的ClO2气体易爆炸。
(1)“电解”采用无隔膜环境制备NaClO3,阴极生成的气体是___________ 。(写化学式)
(2)该流程中“制备ClO2”时,为防止ClO2气体爆炸所采取的措施是___________ 。充分反应一段时间,ClO2逸出后,溶液中主要的阴离子为___________ 。(写化学式)
(3)“吸收ClO2”时反应的离子方程式为___________ 。“吸收ClO2”时温度不能过高,原因是___________ 、___________ 。

已知:高浓度的ClO2气体易爆炸。
(1)“电解”采用无隔膜环境制备NaClO3,阴极生成的气体是
(2)该流程中“制备ClO2”时,为防止ClO2气体爆炸所采取的措施是
(3)“吸收ClO2”时反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】利用钴渣[含Co(OH)3、Fe(OH)3等]制备钴氧化物的工艺流程如下:
Co(OH)3溶解还原反应的离子方程式为____________________________________ 。铁渣中铁元素的化合价为________ 。在空气中煅烧CoC2O4生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41 g,CO2的体积为1.344 L(标准状况),则钴氧化物的化学式为________ 。

Co(OH)3溶解还原反应的离子方程式为
您最近一年使用:0次



