| 主族\周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | O |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(2)④与⑤两种元素相比较,原子半径较大的是
(3)④,⑤,⑥,⑦四种元素形成的简单离子,半径由大到小的顺序为
(4)元素①和元素⑦形成化合物属于
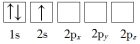
(5)由②和氢元素形成的两种多原子分子,A为10电子结构B为18电子结构,B可由A与次氯酸钠反应制得,该反应的离子方程式为:
相似题推荐
(1)最高价氧化物对应水化物碱性最强的是
(2)氧化物中具有两性的是
(3)最高价氧化物对应水化物酸性最强的是
(4)最不稳定的气态氢化物是
(5)原子半径最小的元素是
(6)金属性最强的元素是
 族 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ |
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为
(2)地壳中含量最多的金属元素是
(3)②与④形成的化合物的电子式
(4)这些元素中的最高价氧化物对应的水化物中,酸性最强的是
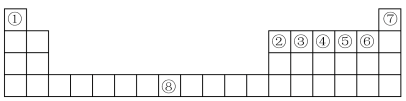
(1)根据元素原子的外围电子排布特征,元素周期表可划分为五个区域,⑦元素位于周期表的
(2)②、⑥两元素形成的化合物的空间构型为
(3)写出元素⑧基态原子的电子排布式
(4)③④⑤⑥四种元素第一电离能的由小到大的顺序为
(5)与③⑤形成的三原子化合物互为等电子体的分子为
(6)元素⑧与CO可形成的X(CO)5型化合物,该化合物常温下呈液态,熔点为−20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
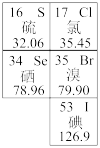
(1)市场上流行一种“富硒鸡蛋”,其中的硒是人体必需的微量元素,硒在元素周期表中的位置是:
(2)写出硒元素中子数为46的核素的符号:
(3)溴化硒(R)是一种重要的电子元件材料,其分子的球棍模型如图所示。
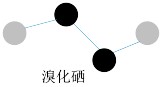
①写出该分子的电子式:
②下列说法正确的是
A.R属于离子化合物
B.离子半径:r(Se2-)>r(Cl-)
C.气态氢化物的还原性:H2Se<HCl
D.R分子中只有极性共价键
(4)下列事实不能说明溴元素的非金属性比硒元素强的是_______(填标号)。
| A.酸性:HBr>H2Se |
| B.化合物Se2Br2中硒显正价而溴显负价 |
| C.在溴水中通入H2Se,有沉淀生成 |
| D.稳定性:H2Se<HBr |
 和
和 均可作自来水消毒剂,且消毒时还原产物均为
均可作自来水消毒剂,且消毒时还原产物均为 ,则与8.7g
,则与8.7g 的氧化能力相当的
的氧化能力相当的 的质量为
的质量为(6)据报道,
 还可通过
还可通过 与足量的潮湿
与足量的潮湿 固体反应制得,写出该反应的化学方程式
固体反应制得,写出该反应的化学方程式【推荐2】1869 年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经 142 年。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的回答下列问题。

(1)元素 Ga 在元素周期表中的位置为
(2) Sn 的最高正价为
(3)根据元素周期律推断:
①阴影部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③简单氢化物的熔沸点:H2O
(4)①Se2Cl2常用作分析试剂,其电子式为
②硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是
A.原子半径:In>Se
B.In 的金属性比 Se 强
C.In 的金属性比 Al 弱
D.硒化铟的化学式为 InSe2
(5)请设计实验比较 C、Si 的非金属性强弱顺序(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和 Na2CO3溶液、硅酸钠溶液,化学仪器根据需要选择)。
实验步骤 | 实验现象与结论 |
在试管中加入 | 现象: |

(1)
 、
、 、
、 、O元素的原子半径从大到小的顺序是
、O元素的原子半径从大到小的顺序是(2)上述反应中的各物质属于共价化合物是
(3)非金属性S
 ”或“
”或“ ”)。用一个化学方程式证明硫与氧的非金属性强弱:
”)。用一个化学方程式证明硫与氧的非金属性强弱:(4)配平上述反应方程式,并标出电子转移的方向和数目。
_______
 _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
(1)反应涉及的元素原子半径从大到小的排列顺序为
(2)反应涉及的化合物中,写出属于非极性分子的结构式:
(3)氯和硫是同一周期元素,写出一个能比较氯和硫非金属性强弱的化学方程式:
(4)在一定温度下进行上述反应,若反应容器的容积为2L,3分钟后达到平衡,测得气体质量减小8.4g,则在3分钟内H2的平均反应速率为
(5)该反应的平衡常数表达式K=
(6)一定条件下,在密闭恒容器中,能表示上述反应一定达到化学平衡状态的是
a.v逆(SiCl4)=2v正(H2)
b.固体质量保持不变
c.混合气体密度保持不变
d.c(SiCl4):c(H2):c(HCl)=1:2:4
① | ② | ⑨ | ⑩ | ||||||
③ | ④ | ⑤ | ⑥ | ||||||
⑦ | ⑧ |
(1)元素⑧周期表中的位置是
(2)可利用一个化学反应比较⑥⑧非金属性的强弱,写出该反应的化学方程式
(3)②和③可形成一种化合物,能作呼吸面具中的供氧剂的。写出该化合物的电子式
(4)元素③的最高价氧化物对应水化物中含有的化学键类型为
(5)比较元素⑤⑥的最高价氧化物对应的水化物的酸性强弱
(6)比较元素③和⑨的简单离子半径大小
(7)锗为第四周期与硅同主族,根据元素周期率推测其单质、化合物的性质正确的是 。(填字母)
| A.锗的金属性比⑦强 | B.锗的原子半径比⑧大 |
| C.锗的单质可用于制半导体 | D.锗的最高正价为+3 |
(1)上述物质中互为同素异形体的是
(2)含非极性键的共价化合物是
(3)属于离子化合物的有
(4)Na2O2、HCIO、H2O2均能用于制备O2。
①HClO在光照条件下分解生成O2和HCl,用电子式表示HCl的形成过程
②写出Na2O2与H2O反应的方程式并标出电子转移方向和数目
③H2O2在二氧化锰催化作用下可以制备O2。若6.8gH2O2参加反应,则转移电子数目为
族 周期 | ⅠA | 0 | ||||||
| 一 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 二 | ② | ③ | ④ | |||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)①~⑧八种元素的最高价氧化物对应的水化物中,碱性最强的是
(3)元素④与⑦的简单气态氢化物中更稳定的是
(4)①与②形成的简单化合物的电子式为
(5)元素⑥常见氧化物溶于⑤的最高价氢氧化物水溶液的离子方程式为
(6)为了证明⑦和⑧两种元素的非金属性强弱,下列说法或实验能提供证据的是___________(填序号)。
| A.比较两种元素的单质的熔点、沸点高低 |
| B.⑦的最高价含氧酸的酸性弱于⑧的最高价含氧酸的酸性 |
| C.将⑧的单质通入⑦的简单氢化物水溶液中 |
| D.比较⑦⑧形成的简单氢化物的相对分子质量的大小 |
A.金刚石 B.HCl C.NaCl D.Na2SO4 E.Na2S F .He G.N2
请用序号回答(1)-(4)题:
(1)这些物质中只含共价键的是
(2)既含离子键又含共价键的是
(3)固态时属于离子晶体的是
(4)熔化时需克服共价键的是
(5)试写出E、G的电子式: