元素周期表在学习研究中有很重要的作用,如图是元素周期表的一部分。
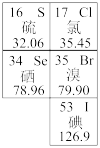
(1)市场上流行一种“富硒鸡蛋”,其中的硒是人体必需的微量元素,硒在元素周期表中的位置是:_______ 。
(2)写出硒元素中子数为46的核素的符号:_______ 。
(3)溴化硒(R)是一种重要的电子元件材料,其分子的球棍模型如图所示。
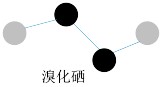
①写出该分子的电子式:_______ 。
②下列说法正确的是_______ (填标号)。
A.R属于离子化合物
B.离子半径:r(Se2-)>r(Cl-)
C.气态氢化物的还原性:H2Se<HCl
D.R分子中只有极性共价键
(4)下列事实不能说明溴元素的非金属性比硒元素强的是_______(填标号)。
(5) 和
和 均可作自来水消毒剂,且消毒时还原产物均为
均可作自来水消毒剂,且消毒时还原产物均为 ,则与8.7g
,则与8.7g 的氧化能力相当的
的氧化能力相当的 的质量为
的质量为_______ g。
(6)据报道, 还可通过
还可通过 与足量的潮湿
与足量的潮湿 固体反应制得,写出该反应的化学方程式
固体反应制得,写出该反应的化学方程式_______ 。
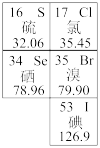
(1)市场上流行一种“富硒鸡蛋”,其中的硒是人体必需的微量元素,硒在元素周期表中的位置是:
(2)写出硒元素中子数为46的核素的符号:
(3)溴化硒(R)是一种重要的电子元件材料,其分子的球棍模型如图所示。

①写出该分子的电子式:
②下列说法正确的是
A.R属于离子化合物
B.离子半径:r(Se2-)>r(Cl-)
C.气态氢化物的还原性:H2Se<HCl
D.R分子中只有极性共价键
(4)下列事实不能说明溴元素的非金属性比硒元素强的是_______(填标号)。
| A.酸性:HBr>H2Se |
| B.化合物Se2Br2中硒显正价而溴显负价 |
| C.在溴水中通入H2Se,有沉淀生成 |
| D.稳定性:H2Se<HBr |
 和
和 均可作自来水消毒剂,且消毒时还原产物均为
均可作自来水消毒剂,且消毒时还原产物均为 ,则与8.7g
,则与8.7g 的氧化能力相当的
的氧化能力相当的 的质量为
的质量为(6)据报道,
 还可通过
还可通过 与足量的潮湿
与足量的潮湿 固体反应制得,写出该反应的化学方程式
固体反应制得,写出该反应的化学方程式
更新时间:2021-11-26 19:46:09
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下列是有水参与的反应:
①2Na+2H2O=2NaOH+H2↑ ②2Na2O2+2H2O=4NaOH+O2↑
③Na2O+H2O=2NaOH ④2H2O 2H2↑+O2↑
2H2↑+O2↑
⑤2F2+2H2O=4HF+O2
(1)其中不属于氧化还原反应的是___________ (填序号)。
(2)在这些氧化还原反应中,水只作氧化剂的反应是___________ (填序号,下同);水只作还原剂的反应是___________ 。
(3)反应④中,氧化产物与还原产物分子个数之比为___________ 。
(4)在一定条件下,RO 和
和 可发生反应:
可发生反应: ,在上述过程中RO
,在上述过程中RO 被
被___________ (填“氧化”或“还原”),RO 中R的化合价是
中R的化合价是___________ 价。
(5)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生过程:H2O2→O2。
①该反应中的氧化剂是___________ 。(填化学式,下同)
②该反应中,发生还原反应的过程是:___________ →___________ 。
(6)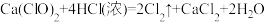 用双线桥表示反应电子转移方向和数目
用双线桥表示反应电子转移方向和数目___________ 。
①2Na+2H2O=2NaOH+H2↑ ②2Na2O2+2H2O=4NaOH+O2↑
③Na2O+H2O=2NaOH ④2H2O
 2H2↑+O2↑
2H2↑+O2↑⑤2F2+2H2O=4HF+O2
(1)其中不属于氧化还原反应的是
(2)在这些氧化还原反应中,水只作氧化剂的反应是
(3)反应④中,氧化产物与还原产物分子个数之比为
(4)在一定条件下,RO
 和
和 可发生反应:
可发生反应: ,在上述过程中RO
,在上述过程中RO 被
被 中R的化合价是
中R的化合价是(5)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生过程:H2O2→O2。
①该反应中的氧化剂是
②该反应中,发生还原反应的过程是:
(6)
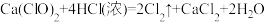 用双线桥表示反应电子转移方向和数目
用双线桥表示反应电子转移方向和数目
您最近一年使用:0次
【推荐2】(1)有以下6个反应(反应条件略):
A.2Na+2H2O=2NaOH+H2↑ B.CH4+2O2 CO2+2H2O
CO2+2H2O
C.2KClO3 2KCl+3O2↑ D.CaCO3+2HCl=CaCl2+H2O+CO2↑
2KCl+3O2↑ D.CaCO3+2HCl=CaCl2+H2O+CO2↑
E.Na2O+CO2=Na2CO3 F.CO2+C 2CO
2CO
既属于化合反应又属于氧化还原反应的有_______ (填序号,下同),不属于氧化还原反应的有_______ 。
(2)反应①H2SO3+I2+H2O=2HI+H2SO4 反应②2FeCl3+2HI=2FeCl2+I2+2HCl
请判断:H2SO3、HI、FeCl2三者还原性由强到弱的顺序为_______ 。
(3)已知实验室制备氯气的化学方程式是:_______ ,氧化产物是_______ ,有2 mol HCl发生氧化反应时共转移_______ 个电子。
A.2Na+2H2O=2NaOH+H2↑ B.CH4+2O2
 CO2+2H2O
CO2+2H2O C.2KClO3
 2KCl+3O2↑ D.CaCO3+2HCl=CaCl2+H2O+CO2↑
2KCl+3O2↑ D.CaCO3+2HCl=CaCl2+H2O+CO2↑ E.Na2O+CO2=Na2CO3 F.CO2+C
 2CO
2CO既属于化合反应又属于氧化还原反应的有
(2)反应①H2SO3+I2+H2O=2HI+H2SO4 反应②2FeCl3+2HI=2FeCl2+I2+2HCl
请判断:H2SO3、HI、FeCl2三者还原性由强到弱的顺序为
(3)已知实验室制备氯气的化学方程式是:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】钠及其化合物在生活生产中应用广泛,下面是一些它们的具体应用及反应原理。
①碳酸氢钠作食品膨松剂: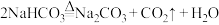
②氢化钠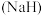 可用作野外生氢剂:
可用作野外生氢剂: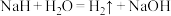
③钠单质组成“可呼吸”的 充电电池:
充电电池: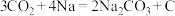
④饱和食盐水作侯氏制碱原料: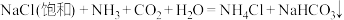
⑤电解饱和食盐水制备氯气和氢氧化钠(氯碱工业):
⑥高铁酸钠 可同时消毒和净水:
可同时消毒和净水: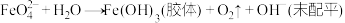
回答下列问题:
(1)以上反应中不属于氧化还原反应的是___________ (填标号)。
(2)钠是一种很活泼的金属,可用石蜡封存,实验室少量 保存于
保存于___________ 中(填字母)。
A.细沙 B.水 C.煤油
(3)野外生氢剂 中氢元素的化合价为
中氢元素的化合价为___________ 价,常用作___________ (填“氧化剂”或“还原剂”)。
(4)“可呼吸” 充电电池消耗
充电电池消耗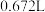 (标准状况)
(标准状况) 气体时,转移电子数为
气体时,转移电子数为_____  。
。
(5)氯碱工业生产中会使用阳离子交换膜,目的之一是将 溶液和
溶液和 分隔开,若未分隔开,两者会发生反应,该反应的化学反应方程式为
分隔开,若未分隔开,两者会发生反应,该反应的化学反应方程式为___________ 。
(6)请配平高铁酸钠 (
( 为
为 价)在水中发生反应的离子反应方程式:
价)在水中发生反应的离子反应方程式:___________ 。
并比较氧化性强弱:
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
①碳酸氢钠作食品膨松剂:
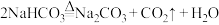
②氢化钠
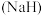 可用作野外生氢剂:
可用作野外生氢剂: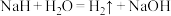
③钠单质组成“可呼吸”的
 充电电池:
充电电池: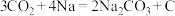
④饱和食盐水作侯氏制碱原料:
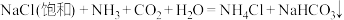
⑤电解饱和食盐水制备氯气和氢氧化钠(氯碱工业):

⑥高铁酸钠
 可同时消毒和净水:
可同时消毒和净水: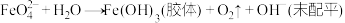
回答下列问题:
(1)以上反应中不属于氧化还原反应的是
(2)钠是一种很活泼的金属,可用石蜡封存,实验室少量
 保存于
保存于A.细沙 B.水 C.煤油
(3)野外生氢剂
 中氢元素的化合价为
中氢元素的化合价为(4)“可呼吸”
 充电电池消耗
充电电池消耗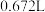 (标准状况)
(标准状况) 气体时,转移电子数为
气体时,转移电子数为 。
。(5)氯碱工业生产中会使用阳离子交换膜,目的之一是将
 溶液和
溶液和 分隔开,若未分隔开,两者会发生反应,该反应的化学反应方程式为
分隔开,若未分隔开,两者会发生反应,该反应的化学反应方程式为(6)请配平高铁酸钠
 (
( 为
为 价)在水中发生反应的离子反应方程式:
价)在水中发生反应的离子反应方程式:
并比较氧化性强弱:

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】绿水青山,保护环境是当社会发展必须关注的重要课题。氮氧化物和硫氧化物是造成大气污染的主要原因之一,消除氮氧化物有多种方法。
(1)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示:
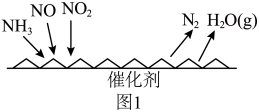
①氮氧化物会带来什么污染___________ (回答任一点);NH3与NO2反应的化学方程式___________ 。
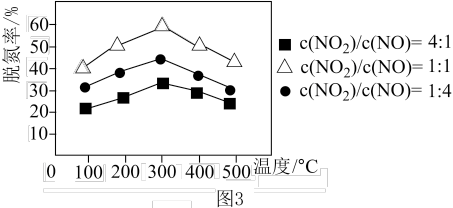
②用Fe做催化剂时,在氨气足量的情况下,不同 对应的脱氮率如图3所示,脱氮效果最佳的
对应的脱氮率如图3所示,脱氮效果最佳的 =
=___________ 。
(2)利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的亚硝酸钙Ca(NO2)2其部分工艺流程如图:
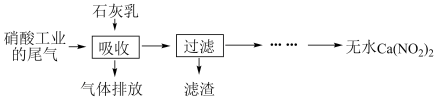
①上述工艺流程中采用气-液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋)法,其目的是___________ ;
②生产中溶液需保持弱碱性。在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,其反应的离子方程式为___________ 。
(3)氢能是可循环利用的清洁能源,在2020年上海进博会展览中,诸多氢能源汽车纷纷亮相。氢-氧燃料电池被誉为氢能源汽车的心脏。某种氢-氧燃料电池的内部结构如图,
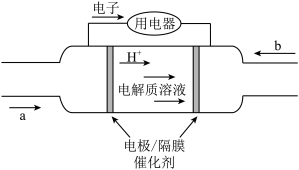

根据原电池的原理,回答下问题:
①a通入的是___________ 。
②右侧的电极反应式为___________ 。
(1)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示:

①氮氧化物会带来什么污染
②用Fe做催化剂时,在氨气足量的情况下,不同
 对应的脱氮率如图3所示,脱氮效果最佳的
对应的脱氮率如图3所示,脱氮效果最佳的 =
=
(2)利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的亚硝酸钙Ca(NO2)2其部分工艺流程如图:

①上述工艺流程中采用气-液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋)法,其目的是
②生产中溶液需保持弱碱性。在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,其反应的离子方程式为
(3)氢能是可循环利用的清洁能源,在2020年上海进博会展览中,诸多氢能源汽车纷纷亮相。氢-氧燃料电池被誉为氢能源汽车的心脏。某种氢-氧燃料电池的内部结构如图,


根据原电池的原理,回答下问题:
①a通入的是
②右侧的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】2019年是“国际化学元素周期表年”。元素周期表中的成员数不断增加,ⅤA族元素是元素周期表中的重要组成元素。
(1)2016年 确认了四种新元素,其中之一为
确认了四种新元素,其中之一为 ,中文名为“镆”,位于第七周期ⅤA族,
,中文名为“镆”,位于第七周期ⅤA族,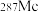 与
与 互为
互为______ 。
(2) 的同族元素氮的氧化物是大气中的主要污染物,常用氧化还原法消除,其中一种方法是:
的同族元素氮的氧化物是大气中的主要污染物,常用氧化还原法消除,其中一种方法是: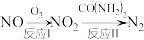
① 的电子式为
的电子式为______ ;反应Ⅰ为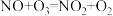 ,其中还原产物为
,其中还原产物为______ ;每消除 ,转移电子
,转移电子______  。
。
②反应Ⅱ中氧化产物与还原产物的质量比为______ 。
(3)①三碘化磷( )是一种强还原剂和脱氧剂,它遇水能水解生成亚磷酸和氢碘酸。实验室中可由白磷(
)是一种强还原剂和脱氧剂,它遇水能水解生成亚磷酸和氢碘酸。实验室中可由白磷( )与
)与 在
在 溶剂中反应制得。该反应的化学方程式为
溶剂中反应制得。该反应的化学方程式为______ 。制备时常在溶剂中加入 ,其作用是
,其作用是______ 。
②亚磷酸( )是一种中强酸,与足量的
)是一种中强酸,与足量的 溶液反应生成
溶液反应生成 和
和 。
。 属于
属于______ 元酸(填“一”“二”或“三”), 属于
属于______ (填“正盐”或“酸式盐”)。亚磷酸具有强还原性,能与 溶液反应置换出
溶液反应置换出 ,写出其离子反应方程式
,写出其离子反应方程式______ 。
(1)2016年
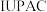 确认了四种新元素,其中之一为
确认了四种新元素,其中之一为 ,中文名为“镆”,位于第七周期ⅤA族,
,中文名为“镆”,位于第七周期ⅤA族, 与
与 互为
互为(2)
 的同族元素氮的氧化物是大气中的主要污染物,常用氧化还原法消除,其中一种方法是:
的同族元素氮的氧化物是大气中的主要污染物,常用氧化还原法消除,其中一种方法是: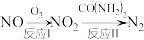
①
 的电子式为
的电子式为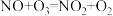 ,其中还原产物为
,其中还原产物为 ,转移电子
,转移电子 。
。②反应Ⅱ中氧化产物与还原产物的质量比为
(3)①三碘化磷(
 )是一种强还原剂和脱氧剂,它遇水能水解生成亚磷酸和氢碘酸。实验室中可由白磷(
)是一种强还原剂和脱氧剂,它遇水能水解生成亚磷酸和氢碘酸。实验室中可由白磷( )与
)与 在
在 溶剂中反应制得。该反应的化学方程式为
溶剂中反应制得。该反应的化学方程式为 ,其作用是
,其作用是②亚磷酸(
 )是一种中强酸,与足量的
)是一种中强酸,与足量的 溶液反应生成
溶液反应生成 和
和 。
。 属于
属于 属于
属于 溶液反应置换出
溶液反应置换出 ,写出其离子反应方程式
,写出其离子反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请完成以下各空:
(1)食盐不慎洒落在天然气的火焰上,观察的现象是____ 。
(2)厨房中的调味品,①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。主要成分中属于盐类的是____ (填序号);
(3)铝合金具有广泛的用途,但铝制器具不宜盛放碱性食物,其请写出该反应的离子方程式____ 。若生成6.72 L气体(标准状况),则消耗铝的质量为____ g。
(4)已知: ,则该反应中氧化剂与还原剂的质量比为
,则该反应中氧化剂与还原剂的质量比为____ 。
(5)Mn2+、Bi3+、 、
、 、
、 、H2O组成的一个氧化还原反应体系中,发生
、H2O组成的一个氧化还原反应体系中,发生 的反应过程。
的反应过程。
①该反应中,被氧化的元素是____ (填元素符号)。
②将以上物质分别填入下面对应的横线上,组成一个配平的离子方程式:_____ 。
(6)过氧化钙性质类似于过氧化钠,请写出过氧化钙与水反应的方程式:____ 。
(1)食盐不慎洒落在天然气的火焰上,观察的现象是
(2)厨房中的调味品,①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。主要成分中属于盐类的是
(3)铝合金具有广泛的用途,但铝制器具不宜盛放碱性食物,其请写出该反应的离子方程式
(4)已知:
 ,则该反应中氧化剂与还原剂的质量比为
,则该反应中氧化剂与还原剂的质量比为(5)Mn2+、Bi3+、
 、
、 、
、 、H2O组成的一个氧化还原反应体系中,发生
、H2O组成的一个氧化还原反应体系中,发生 的反应过程。
的反应过程。①该反应中,被氧化的元素是
②将以上物质分别填入下面对应的横线上,组成一个配平的离子方程式:
(6)过氧化钙性质类似于过氧化钠,请写出过氧化钙与水反应的方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下表是元素周期表中的一部分,根据表中给出的10种元素,回答下列问题:
(1)元素f的原子结构示意图为___________ 。
(2)元素g位于元素周期表中第___________ 周期第___________ 族。
(3)元素b有多种同素异形体,写出其中两种的名称___________ 、___________ 。
(4)元素h的最高价氧化物对应水化物的化学式为___________ 。
(5)元素a~j中非金属性最强的是___________ (填元素符号)。
(6)按物质的性质分类,元素i的氧化物属于___________ 氧化物。
(7)e单质和水反应的离子方程式为___________ 。
(8)有3位科学家因在基于a的电池研究方面的成就获得了2019年诺贝尔化学奖。基于e的电池也日益受到重视。下列关于a和e的说法不正确的有___________ (填字母序号)。
A.a的金属性比e强 B.a的原子半径比e大
C.自然界中,e的储量比a高 D.基于a的电池质量轻、易携带
| a | b | c | d | ||||||||||||||
| e | f | g | h | ||||||||||||||
| i | j |
(1)元素f的原子结构示意图为
(2)元素g位于元素周期表中第
(3)元素b有多种同素异形体,写出其中两种的名称
(4)元素h的最高价氧化物对应水化物的化学式为
(5)元素a~j中非金属性最强的是
(6)按物质的性质分类,元素i的氧化物属于
(7)e单质和水反应的离子方程式为
(8)有3位科学家因在基于a的电池研究方面的成就获得了2019年诺贝尔化学奖。基于e的电池也日益受到重视。下列关于a和e的说法不正确的有
A.a的金属性比e强 B.a的原子半径比e大
C.自然界中,e的储量比a高 D.基于a的电池质量轻、易携带
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下表是元素周期表的一部分。
(1)表中原子半径最小的元素符号是____ ;
(2)表中氧化性最强的单质的化学式为____ ;
(3)表中最高价氧化物的水化物中碱性最强的物质的化学式是__ ,酸性最强的物质的化学式是_______ ;
(4)④⑤⑥三种元素中,离子半径大小的顺序为____ >____ >____ (填离子符号);
(5)③⑦⑧三种元素的气态氢化物的稳定性强弱顺序为__ >__ >___ (填化学式);
(6)元素②的氢化物与元素⑧的氢化物反应的化学方程式为________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
1 | ① | ||||||
2 | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
(1)表中原子半径最小的元素符号是
(2)表中氧化性最强的单质的化学式为
(3)表中最高价氧化物的水化物中碱性最强的物质的化学式是
(4)④⑤⑥三种元素中,离子半径大小的顺序为
(5)③⑦⑧三种元素的气态氢化物的稳定性强弱顺序为
(6)元素②的氢化物与元素⑧的氢化物反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Na2S 常用作皮革脱毛剂,工业上用反应 Na2SO4 +2C Na2S+2CO2↑ 进行制取。
Na2S+2CO2↑ 进行制取。
完成下列填空:
(1)硫元素在周期表中的位置为______________ 。上述反应中涉及的各元素中原子半径最小的是
__________ (填元素符号)。写出硫化钠的电子式:___________ 。
(2)用上述反应中涉及的元素,写出一个含有非极性键的化合物的化学式。_____________
(3)写出一个能比较 S 和 O 非金属性强弱的化学事实。________________________________
(4)在 2L 的容器内发生上述反应,2 小时内共生成 78 g 硫化钠,则这段时间内用二氧化碳表示的平均反应速率为______________ mol/(L·h) 。
(5)将硫化钠溶液滴入氯化铝溶液中,产生白色沉淀,同时有臭鸡蛋气味的气体生成,用平衡移动原理解
释上述现象。______________________________
 Na2S+2CO2↑ 进行制取。
Na2S+2CO2↑ 进行制取。完成下列填空:
(1)硫元素在周期表中的位置为
(2)用上述反应中涉及的元素,写出一个含有非极性键的化合物的化学式。
(3)写出一个能比较 S 和 O 非金属性强弱的化学事实。
(4)在 2L 的容器内发生上述反应,2 小时内共生成 78 g 硫化钠,则这段时间内用二氧化碳表示的平均反应速率为
(5)将硫化钠溶液滴入氯化铝溶液中,产生白色沉淀,同时有臭鸡蛋气味的气体生成,用平衡移动原理解
释上述现象。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氧、碳等非金属元素形成的物质种类繁多、性状各异。
(1)氧、氟、氮三种元素都可形成简单离子,它们的离子半径最小的是___________ (填离子符号),硅元素在元素周期表中的位置是___________ 。CO2和SiO2是同一主族元素的最高正价氧化物,常温下CO2为气体,SiO2为高熔点固体。请分析原因:___________ 。
(2)比较硫和氯性质的强弱。热稳定性H2S___________ HCl(选填“<”、“>”或“=”,下同);酸性:HClO4___________ H2SO4。用一个离子方程式说明氯元素和硫元素非金属性的相对强弱:___________ 。
(3)红酒中添加一定量的SO2 可以防止酒液氧化,这利用了SO2 的___________ 性。若将SO2气体通入H2S水溶液中直至过量,下列表示溶液的pH随通入SO2气体体积变化的示意图正确的是___________ (填序号)。
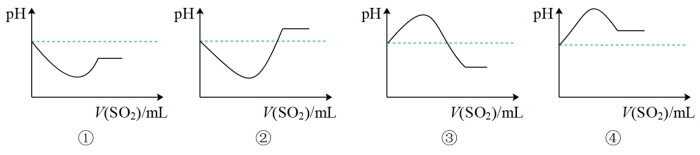
已知NaHSO3溶液呈酸性,而HSO 既能电离又能水解。则在NaHSO3溶液中c(H2SO3)
既能电离又能水解。则在NaHSO3溶液中c(H2SO3)___________ c(SO )(选填“<”、“>”或“=”) 。
)(选填“<”、“>”或“=”) 。
(4)亚硫酸钠和碘酸钾在酸性条件下反应生成硫酸钠、硫酸钾、碘和水,配平该反应方程式_____
___Na2SO3+____KIO3+____H2SO4 _____Na2SO4+____K2SO4+______I2+_____ H2O
_____Na2SO4+____K2SO4+______I2+_____ H2O
(1)氧、氟、氮三种元素都可形成简单离子,它们的离子半径最小的是
(2)比较硫和氯性质的强弱。热稳定性H2S
(3)红酒中添加一定量的SO2 可以防止酒液氧化,这利用了SO2 的

已知NaHSO3溶液呈酸性,而HSO
 既能电离又能水解。则在NaHSO3溶液中c(H2SO3)
既能电离又能水解。则在NaHSO3溶液中c(H2SO3) )(选填“<”、“>”或“=”) 。
)(选填“<”、“>”或“=”) 。(4)亚硫酸钠和碘酸钾在酸性条件下反应生成硫酸钠、硫酸钾、碘和水,配平该反应方程式
___Na2SO3+____KIO3+____H2SO4
 _____Na2SO4+____K2SO4+______I2+_____ H2O
_____Na2SO4+____K2SO4+______I2+_____ H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表中的一部分。
根据A—J在周期表中的位置,用元素符号、化学式或反应式 回答下列问题:
(1)氧化性最强的单质是___ ,用一个化学反应证明H单质的氧化性强于G单质__________ 。
(2)A分别与F、G、H形成的简单化合物中,稳定性由强到弱的顺序为_________ 。
(3)B、C、G、H离子半径由大到小的顺序是_________ 。
(4)D单质可用来制造D—空气燃料电池,该电池通常以氯化钠或氢氧化钾溶液为电解质溶液,通入空气的电极为正极。若以氯化钠为电解质溶液时,正极的反应式为______ 。若以氢氧化钾溶液为电解质溶液时,电池的总反应式为____ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | A | |||||||
| 2 | E | F | G | H | J | |||
| 3 | B | C | D | I |
(1)氧化性最强的单质是
(2)A分别与F、G、H形成的简单化合物中,稳定性由强到弱的顺序为
(3)B、C、G、H离子半径由大到小的顺序是
(4)D单质可用来制造D—空气燃料电池,该电池通常以氯化钠或氢氧化钾溶液为电解质溶液,通入空气的电极为正极。若以氯化钠为电解质溶液时,正极的反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】元素在周期表中的位置,反映了元素的原子结构和元素的性质。下图是元素周期表的一部分。
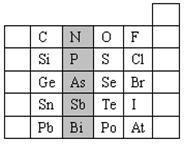
(1)阴影部分元素N的最高价氧化物为______ 。根据元素周期律,请你预测:H3AsO4、H3PO4 的酸性强弱:H3AsO4______ H3PO4。(用“>”、“<”或“=”表示)
(2)元素S的最高正价和最低负价分别为______ 、______ ,
(3)在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断在相同条件下Se与H2反应的限度______ (选填“更大”、“更小”或“相同”)。
(4)羰基硫(COS)分子结构与二氧化碳分子结构相似,所有原子的最外层都满足8电子结构。请写出羰基硫分子的电子式______
(5)单质砷和热的浓H2SO4反应,生成As2O3,反应的化学方程式为______ ;

(1)阴影部分元素N的最高价氧化物为
(2)元素S的最高正价和最低负价分别为
(3)在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断在相同条件下Se与H2反应的限度
(4)羰基硫(COS)分子结构与二氧化碳分子结构相似,所有原子的最外层都满足8电子结构。请写出羰基硫分子的电子式
(5)单质砷和热的浓H2SO4反应,生成As2O3,反应的化学方程式为
您最近一年使用:0次



