科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似。已知断裂1molN—N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,则


| A.1molN4气体转化为N2时要吸收217kJ能量 | B.N4是N2的同位素 |
| C.1molN4气体转化为N2时要放出724kJ能量 | D.N4是一种新型化合物 |
更新时间:2018-08-29 14:21:47
|
相似题推荐
【推荐1】下列有关热化学方程式的叙述中正确的是
A.中和热的离子方程式为:  |
B.已知  , ,  则 则 |
C.已知  ,则 ,则 的摩尔燃烧焓为 的摩尔燃烧焓为 |
D.已知C(石墨,s) C(金刚石,s) C(金刚石,s)  ,则金刚石比石墨稳定 ,则金刚石比石墨稳定 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】已知化学反应:C(s)+ O2(g)=CO(g) ΔH1<0
O2(g)=CO(g) ΔH1<0
CO(g)+ O2(g)=CO2(g) ΔH2<0
O2(g)=CO2(g) ΔH2<0
C(s)+O2(g)=CO2(g) ΔH3<0
下列说法正确的是
 O2(g)=CO(g) ΔH1<0
O2(g)=CO(g) ΔH1<0CO(g)+
 O2(g)=CO2(g) ΔH2<0
O2(g)=CO2(g) ΔH2<0C(s)+O2(g)=CO2(g) ΔH3<0
下列说法正确的是
| A.56 g CO和32 g O2所具有的总能量小于88 g CO2所具有的总能量 |
| B.碳的燃烧热是ΔH3 |
| C.ΔH1<ΔH3 |
| D.28 g CO的总能量比44 g CO2的总能量高 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】工业制氢气的一个重要反应是CO(g)+H2O(g)=CO2(g)+H2(g)。已知在25 ℃时:
①C(石墨)+1/2O2(g)=CO(g) ΔH1=-111 kJ/mol;
②H2(g)+1/2O2(g)=H2O(g) ΔH2=-242 kJ/mol;
③C(石墨)+O2(g)=CO2(g) ΔH3=-394 kJ/mol。
则25 ℃时,CO2(g)+H2(g)=CO(g)+H2O(g) ΔH= ( )
①C(石墨)+1/2O2(g)=CO(g) ΔH1=-111 kJ/mol;
②H2(g)+1/2O2(g)=H2O(g) ΔH2=-242 kJ/mol;
③C(石墨)+O2(g)=CO2(g) ΔH3=-394 kJ/mol。
则25 ℃时,CO2(g)+H2(g)=CO(g)+H2O(g) ΔH= ( )
| A.+41 kJ/mol | B.-41 kJ/mol | C.-283 kJ/mol | D.-131 kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】科学家最新发现,通过简单的化学反应,可以将树木纤维素转变成超级储能装置,如图是该反应的微观示意图,下列说法错误的是
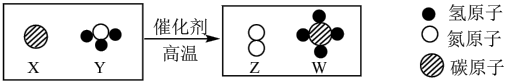
| A.该反应过程伴有能量变化 |
| B.该反应前后原子的种类、个数、质量均保持不变 |
| C.反应物X的能量低于生成物W的能量 |
| D.断裂反应物(X+Y)中化学键吸收能量,形成生成物(Z+W)中化学键释放能量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】将盛有NH4HCO3,粉末的小烧杯放入盛有少量醋酸的大烧杯中,然后向小烧杯中加入盐酸,大烧杯中醋酸逐渐凝固。由此判断,下列说法正确的是
| A.小烧杯中的反应是放热反应 |
| B.小烧杯中的反应是吸热反应 |
| C.小烧杯中发生的反应中反应物的总能量高于生成物的总能量 |
| D.该实验说明放热反应无需加热就能进行 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】生石灰遇水生成熟石灰,下列对此反应过程中化学键变化的判断正确的是
| A.断裂离子键和共价键,形成离子键和共价键 | B.只断裂离子键,形成离子键和共价键 |
| C.只断裂共价键,形成共价键 | D.离子键和共价键在反应前后没有变化 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】 与
与 在铁催化剂表面合成
在铁催化剂表面合成 的反应历程如图所示,则下列说法正确的是
的反应历程如图所示,则下列说法正确的是

 与
与 在铁催化剂表面合成
在铁催化剂表面合成 的反应历程如图所示,则下列说法正确的是
的反应历程如图所示,则下列说法正确的是
| A.Ⅰ中破坏的均为极性键 |
B.Ⅳ中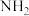 与 与 生成 生成 |
| C.Ⅱ、Ⅲ、Ⅳ均为放热过程 |
D.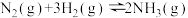 为吸热反应 为吸热反应 |
您最近一年使用:0次

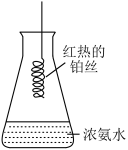
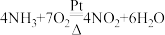
 的化学反应,能量关系如下图,下列叙述正确的是
的化学反应,能量关系如下图,下列叙述正确的是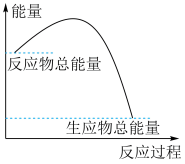
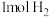 所含的能量
所含的能量

