现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、C、H,它们之间能发生如下图的反应(图中有些反应的产物和反应的条件没有全部标出)。
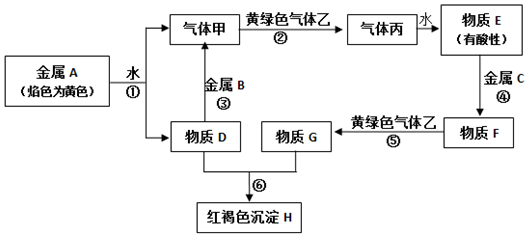
请根据以上信息回答下列问题:
(1)写出下列物质化学式:A_____ 、B_____ 、C____ 、F____ 、H_____ 、乙____ 。
(2)写出下列反应的化学方程式:
反应①______________________________ 。
反应③________________________________ 。
反应⑤_________________________________ 。
(3)物质G中的阳离子如何检验____________________________ 。

请根据以上信息回答下列问题:
(1)写出下列物质化学式:A
(2)写出下列反应的化学方程式:
反应①
反应③
反应⑤
(3)物质G中的阳离子如何检验
更新时间:2018-09-05 10:39:08
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】1.A、B、C、D四种物质之间有如图所示的转化关系。已知:A是空气中的主要成分之一,B、C、D均为化合物,且C为一种红棕色气体。
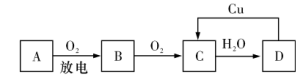
请回答下列问题:
(1)写出B的化学式:___ 。
(2)在D→C的过程中,D表现出强___ (填“氧化性”或“还原性”)。
(3)写出C→D的化学方程式:___ 。
2.汽车尾气中含有NO,在汽车尾气排放管中安装一个“催化转换器”(用铂、钯合金作催化剂),可将尾气中另一种有害气体CO跟NO反应转化为无毒气体。写出CO与NO反应的化学方程式:___ 。
3.控制或者减少城市汽车尾气污染的方法还可以有___ 。
a.开发氢能源 b.使用电动车 c.使用含铅汽油 d.严禁车辆行驶

请回答下列问题:
(1)写出B的化学式:
(2)在D→C的过程中,D表现出强
(3)写出C→D的化学方程式:
2.汽车尾气中含有NO,在汽车尾气排放管中安装一个“催化转换器”(用铂、钯合金作催化剂),可将尾气中另一种有害气体CO跟NO反应转化为无毒气体。写出CO与NO反应的化学方程式:
3.控制或者减少城市汽车尾气污染的方法还可以有
a.开发氢能源 b.使用电动车 c.使用含铅汽油 d.严禁车辆行驶
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】A、B、C、D四种物质之间有下图所示的转化关系,A是一种淡黄色的非金属单质;B、C、D均为化合物;B是形成酸雨的主要成分之一;D是三大强酸之一。

请回答下列问题:
(1)化合物B是___ (填化学式,下同),化合物D是___ 。
(2)B→C化学反应的类型是___ 反应(填“化合”、“分解”、“置换”或“复分解”)。
(3)向D的稀溶液中滴加BaCl2溶液,能产生白色沉淀。写出该反应的离子方程式:____ 。

请回答下列问题:
(1)化合物B是
(2)B→C化学反应的类型是
(3)向D的稀溶液中滴加BaCl2溶液,能产生白色沉淀。写出该反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】含氯消毒剂、医用酒精、过氧化物等均能有效灭活病毒,为抗击新型冠状肺炎(COVID-19)作出了贡献。请回答下列问题:
(1)下列物质用作消毒剂时,原理与其它不同的是___________ (填字母)。
A.NaClO B.ClO2 C.医用酒精 D.H2O2
(2)兴趣小组欲探究过氧化钠样品是否变质,进行下列操作:取少量样品,溶解,加入___________ ,振荡,有白色沉淀产生,证明Na2O2已变质。
(3)亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂,可由ClO2与Cl2O按一定比例混合后在NaOH溶液中反应制得。
①NaClO2中氯元素的化合价是___________ 。
②制备时Cl2O与ClO2完全反应的物质的量理论比为___________ 。
(4)兴趣小组设计如下图实验装置制取少量漂白液

①MnO2与浓盐酸反应的离子方程式为___________ 。
②充分反应后,测得漂白液中NaClO质量分数偏低。经分析可能的原因有:
I.___________ (用文字简述)。
Ⅱ.氯气与NaOH反应放热,温度较高时生成NaClO3,该反应方程式为___________ 。
(1)下列物质用作消毒剂时,原理与其它不同的是
A.NaClO B.ClO2 C.医用酒精 D.H2O2
(2)兴趣小组欲探究过氧化钠样品是否变质,进行下列操作:取少量样品,溶解,加入
(3)亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂,可由ClO2与Cl2O按一定比例混合后在NaOH溶液中反应制得。
①NaClO2中氯元素的化合价是
②制备时Cl2O与ClO2完全反应的物质的量理论比为
(4)兴趣小组设计如下图实验装置制取少量漂白液

①MnO2与浓盐酸反应的离子方程式为
②充分反应后,测得漂白液中NaClO质量分数偏低。经分析可能的原因有:
I.
Ⅱ.氯气与NaOH反应放热,温度较高时生成NaClO3,该反应方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】K2FeO4为暗紫色有光泽的粉末,是一种新型绿色消毒剂,在实验室通过两步操作制备K2FeO4。回答下列问题:
Ⅰ.制备KClO,装置如下:
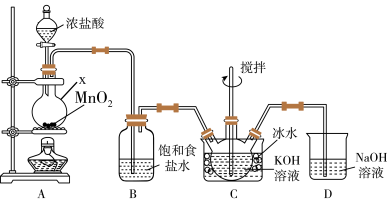
(1)仪器x的名称为___________ ,x中反应的化学方程式为___________ 。
(2)装置B的作用为___________ ;装置C中Cl2与KOH反应得到KClO,该反应离子方程式为___________ 。
(3)装置D的作用为___________ 。
Ⅱ.制备K2FeO4:
(4)待装置C中得到足量KClO后,将三口烧瓶上的导管取下,依次加入适量KOH溶液、Fe(NO3)3溶液并搅拌,控制水浴温度为25 ℃,得到紫色K2FeO4溶液,反应的离子方程式为 。该过程中每制备1 mol K2FeO4,转移电子数目为
。该过程中每制备1 mol K2FeO4,转移电子数目为___________ (用NA表示阿伏加德罗常数的值)。
Ⅰ.制备KClO,装置如下:

(1)仪器x的名称为
(2)装置B的作用为
(3)装置D的作用为
Ⅱ.制备K2FeO4:
(4)待装置C中得到足量KClO后,将三口烧瓶上的导管取下,依次加入适量KOH溶液、Fe(NO3)3溶液并搅拌,控制水浴温度为25 ℃,得到紫色K2FeO4溶液,反应的离子方程式为
 。该过程中每制备1 mol K2FeO4,转移电子数目为
。该过程中每制备1 mol K2FeO4,转移电子数目为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】回答下列问题
Ⅰ、在探究金属钠与水反应的实验过程中,某课外小组同学记录了如下实验现象和实验结论:
①有碱生成 ②溶液变红 ③钠四处游动 ④钠浮在水面上 ⑤有气体产生 ⑥钠的密度比水小 ⑦钠熔成光亮的小球 ⑧反应放热,钠熔点低
(1)请填写下表中的空格(从①___________ ⑧中选择,填序号):
(2)写出钠与水反应的离子方程式___________ 。
Ⅱ、如图为实验室用软锰矿制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条; 中为红色的铜网,其右端出气管口放有脱脂棉。
中为红色的铜网,其右端出气管口放有脱脂棉。
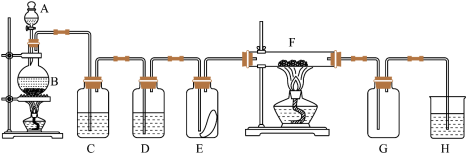
(3)B中反应的化学方程式为___________ ;若制得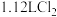 体积(标准状况下),则被氧化的HCl
体积(标准状况下),则被氧化的HCl_________ mol,反应中转移电子的物质的量为___________  。
。
(4)装置C中盛装的溶液是___________ ,D中试剂的作用是___________ 。
(5)H用来吸收多余氯气。工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白精,该反应的化学方程式为___________ 。
Ⅰ、在探究金属钠与水反应的实验过程中,某课外小组同学记录了如下实验现象和实验结论:
①有碱生成 ②溶液变红 ③钠四处游动 ④钠浮在水面上 ⑤有气体产生 ⑥钠的密度比水小 ⑦钠熔成光亮的小球 ⑧反应放热,钠熔点低
(1)请填写下表中的空格(从①
| 实验现象 | ⑦ | ③ | ||
| 实验结论 | ⑥ | ① |
(2)写出钠与水反应的离子方程式
Ⅱ、如图为实验室用软锰矿制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条;
 中为红色的铜网,其右端出气管口放有脱脂棉。
中为红色的铜网,其右端出气管口放有脱脂棉。
(3)B中反应的化学方程式为
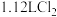 体积(标准状况下),则被氧化的HCl
体积(标准状况下),则被氧化的HCl 。
。(4)装置C中盛装的溶液是
(5)H用来吸收多余氯气。工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白精,该反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】目前,世界上多采用电解熔融氯化钠的方法来生产金属钠:2NaCl(熔融) 2Na+Cl2↑。已知物质A、B、C、D、E、F有如图转化关系:
2Na+Cl2↑。已知物质A、B、C、D、E、F有如图转化关系:
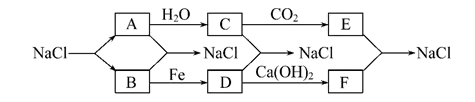
(1)试根据上述变化写出下列物质的化学式:
A_______ ,B_________ ,D________ ,E________
(2)请写出下列反应的化学方程式:
C+D→NaCl:__________
E+F→NaCl:___________
(3)若把A投入盛有CuSO4溶液的烧杯中,烧杯中的现象是______ ;烧杯中反应的化学方程式有_______
(4)工业上常用B和C反应制取“84”消毒液,写出该反应的化学方程式:_______
 2Na+Cl2↑。已知物质A、B、C、D、E、F有如图转化关系:
2Na+Cl2↑。已知物质A、B、C、D、E、F有如图转化关系:
(1)试根据上述变化写出下列物质的化学式:
A
(2)请写出下列反应的化学方程式:
C+D→NaCl:
E+F→NaCl:
(3)若把A投入盛有CuSO4溶液的烧杯中,烧杯中的现象是
(4)工业上常用B和C反应制取“84”消毒液,写出该反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】实验室里常用Na2O2与H2O反应快速制取少量的O2,下面装置用来制取O2并演示Na在O2中的燃烧实验。

(1)关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴,直至全部流入试管。试判断装置是否漏气________ (填“漏气”“不漏气”或“无法确定”),判断理由是__________________________ 。
(2)写出A装置中反应的化学方程式_______________________ 。
(3)B装置中盛放的试剂是____________ ,其作用是________________ ;
D装置中盛放的试剂是_______ ,作用是_________________________ 。
(4)C装置中观察到的现象是____________________________________ 。

A B C
(1)关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴,直至全部流入试管。试判断装置是否漏气
(2)写出A装置中反应的化学方程式
(3)B装置中盛放的试剂是
D装置中盛放的试剂是
(4)C装置中观察到的现象是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】物质A、B、C、D、E、F、G、H、I、J、K有如图所示转化关系,其中气体D、E为单质,试回答:
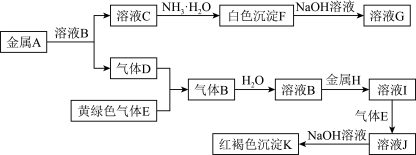
(1)写出下列物质的化学式:A是_______ ,D是_______ , E是_______ 。
(2)写出反应“C→F”的离子方程式:_______ ;
(3)在溶液I中滴入NaOH溶液,可观察到的现象是:_______ 。

(1)写出下列物质的化学式:A是
(2)写出反应“C→F”的离子方程式:
(3)在溶液I中滴入NaOH溶液,可观察到的现象是:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】已知:单质 为目前人类使用最广泛的金属,氧化物
为目前人类使用最广泛的金属,氧化物 为具有磁性的黑色晶体,根据下列转化关系填空。
为具有磁性的黑色晶体,根据下列转化关系填空。

(1)试判断: 的
的名称 为______________ ,写出 的化学反应方程式
的化学反应方程式______________ 。
(2)实验室检验 溶液中的阳离子时,可加入氢氧化钠溶液,若先产生
溶液中的阳离子时,可加入氢氧化钠溶液,若先产生__________ 色沉淀,该沉淀在空气中迅速变为灰绿色,最终变为________ 色,则含该离子。
(3)实验室检验 溶液中的阳离子时,通常可滴加
溶液中的阳离子时,通常可滴加________ (填写化学式),若溶液变为红色,则含该离子。
(4)写出固体 与过量盐酸反应的
与过量盐酸反应的离子方程式 ________________ 。
(5)写出 的
的离子方程式 __________________________________ 。
 为目前人类使用最广泛的金属,氧化物
为目前人类使用最广泛的金属,氧化物 为具有磁性的黑色晶体,根据下列转化关系填空。
为具有磁性的黑色晶体,根据下列转化关系填空。 
(1)试判断:
 的
的 的化学反应方程式
的化学反应方程式(2)实验室检验
 溶液中的阳离子时,可加入氢氧化钠溶液,若先产生
溶液中的阳离子时,可加入氢氧化钠溶液,若先产生(3)实验室检验
 溶液中的阳离子时,通常可滴加
溶液中的阳离子时,通常可滴加(4)写出固体
 与过量盐酸反应的
与过量盐酸反应的(5)写出
 的
的
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】已知A为常见的金属单质,根据如图所示的关系:

(1)确定A、B、E、F的化学式:A___________ ,B___________ ,E___________ ,F___________ 。
(2)写出⑧的化学方程式___________ ,④、⑤的离子方程式___________ ,___________ 。

(1)确定A、B、E、F的化学式:A
(2)写出⑧的化学方程式
您最近一年使用:0次





