按要求回答问题:
(1)以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池中:
①H+向___________ 极移动(填“正”或“负”)。
②电子流动方向由____________ 极流向____________ 极(填:“正”、“负”)。
③若有1mol e- 流过导线,则理论上负极质量减少____________ g。
④若将稀硫酸换成硫酸铜溶液,电极质量增加的是___________ (填“锌极”或“铜极”),原因是_____________ (用电极方程式表示)。
(2)一定温度下,在容积为2 L的密闭容器中进行反应:aN(g) bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:

①反应化学方程式中各物质的系数比为a∶b∶c=_________ 。
②1 min到3 min这段时刻,以M的浓度变化表示的平均反应速率为:__________ 。
③下列叙述中能说明上述反应达到平衡状态的是____________________________ 。
A.反应中当M与N的物质的量相等时
B.P的质量不随时间变化而变化
C.混合气体的总物质的量不随时间变化而变化
D.单位时间内每消耗a mol N,同时消耗b mol M
E.混合气体的压强不随时间的变化而变化
F.M的物质的量浓度保持不变
(1)以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池中:
①H+向
②电子流动方向由
③若有1mol e- 流过导线,则理论上负极质量减少
④若将稀硫酸换成硫酸铜溶液,电极质量增加的是
(2)一定温度下,在容积为2 L的密闭容器中进行反应:aN(g)
 bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
①反应化学方程式中各物质的系数比为a∶b∶c=
②1 min到3 min这段时刻,以M的浓度变化表示的平均反应速率为:
③下列叙述中能说明上述反应达到平衡状态的是
A.反应中当M与N的物质的量相等时
B.P的质量不随时间变化而变化
C.混合气体的总物质的量不随时间变化而变化
D.单位时间内每消耗a mol N,同时消耗b mol M
E.混合气体的压强不随时间的变化而变化
F.M的物质的量浓度保持不变
17-18高一下·天津·期末 查看更多[5]
(已下线)【南昌新东方】2019 八一中学、洪都中学、麻丘高中等七校 高一下 期末河北省张家口市第一中学西校区、万全中学2019-2020学年高二第一学期期初考试化学试题新疆兵团第二师华山中学2018-2019学年高一下学期期中考试化学试题(已下线)2019年4月14日《每日一题》 必修2 每周一测天津市部分区2017~2018学年高一下学期期末考试化学试题
更新时间:2018-09-22 16:02:53
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】研究和深度开发CO、CO2的应用具有重要的社会意义。回答下列问题:
I.CO可用于高炉炼铁,已知:
Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g) △H1=akJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H2=bkJ/mol
则反应Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)的△H=__ kJ/mol。
Ⅱ.某温度下,在容积为2L的密闭容器中投入8molCO2(g)、16molH2(g)发生反应:CO2(g)+H2(g) CO(g)+H2O(g),15min后达到平衡,此时CO2的转化率为75%。则
CO(g)+H2O(g),15min后达到平衡,此时CO2的转化率为75%。则
①0~15min内用二氧化碳表示平均反应速率v(CO2)=__ ,
②计算此条件下该反应的平衡常数K=__ 。
Ⅲ.捕碳技术是指从空气中捕获二氧化碳的各种科学技术的统称。目前NH3和(NH4)2CO3等物质已经被用作工业捕碳剂。
(1)下列物质中能作为CO2捕获剂的是__ 。
A.Na2CO3 B.NaOH C.CH3CH2OH D.NH4Cl
(2)用(NH4)2CO3捕碳的反应:(NH4)2CO3(aq)+H2O(1)+CO2(g) 2NH4HCO3(aq)。为研究温度对(NH4)2CO3捕获CO2效率的影响,将一定量的(NH4)2CO3溶液置于密闭容器中,并充人一定量的CO2气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到趋势图:
2NH4HCO3(aq)。为研究温度对(NH4)2CO3捕获CO2效率的影响,将一定量的(NH4)2CO3溶液置于密闭容器中,并充人一定量的CO2气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到趋势图:
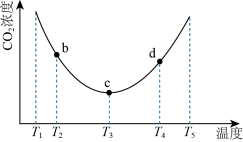
b、c、d三点的平衡常数Kb、Kc、Kd从大到小的顺序为__ 。
I.CO可用于高炉炼铁,已知:
Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g) △H1=akJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H2=bkJ/mol
则反应Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)的△H=
Ⅱ.某温度下,在容积为2L的密闭容器中投入8molCO2(g)、16molH2(g)发生反应:CO2(g)+H2(g)
 CO(g)+H2O(g),15min后达到平衡,此时CO2的转化率为75%。则
CO(g)+H2O(g),15min后达到平衡,此时CO2的转化率为75%。则①0~15min内用二氧化碳表示平均反应速率v(CO2)=
②计算此条件下该反应的平衡常数K=
Ⅲ.捕碳技术是指从空气中捕获二氧化碳的各种科学技术的统称。目前NH3和(NH4)2CO3等物质已经被用作工业捕碳剂。
(1)下列物质中能作为CO2捕获剂的是
A.Na2CO3 B.NaOH C.CH3CH2OH D.NH4Cl
(2)用(NH4)2CO3捕碳的反应:(NH4)2CO3(aq)+H2O(1)+CO2(g)
 2NH4HCO3(aq)。为研究温度对(NH4)2CO3捕获CO2效率的影响,将一定量的(NH4)2CO3溶液置于密闭容器中,并充人一定量的CO2气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到趋势图:
2NH4HCO3(aq)。为研究温度对(NH4)2CO3捕获CO2效率的影响,将一定量的(NH4)2CO3溶液置于密闭容器中,并充人一定量的CO2气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到趋势图:
b、c、d三点的平衡常数Kb、Kc、Kd从大到小的顺序为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】Ⅰ.温度为T时,某容积为 的密闭容器内,A、B两种气态物质的物质的量随时间变化的曲线如图所示,回答下列问题:
的密闭容器内,A、B两种气态物质的物质的量随时间变化的曲线如图所示,回答下列问题:
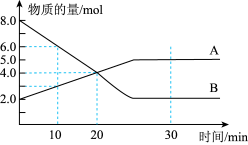
(1)该反应的化学方程式为___________ 。
(2) ,用B表示的平均反应速率
,用B表示的平均反应速率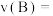
___________  。
。
(3)下列措施能增大反应速率的是___________(填字母)。
Ⅱ.纸电池是未来电池发展的重要研究方向。某学生在课外活动时,根据如图纸电池结构示意图,利用实验室中的稀硫酸、蒸馏水和滤纸制作电解液,用铜片与镁片作为电极材料。

(4)电池工作时 向
向___________ (填a或b)极作定向移动。
(5)某学生用硫酸铜溶液替代稀硫酸,正极发生的电极反应式为___________ 。
 的密闭容器内,A、B两种气态物质的物质的量随时间变化的曲线如图所示,回答下列问题:
的密闭容器内,A、B两种气态物质的物质的量随时间变化的曲线如图所示,回答下列问题:
(1)该反应的化学方程式为
(2)
 ,用B表示的平均反应速率
,用B表示的平均反应速率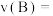
 。
。(3)下列措施能增大反应速率的是___________(填字母)。
| A.升高温度 | B.减小A的浓度 |
| C.缩小容器体积 | D.恒温恒容条件下充入氦气 |
Ⅱ.纸电池是未来电池发展的重要研究方向。某学生在课外活动时,根据如图纸电池结构示意图,利用实验室中的稀硫酸、蒸馏水和滤纸制作电解液,用铜片与镁片作为电极材料。

(4)电池工作时
 向
向(5)某学生用硫酸铜溶液替代稀硫酸,正极发生的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】某温度时,在2L恒容密闭容器中充入0.9molA(g)、0.6molB(g)、0.3molC(g),发生反应aA(g)+bB(g) cC(g),各物质间的转化关系如图所示,回答下列问题:
cC(g),各物质间的转化关系如图所示,回答下列问题:
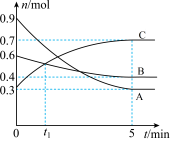
(1)该反应的化学方程式为______ 。
(2)0~5min内,v(B)=______ mol•L-1•min-1。
(3)反应达到平衡时,c(C)=_____ mol•L-1。
(4)若仅改变下列一个条件,推测该反应的速率发生的变化(填“增大”、“减小”或“不变”):
①降低温度,化学反应速率______ 。
②充入少量不参加反应的稀有气体,化学反应速率_____ 。
③将容器的体积压缩至原来的一半,化学反应速率_____ 。
(5)t1min时,反应______ (填“达到”或“没有达到”)化学平衡;5min时,v(正)______ (填“>”、“<”或“=”)v(逆)。
 cC(g),各物质间的转化关系如图所示,回答下列问题:
cC(g),各物质间的转化关系如图所示,回答下列问题:
(1)该反应的化学方程式为
(2)0~5min内,v(B)=
(3)反应达到平衡时,c(C)=
(4)若仅改变下列一个条件,推测该反应的速率发生的变化(填“增大”、“减小”或“不变”):
①降低温度,化学反应速率
②充入少量不参加反应的稀有气体,化学反应速率
③将容器的体积压缩至原来的一半,化学反应速率
(5)t1min时,反应
您最近一年使用:0次
【推荐1】将 和
和 置于预先抽成真空的特制2L恒容密闭容器中,加热至1500K,体系达到平衡,总压强为
置于预先抽成真空的特制2L恒容密闭容器中,加热至1500K,体系达到平衡,总压强为 体系中存在以下反应关系:
体系中存在以下反应关系:



回答下列问题:
(1) 与
与 、
、 、
、 的关系是
的关系是______ 。
(2)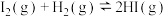 反应过程中碘单质的转化率随时间的变化曲线如图所示,A点时
反应过程中碘单质的转化率随时间的变化曲线如图所示,A点时
______  填“
填“ ”“
”“ ”或“
”或“ ”
” ,前
,前 的生成速率
的生成速率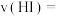
______ 。

(3)达到平衡状态时,氢气的物质的量分数是______ ;
______ ;
______  保留2位有效数字
保留2位有效数字 为用平衡分压代替浓度表示的平衡常数,平衡分压
为用平衡分压代替浓度表示的平衡常数,平衡分压 总压强
总压强 物质的量分数
物质的量分数 。
。
(4)下列说法能说明该体系达到平衡状态的是______ 。
A.颜色不再变化
B.气体平均相对分子质量不再变化
C.气体密度不再变化
D.温度不再变化
(5) 是一种强酸,常温下将
是一种强酸,常温下将 的HI溶液和
的HI溶液和 的氨水等体积混合后,溶液呈中性。此时溶液中离子浓度的大小关系是
的氨水等体积混合后,溶液呈中性。此时溶液中离子浓度的大小关系是______ 。
 和
和 置于预先抽成真空的特制2L恒容密闭容器中,加热至1500K,体系达到平衡,总压强为
置于预先抽成真空的特制2L恒容密闭容器中,加热至1500K,体系达到平衡,总压强为 体系中存在以下反应关系:
体系中存在以下反应关系:



回答下列问题:
(1)
 与
与 、
、 、
、 的关系是
的关系是(2)
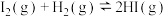 反应过程中碘单质的转化率随时间的变化曲线如图所示,A点时
反应过程中碘单质的转化率随时间的变化曲线如图所示,A点时
 填“
填“ ”“
”“ ”或“
”或“ ”
” ,前
,前 的生成速率
的生成速率

(3)达到平衡状态时,氢气的物质的量分数是


 保留2位有效数字
保留2位有效数字 为用平衡分压代替浓度表示的平衡常数,平衡分压
为用平衡分压代替浓度表示的平衡常数,平衡分压 总压强
总压强 物质的量分数
物质的量分数 。
。(4)下列说法能说明该体系达到平衡状态的是
A.颜色不再变化
B.气体平均相对分子质量不再变化
C.气体密度不再变化
D.温度不再变化
(5)
 是一种强酸,常温下将
是一种强酸,常温下将 的HI溶液和
的HI溶液和 的氨水等体积混合后,溶液呈中性。此时溶液中离子浓度的大小关系是
的氨水等体积混合后,溶液呈中性。此时溶液中离子浓度的大小关系是
您最近一年使用:0次
【推荐2】(1)氮及其化合物的转化很有意义。下面是氮的氧化物在几种不同情况下的转化:
①已知:2SO2(g)+O2(g) 2SO3(g) H= -196.6 kJmol-1
2SO3(g) H= -196.6 kJmol-1
2NO(g)+O2(g) 2NO2(g) H=-113.0kJmol-1
2NO2(g) H=-113.0kJmol-1
则SO2气体与NO2气体反应生成SO3气体和NO气体的热化学方程式为:______________ 。
②a.向绝热恒容密闭容器中通入SO2和NO2,一定条件下使其反应达到平衡,正反应速率随时间变化的示意图如图1所示。反应在c点________ (“达到”或“未到”)平衡状态。

b.开始时,分别在该容器中加入Ⅰ:2mol SO2(g)和2 mol NO2(g)
Ⅱ:2 mol SO3(g)和2 mol NO(g)。则反应达到平衡时,比较容器Ⅰ和容器Ⅱ中反应平衡常数:Ⅰ____ Ⅱ(填“>”“=”或“<”)。 .
(2)已知在温度为T时,CO(g)+H2O(g) CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1 molL-1,c始(H2O)=1 molL-1,某时刻经测定CO的转化率为10%,则该反应
CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1 molL-1,c始(H2O)=1 molL-1,某时刻经测定CO的转化率为10%,则该反应________ (填“已经”或“没有”)达到平衡,原因是________ 。此时刻v正________ v逆(填“>”或“<”)。 .
①已知:2SO2(g)+O2(g)
 2SO3(g) H= -196.6 kJmol-1
2SO3(g) H= -196.6 kJmol-12NO(g)+O2(g)
 2NO2(g) H=-113.0kJmol-1
2NO2(g) H=-113.0kJmol-1则SO2气体与NO2气体反应生成SO3气体和NO气体的热化学方程式为:
②a.向绝热恒容密闭容器中通入SO2和NO2,一定条件下使其反应达到平衡,正反应速率随时间变化的示意图如图1所示。反应在c点

b.开始时,分别在该容器中加入Ⅰ:2mol SO2(g)和2 mol NO2(g)
Ⅱ:2 mol SO3(g)和2 mol NO(g)。则反应达到平衡时,比较容器Ⅰ和容器Ⅱ中反应平衡常数:Ⅰ
(2)已知在温度为T时,CO(g)+H2O(g)
 CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1 molL-1,c始(H2O)=1 molL-1,某时刻经测定CO的转化率为10%,则该反应
CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1 molL-1,c始(H2O)=1 molL-1,某时刻经测定CO的转化率为10%,则该反应
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】CH3OH、CO、CH4等都是重要的能源,也是重要的化工原料。
(1)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
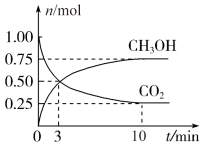
①从反应开始到平衡,CO2的平均反应速率v(CO2)=____ 。
②达到平衡时,H2的浓度为____ mol/L。
(2)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g) CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是____ 。
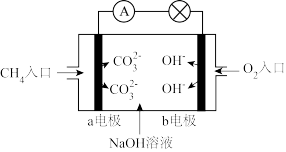
(3)某种甲烷燃料电池的工作原理如图所示氧气通入的一极为电源的____ 极,a电极反应式:____ ,b电极反应式:____ 。
(4)当电路中累计有2 mol电子通过时,消耗的甲烷体积为(在标准状况下)____ L。
(1)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
①从反应开始到平衡,CO2的平均反应速率v(CO2)=
②达到平衡时,H2的浓度为
(2)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g)
 CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是| A.反应中CO与CH3OH的物质的量之比为1:1 |
| B.混合气体的压强不随时间的变化而变化 |
| C.单位时间内每消耗1 mol CO,同时生成1 mol CH3OH |
| D.CH3OH的质量分数在混合气体中保持不变 |
(4)当电路中累计有2 mol电子通过时,消耗的甲烷体积为(在标准状况下)

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】海带中含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:

请回答下列问题:
(1)实验时灼烧海带通常应在__________ (填仪器名称)内进行。
(2)步骤④中反应的离子方程式是___________________________________ 。
(3)上述流程③、⑤中的实验操作分别包括下图中的__________ 、__________ (按操作顺序选填字母代号)。

(4)检验提取碘后的溶液中没有单质碘残留,所用试剂是___________ ,现象是_______________ 。
(5)锂锰电池的体积小,性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2,电池放电的总反应为Li+MnO2==LiMnO2。回答下列问题:

①外电路的电流方向是由_______ 极流向________ 极(填字母)。
②电池负极反应式为________________________ 。
③是否可用水代替电池中的混合有机溶剂?________ (填“是”或“否”),原因是__________________ 。

请回答下列问题:
(1)实验时灼烧海带通常应在
(2)步骤④中反应的离子方程式是
(3)上述流程③、⑤中的实验操作分别包括下图中的

(4)检验提取碘后的溶液中没有单质碘残留,所用试剂是
(5)锂锰电池的体积小,性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2,电池放电的总反应为Li+MnO2==LiMnO2。回答下列问题:

①外电路的电流方向是由
②电池负极反应式为
③是否可用水代替电池中的混合有机溶剂?
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】电池及其相关技术应用非常广泛。回答下列问题:
(1)废旧电池科学的处理方法是_____ (填标号)。
A.露天焚烧 B.深埋处理 C.集中处理、回收资源
(2)锌锰干电池、铅酸蓄电池、氢氧燃料电池等均是常见电池,下列说法正确的是_____ (填标号)。
A.常见的锌锰干电池是二次电池
B.氢氧燃料电池中H2、O2不是储存在电池内部的
C.燃料电池的能量利用率比直接燃烧的利用率高
(3)Li-CO2二次电池的装置如图所示:
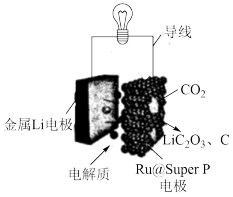
放电时,沿金属Li电极→导线→Ru@SuperP电极方向移动的是_____ (填“电子”“电流”或“Li+”),电池的总反应方程式为________ 。
(4)利用微生物燃料电池既可处理废水又可回收电能,其装置示意图如图:

A极为该电池_____ (填“正”或“负”)极,正极的电极反应式为_____ 。
(1)废旧电池科学的处理方法是
A.露天焚烧 B.深埋处理 C.集中处理、回收资源
(2)锌锰干电池、铅酸蓄电池、氢氧燃料电池等均是常见电池,下列说法正确的是
A.常见的锌锰干电池是二次电池
B.氢氧燃料电池中H2、O2不是储存在电池内部的
C.燃料电池的能量利用率比直接燃烧的利用率高
(3)Li-CO2二次电池的装置如图所示:

放电时,沿金属Li电极→导线→Ru@SuperP电极方向移动的是
(4)利用微生物燃料电池既可处理废水又可回收电能,其装置示意图如图:

A极为该电池
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】 等气体污染环境,电化学技术可以将
等气体污染环境,电化学技术可以将 “变废为宝”,是有效解决该问题的重要方法。
“变废为宝”,是有效解决该问题的重要方法。
(1)某兴趣小组以 为原料,采用电化学方法制取较高浓度的硫酸。装置示意图如下:
为原料,采用电化学方法制取较高浓度的硫酸。装置示意图如下:

①电子的流向:电极M___________ 电极N(填“ ”或“
”或“ ”);
”);
②M极上的电极反应式为___________ ;
③一段时间后,小组成员测得离子交换膜X右侧硫酸溶液的浓度不变,则离子交换膜X为___________ 交换膜(填“阳离子”或“阴离子”)。
(2)某工厂烟气中主要含有 ,可用NaOH溶液吸收烟气中的
,可用NaOH溶液吸收烟气中的 ,将所得的
,将所得的 溶液进行电解,在循环再生NaOH的同时,可得到
溶液进行电解,在循环再生NaOH的同时,可得到 ,其原理如图所示(电极材料为石墨):
,其原理如图所示(电极材料为石墨):

①图中所产生的物质A为___________ ;
②右室(阴离子交换膜右侧)中加入稀硫酸的主要目的是___________ ;
③当左室(阳离子交换膜左侧)增加的阴离子数目为2 时,有
时,有___________ mol 通过阴离子交换膜。
通过阴离子交换膜。
 等气体污染环境,电化学技术可以将
等气体污染环境,电化学技术可以将 “变废为宝”,是有效解决该问题的重要方法。
“变废为宝”,是有效解决该问题的重要方法。(1)某兴趣小组以
 为原料,采用电化学方法制取较高浓度的硫酸。装置示意图如下:
为原料,采用电化学方法制取较高浓度的硫酸。装置示意图如下:
①电子的流向:电极M
 ”或“
”或“ ”);
”);②M极上的电极反应式为
③一段时间后,小组成员测得离子交换膜X右侧硫酸溶液的浓度不变,则离子交换膜X为
(2)某工厂烟气中主要含有
 ,可用NaOH溶液吸收烟气中的
,可用NaOH溶液吸收烟气中的 ,将所得的
,将所得的 溶液进行电解,在循环再生NaOH的同时,可得到
溶液进行电解,在循环再生NaOH的同时,可得到 ,其原理如图所示(电极材料为石墨):
,其原理如图所示(电极材料为石墨):
①图中所产生的物质A为
②右室(阴离子交换膜右侧)中加入稀硫酸的主要目的是
③当左室(阳离子交换膜左侧)增加的阴离子数目为2
 时,有
时,有 通过阴离子交换膜。
通过阴离子交换膜。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】高铁酸钾(K2FeO4)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图是高铁电池的模拟实验装置:

(1)该电池放电时正极的电极反应式为_________ ;若维持电流强度为1A,电池工作十分钟,理论消耗Zn________ g(已知F=96500C·mol-1)。
(2)盐桥中盛有饱和KCl溶液,此盐桥中氯离子向______ (填“左”或“右”)移动;若用阳离子交换膜代替盐桥,则钾离子向________ (填“左”或“右”)移动。
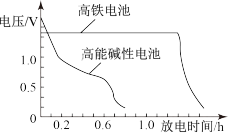
(3)下图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有__________ 。

(1)该电池放电时正极的电极反应式为
(2)盐桥中盛有饱和KCl溶液,此盐桥中氯离子向
(3)下图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】二氧化碳的捕集和资源化利用是缓解温室效应的重要战略方向。
(1)我国在二氧化碳催化加氢合成甲醇上取得了突破性进展,有关反应如下:
反应ⅰ:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.6kJ·mol-1
CH3OH(g)+H2O(g) △H=-49.6kJ·mol-1
反应ⅱ:CO2(g)+H2(g) CO(g)+H2O(g) △H=+41kJ·mol-1
CO(g)+H2O(g) △H=+41kJ·mol-1
根据反应ⅰ和反应ⅱ,推出CO(g)和H2(g)合成甲醇的热化学方程式为_______ 。
(2)在催化剂M的作用下,CO2(g)+H2(g) CO(g)+H2O(g)的微观反应历程和相对能量(E)如图所示,其中吸附在催化剂表面上的物种用“*”标注。已知:
CO(g)+H2O(g)的微观反应历程和相对能量(E)如图所示,其中吸附在催化剂表面上的物种用“*”标注。已知: 表示C,
表示C, 表示O,
表示O, 表示H。
表示H。
历程Ⅰ: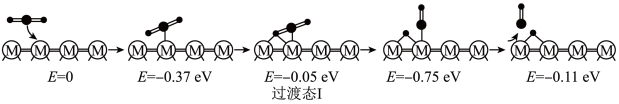
反应甲:CO2(g)=CO(g)+O*
历程Ⅱ: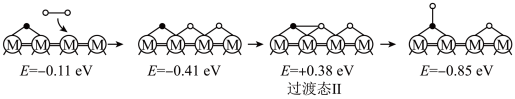
反应乙:H2(g)+O*=HO*+H*
历程Ⅲ: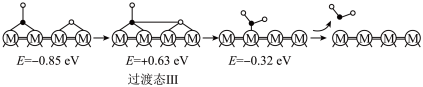
反应丙:_______
①历程Ⅲ中的反应丙可表示为_______ 。
②决定CO2(g)+H2(g) CO(g)+H2O(g)的总反应速率的是历程
CO(g)+H2O(g)的总反应速率的是历程_______ (填“Ⅰ”、“Ⅱ”或“Ⅲ”)。
(3)将CO2和H2按物质的量之比1:3充入一恒容密闭容器中,同时发生了反应ⅰ和反应ⅱ,测得CO2的平衡转化率随温度、压强变化的情况如图所示。
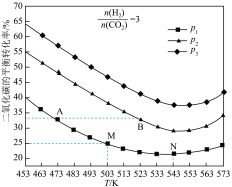
①压强p1、p2、p3 的大小关系为_______ 。
②A点、B点的化学反应速率大小:v(A)_______ v(B) (填“<”、“=”或“>”)。
③温度高于543K时,CO2的平衡转化率随温度的升高而增大的原因是_______ 。
④图中M点对应的温度下,已知CO的选择性(生成的CO与转化的CO2的百分比)为50%,该温度下反应ii的平衡常数为_______ (结果保留3位小数)。
如图是某科研团队设计的光电催化反应器,可由CO2制得异丙醇,其中A、B均是惰性电极。
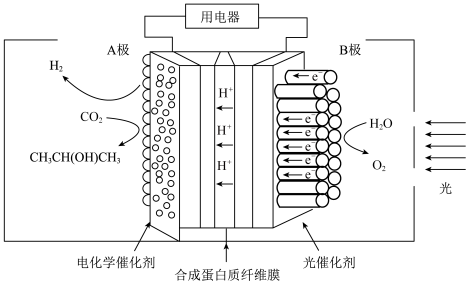
(4)B电极为该电化学装置的_______ 极。
(5)A极上CO2参与的电极反应式为_______ 。
(1)我国在二氧化碳催化加氢合成甲醇上取得了突破性进展,有关反应如下:
反应ⅰ:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H=-49.6kJ·mol-1
CH3OH(g)+H2O(g) △H=-49.6kJ·mol-1反应ⅱ:CO2(g)+H2(g)
 CO(g)+H2O(g) △H=+41kJ·mol-1
CO(g)+H2O(g) △H=+41kJ·mol-1根据反应ⅰ和反应ⅱ,推出CO(g)和H2(g)合成甲醇的热化学方程式为
(2)在催化剂M的作用下,CO2(g)+H2(g)
 CO(g)+H2O(g)的微观反应历程和相对能量(E)如图所示,其中吸附在催化剂表面上的物种用“*”标注。已知:
CO(g)+H2O(g)的微观反应历程和相对能量(E)如图所示,其中吸附在催化剂表面上的物种用“*”标注。已知: 表示C,
表示C, 表示O,
表示O, 表示H。
表示H。历程Ⅰ:

反应甲:CO2(g)=CO(g)+O*
历程Ⅱ:

反应乙:H2(g)+O*=HO*+H*
历程Ⅲ:

反应丙:_______
①历程Ⅲ中的反应丙可表示为
②决定CO2(g)+H2(g)
 CO(g)+H2O(g)的总反应速率的是历程
CO(g)+H2O(g)的总反应速率的是历程(3)将CO2和H2按物质的量之比1:3充入一恒容密闭容器中,同时发生了反应ⅰ和反应ⅱ,测得CO2的平衡转化率随温度、压强变化的情况如图所示。

①压强p1、p2、p3 的大小关系为
②A点、B点的化学反应速率大小:v(A)
③温度高于543K时,CO2的平衡转化率随温度的升高而增大的原因是
④图中M点对应的温度下,已知CO的选择性(生成的CO与转化的CO2的百分比)为50%,该温度下反应ii的平衡常数为
如图是某科研团队设计的光电催化反应器,可由CO2制得异丙醇,其中A、B均是惰性电极。

(4)B电极为该电化学装置的
(5)A极上CO2参与的电极反应式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某学习小组探究某浓度浓硝酸和稀硝酸与铁的反应。
(1)Ⅰ中液面上方气体由无色变为红棕色的化学方程式为_______ 。
(2)取少量Ⅰ中溶液,加入KSCN溶液,_______ (填现象),说明产生了Fe3+。
(3)Ⅱ中现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应。说明硝酸具有_______ 性。
(4)Ⅲ中,连接导线后体系形成了原电池。为分析反应过程,在Fe、Cu之间连接电流计,实验如下。
①用方程式解释现象ⅳ:_______ 。
②推测现象ⅰ中被还原的是_______ 。
③解释现象ii中指针左右偏转,往复多次的原因_______ 。
④现象ⅲ中,Fe一直做负极,难以形成氧化层,可能的原因是_______ 。
| 实验 | 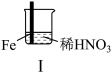 | 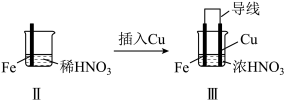 | |
| 现象 | Ⅰ中:Fe表面产生大量无色气泡,液面上方变为红棕色 | Ⅱ中:Fe表面产生红棕色气泡,过一会儿停止 | Ⅲ中:连接导线,一段时间后Fe表面产生红棕色气泡,而后停止;随即又产生红棕色气泡,而后停止,……如此往复多次。Cu表面始终产生红棕色气泡 |
(2)取少量Ⅰ中溶液,加入KSCN溶液,
(3)Ⅱ中现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应。说明硝酸具有
(4)Ⅲ中,连接导线后体系形成了原电池。为分析反应过程,在Fe、Cu之间连接电流计,实验如下。
| 实验 | 现象 |
 | ⅰ.K闭合时,指针向左偏转(Cu做负极),Fe表面无明显现象 ⅱ.过一会儿指针向右偏,Fe表面产生红棕色气体;后又迅速向左偏,Fe表面停止产生气泡,……如此往复多次 ⅲ.一段时间后,指针一直处于右端,Fe表面持续产生红棕色气体 ⅳ.Cu表面始终产生红棕色气泡 |
②推测现象ⅰ中被还原的是
③解释现象ii中指针左右偏转,往复多次的原因
④现象ⅲ中,Fe一直做负极,难以形成氧化层,可能的原因是
您最近一年使用:0次



