氯化硫(S2Cl2)是一种黄红色液体,有刺激性、窒息性恶臭,熔点为-80℃,沸点137.1℃。在空气中强烈发烟,易与水发生水解反应。人们使用它作橡胶硫化剂,使橡胶硫化,改变生橡胶热发粘冷变硬的不良性能。在熔融的硫中通入氯气即可生成S2Cl2。下图是实验室用S和Cl2制备S2Cl2的装置(夹持装置、加热装置均已略去)。

(1)仪器d的名称___________
(2)已知S2Cl2分子结构与H2O2相似,请写出S2Cl2的结构式__________________ 。
(3)装置a中的溶液为_________ ;f装置的作用为__________________________________________ 。
(4)该实验的操作顺序应为_______________________________ (用序号表示)。
①加热装置c ②通入Cl2 ③通冷凝水 ④停止通Cl2 ⑤停止加热装置c
(5)已知S2Cl2水解时,只有一种元素的化合价发生了变化,且被氧化和被还原的该元素的物质的量之比为1:3,请写出该反应的化学方程式____________________________________________ 。

(1)仪器d的名称
(2)已知S2Cl2分子结构与H2O2相似,请写出S2Cl2的结构式
(3)装置a中的溶液为
(4)该实验的操作顺序应为
①加热装置c ②通入Cl2 ③通冷凝水 ④停止通Cl2 ⑤停止加热装置c
(5)已知S2Cl2水解时,只有一种元素的化合价发生了变化,且被氧化和被还原的该元素的物质的量之比为1:3,请写出该反应的化学方程式
更新时间:2018-10-11 15:07:21
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】在我国南方,遭遇冰雪灾害时常使用一种融雪剂,其主要成分的化学式为XY2,X、Y均为元素周期表前20号元素,X的阳离子和Y的阴离子电子层结构相同,且1 mol XY2含有54 mol电子。
(1)该融雪剂的化学式是__________________ ,该物质中化学键类型是________________ ,电子式是__________________
(2)D、E元素原子的最外层电子数是其电子层数的2倍,D与Y相邻,则元素D的阴离子结构示意图是________________ 。D与E能形成一种结构类似于CO2的三原子分子,且每个原子均达到了8电子稳定结构,该分子的电子式为____________________ 。
(3)W是与D同主族的短周期元素,Z是第三周期金属性最强的元素,Z的单质与W的单质加热时生成物中化学键类型为__________ ,电子式为__________ 。
(1)该融雪剂的化学式是
(2)D、E元素原子的最外层电子数是其电子层数的2倍,D与Y相邻,则元素D的阴离子结构示意图是
(3)W是与D同主族的短周期元素,Z是第三周期金属性最强的元素,Z的单质与W的单质加热时生成物中化学键类型为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知A、B、C、D、E是短周期中的五种非金属元素,它们的原子序数依次增大。A元素原子形成的离子核外电子数为零,C、D在元素周期表中处于相邻的位置,B原子的最外层电子数是内层电子数的2倍。E元素与D元素同主族;E的单质为黄色固体,易溶于二硫化碳。
(1)请写出元素符号:B___________ D___________ 。
(2)画出E的阴离子的结构示意图______________________ 。
(3)用电子式表示钠与D形成原子个数为2:1的化合物的形成过程:___________________ 。
(1)请写出元素符号:B
(2)画出E的阴离子的结构示意图
(3)用电子式表示钠与D形成原子个数为2:1的化合物的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】如图为元素周期表的一部分,已知D为金属元素且其原子核外内层电子数为最外层电子数的5倍
请回答下列问题:
(1)元素B在元素周期表中的位置为________
(2)元素A和元素E的最简单氢化物中沸点较高的是_____ (填化学式)
(3)已知BC2中所有原子的最外层均满足8电子稳定结构,则BC2的电子式为_____ 其中B元素的化合价为______ 价。
(4)D3A2与H2O反应可生成两种碱,请写出该反应的化学方程式____________
(5)Y与X的原子序数之差为____________ .
| A | B | C | ||||
| D | E | X | ||||
| G | ||||||
| Y |
(1)元素B在元素周期表中的位置为
(2)元素A和元素E的最简单氢化物中沸点较高的是
(3)已知BC2中所有原子的最外层均满足8电子稳定结构,则BC2的电子式为
(4)D3A2与H2O反应可生成两种碱,请写出该反应的化学方程式
(5)Y与X的原子序数之差为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】NaClO2是一种重要的杀菌消毒剂,其一种生产工艺如图:

(1)NaClO2中Cl的化合价为_______ 。
(2)写出“反应”步骤中生成ClO2的化学方程式_______ 。
(3)“尾气吸收”是吸收“电解”过程排出的少量ClO2,发生如下反应:2NaOH+H2O2+2ClO2=2NaClO2+O2+2H2O
①用单线桥表示电子转移方向和数目_______ 。
②此吸收反应中,氧化产物是_______ ,氧化剂与还原剂的物质的量之比为_______ 。
③比较氧化性:ClO2_______ O2(填“>”、“<”或“=”)。

(1)NaClO2中Cl的化合价为
(2)写出“反应”步骤中生成ClO2的化学方程式
(3)“尾气吸收”是吸收“电解”过程排出的少量ClO2,发生如下反应:2NaOH+H2O2+2ClO2=2NaClO2+O2+2H2O
①用单线桥表示电子转移方向和数目
②此吸收反应中,氧化产物是
③比较氧化性:ClO2
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备KClO3和NaClO,并探究其氧化还原性质。
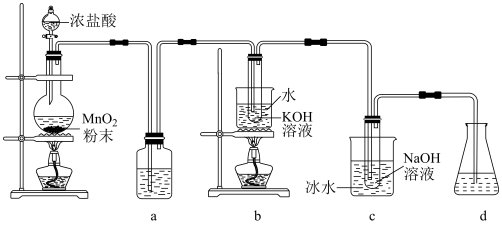
回答下列问题:
(1)盛放MnO2粉末的仪器名称是___________ ,a中的试剂为___________ 。
(2)b中反应的化学方程式为___________ 。
(3)c中反应的离子方程式是___________ ,采用冰水浴冷却的目的是___________ 。
(4)d中可选用试剂___________(填标号)。
(5)反应结束后,取出b中试管,经冷却结晶,___________ ,___________ ,干燥,得到较为纯净的KClO3晶体。取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显___________ 色。可知该条件下KClO3的氧化能力___________ NaClO(填“大于”或“小于”)。

回答下列问题:
(1)盛放MnO2粉末的仪器名称是
(2)b中反应的化学方程式为
(3)c中反应的离子方程式是
(4)d中可选用试剂___________(填标号)。
| A.Na2S溶液 | B.NaCl溶液 | C.NaOH溶液 | D.H2SO4溶液 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】二氧化钒( )是一种具有相变性质的材料,用于智能控温薄膜领域。用钒精矿(主要成分
)是一种具有相变性质的材料,用于智能控温薄膜领域。用钒精矿(主要成分 ,含少量钙)制取二氧化钒的工艺流程如图所示。
,含少量钙)制取二氧化钒的工艺流程如图所示。

已知:“焙烧”时,生成偏钒酸钠( ,易溶于水)、偏钒酸钙[
,易溶于水)、偏钒酸钙[ ,不溶于水]和氧化铁;第1次沉钒生成
,不溶于水]和氧化铁;第1次沉钒生成 。
。
回答下列问题:
(1)“焙烧”时, 转化为偏钒酸钠、氧化铁,该反应中参加反应的物质还有
转化为偏钒酸钠、氧化铁,该反应中参加反应的物质还有_______ 。
(2)“溶浸、除杂”时,滤渣1的主要成分是_______ (填化学式),加入碳酸钠的作用是_______ 。
(3)“还原”时,微沸数分钟得到 溶液,同时生成一种无色无污染的气体,该反应的化学方程式为
溶液,同时生成一种无色无污染的气体,该反应的化学方程式为_______ 。
(4)滤渣3为氧钒碱式碳酸铵晶体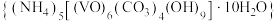 ,该晶体中钒元素的化合价为
,该晶体中钒元素的化合价为_______ ,在“加热”时,通入氮气的目的是_______ 。
 )是一种具有相变性质的材料,用于智能控温薄膜领域。用钒精矿(主要成分
)是一种具有相变性质的材料,用于智能控温薄膜领域。用钒精矿(主要成分 ,含少量钙)制取二氧化钒的工艺流程如图所示。
,含少量钙)制取二氧化钒的工艺流程如图所示。
已知:“焙烧”时,生成偏钒酸钠(
 ,易溶于水)、偏钒酸钙[
,易溶于水)、偏钒酸钙[ ,不溶于水]和氧化铁;第1次沉钒生成
,不溶于水]和氧化铁;第1次沉钒生成 。
。回答下列问题:
(1)“焙烧”时,
 转化为偏钒酸钠、氧化铁,该反应中参加反应的物质还有
转化为偏钒酸钠、氧化铁,该反应中参加反应的物质还有(2)“溶浸、除杂”时,滤渣1的主要成分是
(3)“还原”时,微沸数分钟得到
 溶液,同时生成一种无色无污染的气体,该反应的化学方程式为
溶液,同时生成一种无色无污染的气体,该反应的化学方程式为(4)滤渣3为氧钒碱式碳酸铵晶体
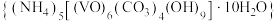 ,该晶体中钒元素的化合价为
,该晶体中钒元素的化合价为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】有A、B、C、D、E、F6种短周期元素,其元素特征信息如表,回答下列问题:
(1)C元素在周期表中位置___________ 。
(2)写出D、E、F元素符号:D___________ 、E___________ 、F___________ 。
(3)写出A、B、C形成的化合物的电子式___________ ;该化合物含有的化学键类型有___________ 、___________ 。
(4)写出三种含B元素的10e-微粒___________ 、___________ 、___________ 。
(5)F的非金属性强于E,下列表述中能证明这一事实的是___________ (填字母)。
A.F的氢化物比E的氢化物稳定
B.F的单质能将E从其钠盐溶液中置换出来
| 编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物 |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,最高正化合价与最低负化合价的代数和为4 |
| F | 其最简单气态氢化物能和其最高价氧化物反应生成一种离子化合物 |
(1)C元素在周期表中位置
(2)写出D、E、F元素符号:D
(3)写出A、B、C形成的化合物的电子式
(4)写出三种含B元素的10e-微粒
(5)F的非金属性强于E,下列表述中能证明这一事实的是
A.F的氢化物比E的氢化物稳定
B.F的单质能将E从其钠盐溶液中置换出来
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】现有部分短周期元素的性质或原子结构如表:
(1)元素X在元素周期表中的位置为____ ,X的一种同位元素可测定文物年代,这种同位素的符号是______ (用元素符号表示)。
(2)元素Z的离子结构示意图为________ ,元素Y与氢元素形成离子YH 的电子式为
的电子式为________ 。
(3)元素X 、Y 、Z的原子半径从大到小的顺序为________ (用元素符号表示)。
(4)元素X与元素Y相比,非金属性较强的是________ (用元素符号表示)。下列表述中能证明这一事实的是________ 。
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物对应水化物的酸性比X的最高价氧化物对应水化物的酸性强
c.X与Y形成的化合物中X元素呈正价状态
(5)Y的最高价氧化物的水化物与气态氢化物合成的化合物含的化学键类型是_________ 。
(6) )写出Z元素最高价氧化物对应的水化物与NaOH溶液反应的离子方程式:________ 。
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 第三周期元素的简单离子中半径最小 |
(2)元素Z的离子结构示意图为
 的电子式为
的电子式为(3)元素X 、Y 、Z的原子半径从大到小的顺序为
(4)元素X与元素Y相比,非金属性较强的是
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物对应水化物的酸性比X的最高价氧化物对应水化物的酸性强
c.X与Y形成的化合物中X元素呈正价状态
(5)Y的最高价氧化物的水化物与气态氢化物合成的化合物含的化学键类型是
(6) )写出Z元素最高价氧化物对应的水化物与NaOH溶液反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A、B、C、D、E、F、G七种前四周期元素且原子序数依次增大,A的最高正价和最低负价的绝对值相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子s能级的电子总数与p能级的电子数相等,F的基态原子的3d轨道电子数是4s电子数的5倍,G的3d轨道有3个未成对电子,请回答下列问题:
(1)F的基态原子电子排布式为_______________ ,G在周期表的位置________________ 。
(2)B、C、D的原子的第一电离能由小到大的顺序为____ (用元素符号回答),A、C、D形成的离子化合物中的化学键类型____________________ 。
(3)下列关于B2A2(B原子最外层满足8电子稳定结构)分子和A2D2分子的说法正确的是___ 。
a.分子中都含有σ键和π键 b.B2A2分子的沸点明显低于A2D2分子
c.都是含极性键和非极性键的非极性分子 d.互为等电子体,分子的空间构型都为直线形
e.中心原子都是sp杂化
(4)用电子式表示E的氯化物的形成过程_____________________________ 。
(5)F的最高正价为+6价,而氧原子最多只能形成2个共价键,试推测CrO5的结构式________ 。
(6)C的最低价的氢化物为CH3,通常情况下,G2+的溶液很稳定,它与CH3形成的配位数为6的配离子却不稳定,在空气中易被氧化为[G(CH3)6]3+,该反应的离子方程式是___________________ ,1 mol [G(CH3)6]3+配离子含有σ键数目为__________ 。
(1)F的基态原子电子排布式为
(2)B、C、D的原子的第一电离能由小到大的顺序为
(3)下列关于B2A2(B原子最外层满足8电子稳定结构)分子和A2D2分子的说法正确的是
a.分子中都含有σ键和π键 b.B2A2分子的沸点明显低于A2D2分子
c.都是含极性键和非极性键的非极性分子 d.互为等电子体,分子的空间构型都为直线形
e.中心原子都是sp杂化
(4)用电子式表示E的氯化物的形成过程
(5)F的最高正价为+6价,而氧原子最多只能形成2个共价键,试推测CrO5的结构式
(6)C的最低价的氢化物为CH3,通常情况下,G2+的溶液很稳定,它与CH3形成的配位数为6的配离子却不稳定,在空气中易被氧化为[G(CH3)6]3+,该反应的离子方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由软锰矿浆(主要成分是MnO2)吸收含硫废渣产生的废气制备,工艺如下图所示。

已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其它金属离子。请回答下列问题:
(1)高温焙烧前需将矿石研成粉末,其目的是____________ 。
(2)“氧化”中添加适量的MnO2的作用是__________ ,写出“沉锰”的离子方程式_________ 。
(3)下列各组试剂中,能准确测定尾气中SO2含量的是______ 。(填编号)
a.NaOH溶液、酚酞试液b.稀H2SO4酸化的KMnO4溶液c.碘水、淀粉溶液d.氨水、酚酞试液
(4)滤渣的主要成分有_____________ 。
(5)若要从MnSO4溶液中得到高纯硫酸锰必须进行的实验操作顺序是________ (用字母填空)。
a.过滤洗涤b.蒸发浓缩c.冷却结晶d.干燥
(6)已知:Ksp[Al(OH)3]=1×10-33,Ksp[Fe(OH)3]=3×10-39。pH=7.1时Mn(OH)2开始沉淀。室温下,除去MnSO4溶液中的Fe3+、Al3+(使其浓度均小于1×10-6mol/L),需调节溶液pH范围为______________ 。

已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其它金属离子。请回答下列问题:
(1)高温焙烧前需将矿石研成粉末,其目的是
(2)“氧化”中添加适量的MnO2的作用是
(3)下列各组试剂中,能准确测定尾气中SO2含量的是
a.NaOH溶液、酚酞试液b.稀H2SO4酸化的KMnO4溶液c.碘水、淀粉溶液d.氨水、酚酞试液
(4)滤渣的主要成分有
(5)若要从MnSO4溶液中得到高纯硫酸锰必须进行的实验操作顺序是
a.过滤洗涤b.蒸发浓缩c.冷却结晶d.干燥
(6)已知:Ksp[Al(OH)3]=1×10-33,Ksp[Fe(OH)3]=3×10-39。pH=7.1时Mn(OH)2开始沉淀。室温下,除去MnSO4溶液中的Fe3+、Al3+(使其浓度均小于1×10-6mol/L),需调节溶液pH范围为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某兴趣小组模拟侯氏制碱法的实验流程如下:
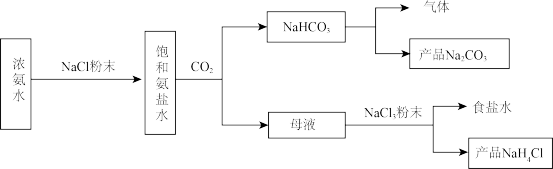
(1)二氧化碳通入饱和氨盐水的装置如图所示。
①图A装置制备二氧化碳气体,该装置主要玻璃仪器名称是_______ 。
②用图B装置对二氧化碳气体进行净化,在图中方框内补齐净化装置和净化试剂_______ 。

(2)母液中加入NaCl固体并通入 ,在
,在_______ (填温度范围)下析出 。
。
(3)验证产品纯碱中是否含有杂质NaCl的方法:取少量试样溶于水后,_______ 。
(4)由实验流程分析可知,可以循环利用的物质是_______ (用化学式表示)。
(5)称取制得的 (杂质NaCl)5.20g,配制成100mL溶液,取出20mL,用0.6000mol/L标准盐酸滴定(甲基橙做指示剂),消耗盐酸溶液体积为20.20mL。
(杂质NaCl)5.20g,配制成100mL溶液,取出20mL,用0.6000mol/L标准盐酸滴定(甲基橙做指示剂),消耗盐酸溶液体积为20.20mL。
①滴定终点颜色变化_______ 。
②制得的 纯度
纯度
_______ 。
③若滴定管用蒸馏水洗涤后,直接注入标准盐酸溶液进行滴定,则测定的 含量
含量_______ (填“偏高”、“偏低”或“无影响”)。
(6)图为实验测得0.1 mol/L 溶液在升温过程中(不考虑水挥发)的pH变化曲线,分析:
溶液在升温过程中(不考虑水挥发)的pH变化曲线,分析:
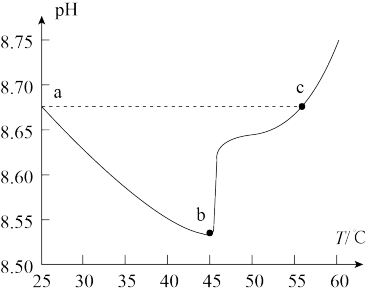
①a、c两点的溶液中由水电离出来的 a
a_______ c(填“>”、“<”或“=”)。
②bc段,随着温度升高pH增大,其原因是:_______ 。

(1)二氧化碳通入饱和氨盐水的装置如图所示。
①图A装置制备二氧化碳气体,该装置主要玻璃仪器名称是
②用图B装置对二氧化碳气体进行净化,在图中方框内补齐净化装置和净化试剂

(2)母液中加入NaCl固体并通入
 ,在
,在 。
。| 温度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
| NaCl溶解度(g/100g水) | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
 溶解度(g/100g水) 溶解度(g/100g水) | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 |
(4)由实验流程分析可知,可以循环利用的物质是
(5)称取制得的
 (杂质NaCl)5.20g,配制成100mL溶液,取出20mL,用0.6000mol/L标准盐酸滴定(甲基橙做指示剂),消耗盐酸溶液体积为20.20mL。
(杂质NaCl)5.20g,配制成100mL溶液,取出20mL,用0.6000mol/L标准盐酸滴定(甲基橙做指示剂),消耗盐酸溶液体积为20.20mL。①滴定终点颜色变化
②制得的
 纯度
纯度
③若滴定管用蒸馏水洗涤后,直接注入标准盐酸溶液进行滴定,则测定的
 含量
含量(6)图为实验测得0.1 mol/L
 溶液在升温过程中(不考虑水挥发)的pH变化曲线,分析:
溶液在升温过程中(不考虑水挥发)的pH变化曲线,分析:
①a、c两点的溶液中由水电离出来的
 a
a②bc段,随着温度升高pH增大,其原因是:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】为了制取氧气和二氧化碳,实验室提供了以下药品和仪器装置。
【药品】①二氧化锰 ②氯酸钾 ③大理石 ④过氧化氢溶液 ⑤稀盐酸
【装置】
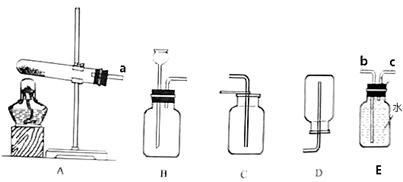
(1)小明同学选择的药品是③和⑤,则发生反应的化学方程式为__________________________________________________________________________________ ,他应该选择的发生装置是__________ (填序号),收集装置是____________ (填序号)。
(2)小东用装置A制取氧气,试管中装入的药品是______________ (填序号),他选择了E作收集装置,如果a与b相连,c端排出的物质主要是__________________________________ ;如果a与c相连,b端排出物质是_________________________________________ 。
【药品】①二氧化锰 ②氯酸钾 ③大理石 ④过氧化氢溶液 ⑤稀盐酸
【装置】

(1)小明同学选择的药品是③和⑤,则发生反应的化学方程式为
(2)小东用装置A制取氧气,试管中装入的药品是
您最近一年使用:0次



