实验表明,液体时纯硫酸的电离能力强于纯硝酸,纯硫酸的导电性强于纯水;又知液态电解质都能像水一样自身电离,而建立电离平衡(即像2H2O H3O++OH-),且在一定温度下都有各自的离子积常数.
H3O++OH-),且在一定温度下都有各自的离子积常数.
据此回答下列问题:
(1)纯硫酸在液态时,自身电离的电离反应方程式是____________________ ,它在25℃时的离子积常数K(H2SO4)比水的离子积常数K(H2O)[K(H2O)=c(H+)·c(OH-)]________ (填“大”“小”或“相等”).
(2)在纯硫酸与纯硝酸的液态混合物中,存在的阴离子主要是________ ;这是因为混合液中不但存在两种电离平衡(即H2SO4和HNO3各自的电离平衡,且硫酸的酸性强于硝酸),又在无水的条件下,混合酸中必发生____________________ (写离子反应方程式)反应而造成的.
 H3O++OH-),且在一定温度下都有各自的离子积常数.
H3O++OH-),且在一定温度下都有各自的离子积常数.据此回答下列问题:
(1)纯硫酸在液态时,自身电离的电离反应方程式是
(2)在纯硫酸与纯硝酸的液态混合物中,存在的阴离子主要是
2018高二上·全国·专题练习 查看更多[1]
(已下线)2018年10月9日 《每日一题》人教选修4-影响水的电离平衡的因素
更新时间:2018-10-16 19:42:00
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】室温下,将1.00mol/L盐酸滴入20.00mL 1.00mol/L氨水中,溶液pH和温度(℃)随加入盐酸体积变化曲线如右图所示。

(1)下列有关说法正确的是___________
A.a点由水电离出的C(H+)=10-14mol/L
B.b点:
C.c点:C(Cl-)=C(NH4+)
D.d点后,容易温度略下降的主要原因是NH3·H2O电离吸热
(2)在滴加过程中,水的电离程度的变化是先___ 后____ (填“增大”、“减小”或“不变”);
(3)在下表中,分别讨论了上述实验过程中离子浓度的大小顺序,对应溶质的化学式和
溶液的pH。试填写表中空白:

(1)下列有关说法正确的是
A.a点由水电离出的C(H+)=10-14mol/L
B.b点:

C.c点:C(Cl-)=C(NH4+)
D.d点后,容易温度略下降的主要原因是NH3·H2O电离吸热
(2)在滴加过程中,水的电离程度的变化是先
(3)在下表中,分别讨论了上述实验过程中离子浓度的大小顺序,对应溶质的化学式和
溶液的pH。试填写表中空白:
| 离子浓度的关系 | 溶质 | 溶液的pH | 物料守恒关系 | |
| ① | C(NH4+)>C(Cl-)>C(OH-)>C(H+) | pH>7 | / | |
| ② | NH4Cl | / | ||
| ③ | C(Cl-)>C(H+)>C(NH4+)>C(OH-) | pH<7 | / |
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】现有常温下浓度均为1 mol∙L−1的下列四种溶液:① 溶液、②
溶液、② 溶液、③
溶液、③ 溶液、④NaOH溶液、⑤
溶液、④NaOH溶液、⑤ 溶液。
溶液。
(1)这5种溶液pH由大到小的顺序是_______ ,其中由水电离的 浓度最小的是
浓度最小的是_______ 。 填序号
填序号
(2)②中各离子浓度由大到小的顺序是_______ , 的水解平衡常数Kh=
的水解平衡常数Kh=_____ 。(已知碳酸的电离常数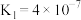 、
、 )
)
(3)向③中通入少量氨气,此时 的值
的值_____  填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变” 。
。
(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积_____ ④的体积(填“>” “<” 或“=”)。
(5)一定量的稀 溶液与足量的Zn反应,为减缓产生的H2速率但又不影响H2的总量,可采取的措施是
溶液与足量的Zn反应,为减缓产生的H2速率但又不影响H2的总量,可采取的措施是______ (填字母)。
A.加 固体 B.加
固体 B.加 固体 C.加
固体 C.加 溶液
溶液
D.加氨水 E.加 溶液
溶液
(6)常温下,向 溶液中加入
溶液中加入 溶液发生反应的离子方程式为
溶液发生反应的离子方程式为_______ ,若将所得悬浊液的pH调整为4,则溶液中 的溶液为
的溶液为______ mol∙L−1 (已知常温下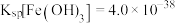 )。
)。
 溶液、②
溶液、② 溶液、③
溶液、③ 溶液、④NaOH溶液、⑤
溶液、④NaOH溶液、⑤ 溶液。
溶液。(1)这5种溶液pH由大到小的顺序是
 浓度最小的是
浓度最小的是 填序号
填序号
(2)②中各离子浓度由大到小的顺序是
 的水解平衡常数Kh=
的水解平衡常数Kh=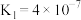 、
、 )
)(3)向③中通入少量氨气,此时
 的值
的值 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变” 。
。(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积
(5)一定量的稀
 溶液与足量的Zn反应,为减缓产生的H2速率但又不影响H2的总量,可采取的措施是
溶液与足量的Zn反应,为减缓产生的H2速率但又不影响H2的总量,可采取的措施是A.加
 固体 B.加
固体 B.加 固体 C.加
固体 C.加 溶液
溶液 D.加氨水 E.加
 溶液
溶液(6)常温下,向
 溶液中加入
溶液中加入 溶液发生反应的离子方程式为
溶液发生反应的离子方程式为 的溶液为
的溶液为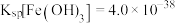 )。
)。
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】完成下列问题。
(1)某温度下,纯水中的c(OH-)=1×10-6 mol/L,则此时c(H+)为_____ mol/L。若在温度不变时,往其中滴加盐酸使 c(H+)=1×10-4mol/L,则溶液中c(OH-)为_____ mol/L。若将此盐酸稀释 1 000 倍,则溶液的c(H+)约为______ mol/L。
(2)已知:Cu(OH)2(s) Cu2+(aq)+2OH-(aq),Ksp=2×10-20。
Cu2+(aq)+2OH-(aq),Ksp=2×10-20。
①某CuSO4溶液里c(Cu2+)=0.02 mol·L-1,如果要使其生成 Cu(OH)2沉淀,应调整溶液的pH,使之大于_____ 。
②要使0.2 mol·L-1CuSO4溶液中的Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液的pH为_____ 。
(3)重金属离子会对河流和海洋造成严重污染。某化工厂废水(pH=2.0)中含有Ag+、Pb2+等重金属离子,其浓度约为0.01 mol/L,排放前拟用沉淀法除去这两种离子,查找有关数据如下:
①你认为往废水中加入_____ (填字母),沉淀效果最好。
A.NaOH B.Na2S C.KI D.Ca(OH)2
②如果用生石灰处理上述废水,使溶液的pH=8,处理后废水中c(Pb2+)=_____ 。
(1)某温度下,纯水中的c(OH-)=1×10-6 mol/L,则此时c(H+)为
(2)已知:Cu(OH)2(s)
 Cu2+(aq)+2OH-(aq),Ksp=2×10-20。
Cu2+(aq)+2OH-(aq),Ksp=2×10-20。①某CuSO4溶液里c(Cu2+)=0.02 mol·L-1,如果要使其生成 Cu(OH)2沉淀,应调整溶液的pH,使之大于
②要使0.2 mol·L-1CuSO4溶液中的Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液的pH为
(3)重金属离子会对河流和海洋造成严重污染。某化工厂废水(pH=2.0)中含有Ag+、Pb2+等重金属离子,其浓度约为0.01 mol/L,排放前拟用沉淀法除去这两种离子,查找有关数据如下:
| 难溶电解质 | AgI | AgOH | Ag2S |
| Ksp | 8.3×10-12 | 5.6×10-8 | 6.3×10-50 |
| 难溶电解质 | PbI2 | Pb(OH)2 | PbS |
| Ksp | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
A.NaOH B.Na2S C.KI D.Ca(OH)2
②如果用生石灰处理上述废水,使溶液的pH=8,处理后废水中c(Pb2+)=
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】Ⅰ.现有NH4Cl和氨水组成的混合溶液。请回答下列问题(填“>”、“<”或“=”):
(1)若溶液的pH=7,则该溶液中c(NH4+)________ c(Cl-)。
(2)若溶液中pH>7,则该溶液中c(NH4+)________ c(Cl-)。
Ⅱ.常温下有浓度均为0.1mol•L-1的三种溶液:①Na2CO3、②NaHCO3、③HCl
(1)溶液②中按物质的量浓度由大到小顺序排列该溶液中各离子浓度__________________ ;
(2)溶液②中,c(CO32-)+c(HCO3-)+c(H2CO3)=__________ mol•L-1;
(3)将10mL溶液③加水稀释至100mL,则此时溶液中由水电离出的c( H+)=_____ mol•L-1。
(1)若溶液的pH=7,则该溶液中c(NH4+)
(2)若溶液中pH>7,则该溶液中c(NH4+)
Ⅱ.常温下有浓度均为0.1mol•L-1的三种溶液:①Na2CO3、②NaHCO3、③HCl
(1)溶液②中按物质的量浓度由大到小顺序排列该溶液中各离子浓度
(2)溶液②中,c(CO32-)+c(HCO3-)+c(H2CO3)=
(3)将10mL溶液③加水稀释至100mL,则此时溶液中由水电离出的c( H+)=
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】醋酸、盐酸和碳酸钠是生活中常见的物质。
(1)碳酸钠水溶液显碱性的原因是(用离子方程式表示)_____________________ 。
(2)泡沫灭火剂中装有Al2(SO4)3溶液、NaHCO3溶液及起泡剂,写出使用时发生反应的离子方程式___________________________________________ 。
(3)25 ℃时,浓度均为0.1 mol·Lˉ1的盐酸和醋酸溶液,下列说法正确的是_______ 。
a.两溶液的pH相同
b.两溶液的导电能力相同
c.两溶液中由水电离出的c(OH-)相同
d.中和等物质的量的NaOH,消耗两溶液的体积相同
(4)25 ℃时, pH=4的醋酸溶液和氯化铵溶液,醋酸溶液中水电离出的c(H+)与氯化铵溶液中水电离出的c(H+)之比是________________ 。
(5)醋酸溶液中存在电离平衡:CH3COOH CH3COO-+H+,下列叙述不正确的是
CH3COO-+H+,下列叙述不正确的是___
a.CH3COOH溶液中离子浓度关系满足:c(H+)=c(OH-)+c(CH3COO-)
b.0.1 mol·Lˉ1 的CH3COOH 溶液加水稀释,溶液中c(OH-)减小
c.CH3COOH溶液中加入少量CH3COONa固体,平衡逆向移动
d.常温下,pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后溶液的pH>7
e.室温下pH=3的醋酸溶液加水稀释,溶液中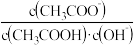 不变
不变
(6)浓度均为0.1mol/L的醋酸溶液和氢氧化钠溶液按体积比2:1混合,混合后溶液中离子浓度从大到小排序为______________________________________________________ 。
(1)碳酸钠水溶液显碱性的原因是(用离子方程式表示)
(2)泡沫灭火剂中装有Al2(SO4)3溶液、NaHCO3溶液及起泡剂,写出使用时发生反应的离子方程式
(3)25 ℃时,浓度均为0.1 mol·Lˉ1的盐酸和醋酸溶液,下列说法正确的是
a.两溶液的pH相同
b.两溶液的导电能力相同
c.两溶液中由水电离出的c(OH-)相同
d.中和等物质的量的NaOH,消耗两溶液的体积相同
(4)25 ℃时, pH=4的醋酸溶液和氯化铵溶液,醋酸溶液中水电离出的c(H+)与氯化铵溶液中水电离出的c(H+)之比是
(5)醋酸溶液中存在电离平衡:CH3COOH
 CH3COO-+H+,下列叙述不正确的是
CH3COO-+H+,下列叙述不正确的是a.CH3COOH溶液中离子浓度关系满足:c(H+)=c(OH-)+c(CH3COO-)
b.0.1 mol·Lˉ1 的CH3COOH 溶液加水稀释,溶液中c(OH-)减小
c.CH3COOH溶液中加入少量CH3COONa固体,平衡逆向移动
d.常温下,pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后溶液的pH>7
e.室温下pH=3的醋酸溶液加水稀释,溶液中
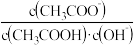 不变
不变(6)浓度均为0.1mol/L的醋酸溶液和氢氧化钠溶液按体积比2:1混合,混合后溶液中离子浓度从大到小排序为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】纯碱工业始于 18 世纪末,至今已有两百多年。在纯碱工业史上,比利时人索尔维,中国人侯德榜等都作出了突出的贡献。据此完成下面小题。
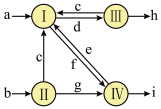
1.下图是1861年索尔维发明的制碱法中物质转化关系图,其中I~IV代表四个主要化学反应,a~i代表除H2O以外不同的物质。若不计其他损耗,,下列说法正确的是( )
2.从母液中析出的NaHCO3中含有NH4Cl,需洗涤后再进行灼烧。若省略洗涤操作,则最终对所得纯碱纯度影响叙述正确的是( )
3.化工专家侯德榜发明的"侯氏制碱法"大大推进了纯碱工业的发展,其最重要贡献是( )
1.下图是1861年索尔维发明的制碱法中物质转化关系图,其中I~IV代表四个主要化学反应,a~i代表除H2O以外不同的物质。若不计其他损耗,,下列说法正确的是( )

| A.水溶液呈碱性的物质只有e、g、h |
| B.水溶液呈酸性的物质只有c、f、i |
| C.每消耗1mol a,同时消耗0.5mol b |
| D.每消耗1mol h,同时消耗0.5mol i |
| A.无明显影响 | B.NH4Cl杂质含量上升 |
| C.NaCl杂质含量上升 | D.NaOH杂质含量上升 |
| A.找到了新型高效的催化剂 | B.充分利用了能量 |
| C.提高了纯碱产品的纯度 | D.提升了Na+的利用率 |
您最近一年使用:0次



