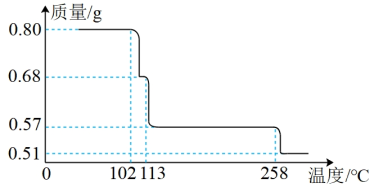
80g CuSO4•5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示。
请回答下列问题:
(1)试确定 200℃时固体物质的化学式_________ ;
(2)取 270℃所得样品,于 570℃灼烧得到的主要产物是黑色粉末和一种氧化性气体,该反应的化学方程式为_______________________ 。把该黑色粉末溶解于稀硫酸中,经浓缩、冷却,有晶体析出,该晶体的化学式为__________ ,其存在的最高温度是__________ ;
(3)上述氧化性气体与水反应生成一种化合物,该化合物的浓溶液与Cu在加热时发生反应的化学方程式为_______________________ 。

请回答下列问题:
(1)试确定 200℃时固体物质的化学式
(2)取 270℃所得样品,于 570℃灼烧得到的主要产物是黑色粉末和一种氧化性气体,该反应的化学方程式为
(3)上述氧化性气体与水反应生成一种化合物,该化合物的浓溶液与Cu在加热时发生反应的化学方程式为
更新时间:2018-11-04 08:43:22
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】雾霾严重影响人们的生活与健康,某地区的雾霾中可能含有如下可溶性无机离子: 、
、 、
、 、
、 、
、 、
、 、
、 、
、 。某同学收集了该地区的雾霾,经必要的预处理后配成试样溶液,设计并完成了如下的实验:
。某同学收集了该地区的雾霾,经必要的预处理后配成试样溶液,设计并完成了如下的实验:
①取试样溶液100mL,向其中加入足量 溶液,得到白色沉淀
溶液,得到白色沉淀 ,滴入足量盐酸,沉淀质量不变,得224mL无色气体
,滴入足量盐酸,沉淀质量不变,得224mL无色气体 标准状况
标准状况 。
。
②另取试样溶液100mL,向其中加入足量NaOH溶液,得到白色沉淀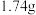 ,再滴入足量盐酸沉淀全部溶解。
,再滴入足量盐酸沉淀全部溶解。
(1)该雾霾中肯定不含的离子为_______ 。
(2)
_______  。
。
(3)该雾霾中 是否存在?
是否存在?_______  填“存在”或“不存在”
填“存在”或“不存在” ;若存在,浓度范围是
;若存在,浓度范围是_______  若不存在,则不必回答第2问
若不存在,则不必回答第2问 。
。
(4)沉淀称量前需洗涤,请描述洗涤沉淀的方法_______ 。
(5)操作 中加盐酸沉淀溶解的离子反应方程式为
中加盐酸沉淀溶解的离子反应方程式为_______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 。某同学收集了该地区的雾霾,经必要的预处理后配成试样溶液,设计并完成了如下的实验:
。某同学收集了该地区的雾霾,经必要的预处理后配成试样溶液,设计并完成了如下的实验:①取试样溶液100mL,向其中加入足量
 溶液,得到白色沉淀
溶液,得到白色沉淀 ,滴入足量盐酸,沉淀质量不变,得224mL无色气体
,滴入足量盐酸,沉淀质量不变,得224mL无色气体 标准状况
标准状况 。
。②另取试样溶液100mL,向其中加入足量NaOH溶液,得到白色沉淀
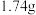 ,再滴入足量盐酸沉淀全部溶解。
,再滴入足量盐酸沉淀全部溶解。(1)该雾霾中肯定不含的离子为
(2)

 。
。(3)该雾霾中
 是否存在?
是否存在? 填“存在”或“不存在”
填“存在”或“不存在” ;若存在,浓度范围是
;若存在,浓度范围是 若不存在,则不必回答第2问
若不存在,则不必回答第2问 。
。(4)沉淀称量前需洗涤,请描述洗涤沉淀的方法
(5)操作
 中加盐酸沉淀溶解的离子反应方程式为
中加盐酸沉淀溶解的离子反应方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整 (所需试剂从稀HNO3、稀H2SO4、稀HCl、蒸馏水中选择):取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,__________ ,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D为四种可溶性的盐,它们包含的阳离子和阴离子分别为Ba2+、Ag+、Na+、Cu2+和NO3-、SO42-、Cl-、CO32-(离子在物质中不能重复出现)。
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。根据①②实验事实可推断它们的化学式为:
(1)A____________ D ______________ ;
(2)写出盐酸与B反应的离子方程式:__________________ ;
(3)将含相同物质的量A、B、C的溶液混合后,混合后溶液中存在的离子为_______ ;在此溶液中加入铁粉,写出发生反应的离子方程式_______________ ;
(4)若现有某E溶液,确定该溶液中是否含SO42﹣的检验方法是:______ 。
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。根据①②实验事实可推断它们的化学式为:
(1)A
(2)写出盐酸与B反应的离子方程式:
(3)将含相同物质的量A、B、C的溶液混合后,混合后溶液中存在的离子为
(4)若现有某E溶液,确定该溶液中是否含SO42﹣的检验方法是:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室可用下图装置对铜与浓硫酸的反应进行探究。

(1)加热条件下铜与浓硫酸反应的化学方程式___________ 。
(2)将产生的气体通入品红溶液中的现象___________ ,通入紫色石蕊溶液中的现象___________ 。
(3)一定条件下,在容积为 的密闭容器中发生反应:
的密闭容器中发生反应: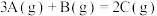 。开始时加入
。开始时加入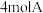 、
、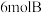 、
、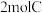 ,在
,在 末测得A的物质的量是
末测得A的物质的量是 。用A的浓度变化表示反应的平均速率:
。用A的浓度变化表示反应的平均速率:__________ 。

(1)加热条件下铜与浓硫酸反应的化学方程式
(2)将产生的气体通入品红溶液中的现象
(3)一定条件下,在容积为
 的密闭容器中发生反应:
的密闭容器中发生反应: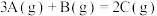 。开始时加入
。开始时加入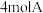 、
、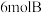 、
、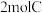 ,在
,在 末测得A的物质的量是
末测得A的物质的量是 。用A的浓度变化表示反应的平均速率:
。用A的浓度变化表示反应的平均速率:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上煅烧含硫矿物产生的SO2可以按如下流程脱除或利用。
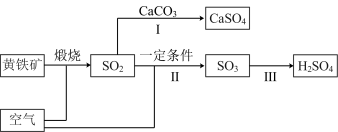
(1)下列说法正确的是_______。
(2)在足量空气中煅烧燃煤,产生的低浓度SO2可以在炉内添加CaCO3通过途径Ⅰ脱除,并产生一种无毒的气体,写出该反应的化学方程式_______ 。
(3)几位同学围绕浓硫酸的化学性质进行了如下探究实验:将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀;然后再加入适量浓硫酸,迅速搅拌,观察到蔗糖逐渐变黑,体积膨胀,并产生有刺激性气味的气体;
①写出产生刺激性气味气体的反应的化学方程式_______ 。
②上述实验现象表明浓硫酸具有_______ (填字母)。
a.酸性 b.脱水性 c.强氧化性 d.挥发性
③某同学将收集到的刺激性气味气体通入品红溶液,品红溶液褪色。然后在该试管口套上气球,将无色溶液加热恢复至红色,冷却后,发现溶液颜色再次变浅。解释“无色→红色→颜色变浅”变化的原因_______ 。

(1)下列说法正确的是_______。
| A.工业上还可以用硫黄代替黄铁矿制备SO2 |
| B.步骤I,如果通入过量空气,可以实现SO2的完全转化 |
| C.SO2是无色、无臭、有毒的气体,易溶于水 |
| D.步骤Ⅲ用浓硫酸吸收SO3 |
(2)在足量空气中煅烧燃煤,产生的低浓度SO2可以在炉内添加CaCO3通过途径Ⅰ脱除,并产生一种无毒的气体,写出该反应的化学方程式
(3)几位同学围绕浓硫酸的化学性质进行了如下探究实验:将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀;然后再加入适量浓硫酸,迅速搅拌,观察到蔗糖逐渐变黑,体积膨胀,并产生有刺激性气味的气体;
①写出产生刺激性气味气体的反应的化学方程式
②上述实验现象表明浓硫酸具有
a.酸性 b.脱水性 c.强氧化性 d.挥发性
③某同学将收集到的刺激性气味气体通入品红溶液,品红溶液褪色。然后在该试管口套上气球,将无色溶液加热恢复至红色,冷却后,发现溶液颜色再次变浅。解释“无色→红色→颜色变浅”变化的原因
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】根据物质所处的类别,以及是否具有氧化性或还原性能帮助我们认识其化学性质。
(1)根据下图所示物质的转化信息书写相应的反应方程式。以红土镍矿(主要成分Ni2O3、Fe2O3、SiO2)为原料制备兰尼镍的工艺流程如图所示:

①“酸溶”时,Fe2O3反应的离子方程式为____________ ;
②“还原”步骤中铁元素转化时对应离子方程式(已知H2S是弱酸)为____________ 。
(2)请从下列试剂中选择合适的试剂完成指定转化(试剂可以重复选择)。
试剂:浓盐酸、NaCl溶液、浓硫酸、Na2SO4溶液、FeSO4溶液
①Cl2→Cl-的离子方程式:____________ ;
②H2S→SO2的化学方程式:____________ ;
③Ba(OH)2→NaOH的化学方程式:____________ 。
(1)根据下图所示物质的转化信息书写相应的反应方程式。以红土镍矿(主要成分Ni2O3、Fe2O3、SiO2)为原料制备兰尼镍的工艺流程如图所示:

①“酸溶”时,Fe2O3反应的离子方程式为
②“还原”步骤中铁元素转化时对应离子方程式(已知H2S是弱酸)为
(2)请从下列试剂中选择合适的试剂完成指定转化(试剂可以重复选择)。
试剂:浓盐酸、NaCl溶液、浓硫酸、Na2SO4溶液、FeSO4溶液
①Cl2→Cl-的离子方程式:
②H2S→SO2的化学方程式:
③Ba(OH)2→NaOH的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】铁及其化合物在日常生产生活中应用广泛,研究铁及其化合物的应用意义重大。FeSO4•7H2O广泛用于医药和工业领域,以下是测定某补血剂(有效成分为FeSO4•7H2O)中铁元素含量的流程图。根据题意完成下列填空:

(1)人体能够吸收的是+2价的铁,但是+2价的铁很容易被氧化。补血剂与维生素C一起服用,有利于+2价铁的吸收。由此可推知,维生素C具有____________ (填“氧化性”或“还原性”)。
(2)步骤Ⅱ需要100mL1mol·L-1的稀硫酸,实验室用质量分数为98%的浓硫酸(密度为1.84g·cm-3)来配制,需用量筒量取浓硫酸____________ mL。
(3)步骤Ⅲ所得滤液中滴加KSCN溶液后滤液变为红色,则滤液中含有____________ (填离子符号)。检验滤液中还存在Fe2+,应选用的试剂为____________ (填字母)
A.NaCl溶液B.酸性KMnO4溶液C.NaOH溶液
(4)步骤Ⅳ加入过量H2O2的目的是____________ (用离子方程式表示)。
(5)步骤Ⅵ的一系列操作依次是:①过滤②洗涤③____________ ④冷却⑤称量⑥恒重操作,操作⑥的目的是____________ 。
(6)假设实验无损耗,则每片补血剂含铁元素的质量为____________ g(用含a的代数式表示)。

(1)人体能够吸收的是+2价的铁,但是+2价的铁很容易被氧化。补血剂与维生素C一起服用,有利于+2价铁的吸收。由此可推知,维生素C具有
(2)步骤Ⅱ需要100mL1mol·L-1的稀硫酸,实验室用质量分数为98%的浓硫酸(密度为1.84g·cm-3)来配制,需用量筒量取浓硫酸
(3)步骤Ⅲ所得滤液中滴加KSCN溶液后滤液变为红色,则滤液中含有
A.NaCl溶液B.酸性KMnO4溶液C.NaOH溶液
(4)步骤Ⅳ加入过量H2O2的目的是
(5)步骤Ⅵ的一系列操作依次是:①过滤②洗涤③
(6)假设实验无损耗,则每片补血剂含铁元素的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】过氧化钠(Na2O2)常用作漂白剂、杀菌剂、供氧剂,能与水和二氧化碳等物质发生反应,保存不当时容易变质。某实验小组以过氧化钠为研究对象进行了如下实验。
(1)探究 Na2O2样品是否已经变质:Na2O2在空气中久置易变质生成_______ ,现取少量样品加水溶解,加入_______ 溶液,充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该实验小组为了粗略测定这包Na2O2样品的质量分数,称取了m g样品,并设计如图所示装置来测定过氧化钠的质量分数。
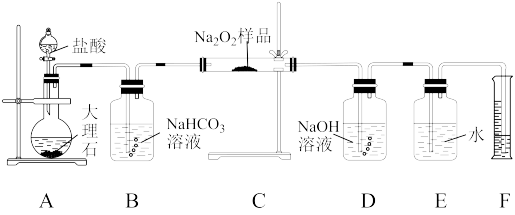
已知:饱和NaHCO3溶液的作用是除去CO2中的HCl气体,E和F是排水集气装置。
①写出装置C中发生的主要反应的化学方程式:_______ 。
②装置D的作用是_______ 。
③反应结束,待冷却后读出量筒内水的体积,将其折算成O2的质量为n g,则样品中过氧化钠的质量分数为_______ ×100%(用含m、n的最简式表示)。
(1)探究 Na2O2样品是否已经变质:Na2O2在空气中久置易变质生成
(2)该实验小组为了粗略测定这包Na2O2样品的质量分数,称取了m g样品,并设计如图所示装置来测定过氧化钠的质量分数。

已知:饱和NaHCO3溶液的作用是除去CO2中的HCl气体,E和F是排水集气装置。
①写出装置C中发生的主要反应的化学方程式:
②装置D的作用是
③反应结束,待冷却后读出量筒内水的体积,将其折算成O2的质量为n g,则样品中过氧化钠的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】铁是人体必需的微量元素,严重缺铁时需要服用补铁剂。实验小组为研究某补铁剂中铁元素的价态及其含量,设计并进行了如下实验:
【查阅资料】
Ⅰ.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
Ⅱ.KSCN中的硫元素为 价。
价。
实验Ⅰ.检验该补铁剂中铁元素的价态。

(1)试剂1是_______ ,试剂2是_______ (写出物质名称)。
(2)加入试剂2后溶液变为浅红色,此现象说明溶液①中含有_______ (填微粒符号)。
(3)能证明溶液①中含有 的实验现象是
的实验现象是_______ 。
(4)写出上述条件下 与
与 发生反应的离子方程式:
发生反应的离子方程式:_______ 。
(5)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的 与
与 发生了化学反应。甲同学猜测的理论依据是
发生了化学反应。甲同学猜测的理论依据是_______ 。
实验Ⅱ.测定该补铁剂中铁元素的含量。

(6)计算每片该补铁剂含铁元素的质量为_______ g。
【查阅资料】
Ⅰ.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
Ⅱ.KSCN中的硫元素为
 价。
价。实验Ⅰ.检验该补铁剂中铁元素的价态。

(1)试剂1是
(2)加入试剂2后溶液变为浅红色,此现象说明溶液①中含有
(3)能证明溶液①中含有
 的实验现象是
的实验现象是(4)写出上述条件下
 与
与 发生反应的离子方程式:
发生反应的离子方程式:(5)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的
 与
与 发生了化学反应。甲同学猜测的理论依据是
发生了化学反应。甲同学猜测的理论依据是实验Ⅱ.测定该补铁剂中铁元素的含量。

(6)计算每片该补铁剂含铁元素的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】草酸晶体的化学式可表示为 (其中
(其中 显
显 价),为测定x的值,进行下列实验:①称取wg某草酸晶体配成
价),为测定x的值,进行下列实验:①称取wg某草酸晶体配成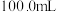 的水溶液,②取
的水溶液,②取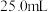 所配溶液置于锥形瓶中,加入适量稀
所配溶液置于锥形瓶中,加入适量稀 ,用浓度为cmol/L的
,用浓度为cmol/L的 溶液滴定,所发生的离子方程式为:
溶液滴定,所发生的离子方程式为: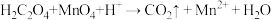
(1)配平离子方程式:
__________  +
+__________  +
+__________ 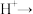
__________ 
__________ 
__________ 
(2)滴定时,指示剂应__________ (若加则写出指示剂的名称,若不加则写不加),滴定终点的颜色变化为__________ .
(3)当w为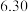 克、
克、 为
为 、滴定终点时消耗
、滴定终点时消耗 的体积为
的体积为 ,则x=
,则x=__________ .
(4)若滴定时所用 溶液的浓度因久置而变小,则
溶液的浓度因久置而变小,则 的值会
的值会__________ (填“偏大”、“偏小”或“不变”),对于一定量草酸,所用 的浓度过浓或过稀均不合理,浓度过浓或浓度过稀不合理的原因是
的浓度过浓或过稀均不合理,浓度过浓或浓度过稀不合理的原因是__________ .
(5)在滴定过程中常常将锥形瓶的内壁用清水冲洗,原因是____________________________ ,滴定时常发现反应速率开始缓慢,后来逐渐加快,估计原因可能是____________________ 。
 (其中
(其中 显
显 价),为测定x的值,进行下列实验:①称取wg某草酸晶体配成
价),为测定x的值,进行下列实验:①称取wg某草酸晶体配成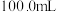 的水溶液,②取
的水溶液,②取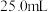 所配溶液置于锥形瓶中,加入适量稀
所配溶液置于锥形瓶中,加入适量稀 ,用浓度为cmol/L的
,用浓度为cmol/L的 溶液滴定,所发生的离子方程式为:
溶液滴定,所发生的离子方程式为: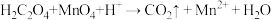
(1)配平离子方程式:
 +
+ +
+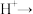



(2)滴定时,指示剂应
(3)当w为
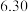 克、
克、 为
为 、滴定终点时消耗
、滴定终点时消耗 的体积为
的体积为 ,则x=
,则x=(4)若滴定时所用
 溶液的浓度因久置而变小,则
溶液的浓度因久置而变小,则 的值会
的值会 的浓度过浓或过稀均不合理,浓度过浓或浓度过稀不合理的原因是
的浓度过浓或过稀均不合理,浓度过浓或浓度过稀不合理的原因是(5)在滴定过程中常常将锥形瓶的内壁用清水冲洗,原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
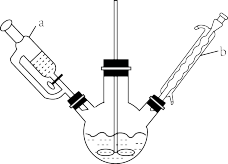
【推荐2】山梨酸酯是一类广谱、高效、低毒的防腐保鲜剂,在食品加工、果蔬保鲜等方面有重要的实用价值,其中山梨酸正丁酯抑菌能力最强,实验室用如图所示装置(夹持、加热装置省略),依据下面的原理制备山梨酸正丁酯。
实验步骤:
在三口烧瓶中加入11.2g山梨酸、14.8g正丁醇、少量催化剂和几粒沸石,水浴加热三口烧瓶,使反应体系保持微沸,回流4小时后停止加热和搅拌,反应液冷却至室温,滤去催化剂和沸石,将滤液倒入200 水中,加入50
水中,加入50 乙醚,倒入分液漏斗中,分液。有机层先用
乙醚,倒入分液漏斗中,分液。有机层先用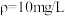 的碳酸氢钠溶液洗涤至中性,再用水洗涤分液,收集有机层。在有机层中加入少量无水
的碳酸氢钠溶液洗涤至中性,再用水洗涤分液,收集有机层。在有机层中加入少量无水 ,静置片刻,过滤。将滤液进行蒸馏,蒸去乙醚,得到纯净的山梨酸正丁酯12.0g。回答下列问题:
,静置片刻,过滤。将滤液进行蒸馏,蒸去乙醚,得到纯净的山梨酸正丁酯12.0g。回答下列问题:
(1)仪器a的名称是___________ ;仪器b的作用是___________ 。
(2)洗涤、分液过程中,加入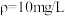 的碳酸氢钠溶液的目的是
的碳酸氢钠溶液的目的是___________ ,之后再用水洗的主要目的是___________ 。
(3)在上述洗涤、分液操作过程中,应先充分振荡,然后静置,待分层后___________(填选项字母)。
(4)实验中加入少量无水 ,的目的是
,的目的是___________ 。
(5)本实验中,山梨酸正丁酯的产率是___________ 。(精确至0.1%)。
(6)为提高反应正向进行的程度,实验室常使用如图所示装置(夹持、加热装置已略去)提高产物的产率。下列说法正确的是___________(填选项字母)。
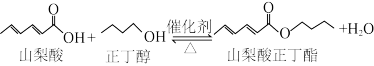
| 物质 | 相对分子质量 | 密度/( ) ) | 沸点/℃ | 水溶性 |
| 山梨酸 | 112 | 1.204 | 228 | 易溶 |
| 正丁醇 | 74 | 0.8089 | 117 | 溶 |
| 山梨酸正丁酯 | 168 | 0.926 | 195 | 难溶 |
| 乙醚 | 74 | 0.714 | 34.6 | 难溶 |
| 环己烷 | 84 | 0.779 | 80.7 | 难溶 |
在三口烧瓶中加入11.2g山梨酸、14.8g正丁醇、少量催化剂和几粒沸石,水浴加热三口烧瓶,使反应体系保持微沸,回流4小时后停止加热和搅拌,反应液冷却至室温,滤去催化剂和沸石,将滤液倒入200
 水中,加入50
水中,加入50 乙醚,倒入分液漏斗中,分液。有机层先用
乙醚,倒入分液漏斗中,分液。有机层先用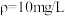 的碳酸氢钠溶液洗涤至中性,再用水洗涤分液,收集有机层。在有机层中加入少量无水
的碳酸氢钠溶液洗涤至中性,再用水洗涤分液,收集有机层。在有机层中加入少量无水 ,静置片刻,过滤。将滤液进行蒸馏,蒸去乙醚,得到纯净的山梨酸正丁酯12.0g。回答下列问题:
,静置片刻,过滤。将滤液进行蒸馏,蒸去乙醚,得到纯净的山梨酸正丁酯12.0g。回答下列问题:(1)仪器a的名称是
(2)洗涤、分液过程中,加入
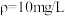 的碳酸氢钠溶液的目的是
的碳酸氢钠溶液的目的是(3)在上述洗涤、分液操作过程中,应先充分振荡,然后静置,待分层后___________(填选项字母)。
| A.直接将有机层从分液漏斗的上口倒出 |
| B.直接将有机层从分液漏斗的下口放出 |
| C.先将水层从分液漏斗的下口放出,再将有机层从下口放出 |
| D.先将水层从分液漏斗的下口放出,再将有机层从上口倒出 |
 ,的目的是
,的目的是(5)本实验中,山梨酸正丁酯的产率是
(6)为提高反应正向进行的程度,实验室常使用如图所示装置(夹持、加热装置已略去)提高产物的产率。下列说法正确的是___________(填选项字母)。
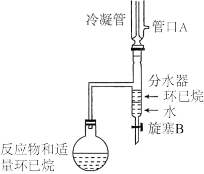
| A.管口A是冷凝水的出水口 |
| B.环己烷可将反应产生的水及时带出 |
| C.工作一段时间后,当环己烷即将流回烧瓶中时,必须将分水器中的水和环己烷放出 |
| D.工作一段时间后,环己烷可在烧瓶与分水器中循环流动 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
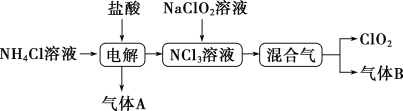
【推荐3】世界环保联盟建议全面禁止使用氯气用于饮用水的消毒,而建议采用高效“绿色”消毒剂二氧化氯。二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或加热。实验室以电解法制备ClO2的流程如图:
已知:①NCl3是黄色黏稠状液体或斜方形晶体,极易爆炸,有类似氯气的刺激性气味,自燃爆炸点为95℃,在热水中易分解,在空气中易挥发,不稳定。
②气体B能使湿润的红色石蕊试纸变蓝。
回答下列问题:
(1)电解时,发生反应的化学方程式为__ 。实验室制备气体B的化学方程式为__ 。为保证实验的安全,在电解时需注意的问题是:
①控制好生成NCl3的浓度;
②_______ 。
(2)NCl3与NaClO2(亚氯酸钠)按物质的量之比为1∶6混合,在溶液中恰好反应生成ClO2,该反应的离子方程式为__ 。
(3)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10mL,稀释成100mL试样;
步骤2:量取V1mL试样加入锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,摇匀,在暗处静置30min;
步骤3:以淀粉溶液做指示剂,用cmol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2mL。(已知I2+2S2O =2I-+S4O
=2I-+S4O )
)
①上述步骤3中滴定终点的现象是__ 。
②根据上述步骤可计算出原ClO2溶液的浓度为___ g /L(用含字母的代数式表示)

已知:①NCl3是黄色黏稠状液体或斜方形晶体,极易爆炸,有类似氯气的刺激性气味,自燃爆炸点为95℃,在热水中易分解,在空气中易挥发,不稳定。
②气体B能使湿润的红色石蕊试纸变蓝。
回答下列问题:
(1)电解时,发生反应的化学方程式为
①控制好生成NCl3的浓度;
②
(2)NCl3与NaClO2(亚氯酸钠)按物质的量之比为1∶6混合,在溶液中恰好反应生成ClO2,该反应的离子方程式为
(3)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10mL,稀释成100mL试样;
步骤2:量取V1mL试样加入锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,摇匀,在暗处静置30min;
步骤3:以淀粉溶液做指示剂,用cmol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2mL。(已知I2+2S2O
 =2I-+S4O
=2I-+S4O )
)①上述步骤3中滴定终点的现象是
②根据上述步骤可计算出原ClO2溶液的浓度为
您最近一年使用:0次



