高锰酸钾和浓盐酸可以发生下列反应:2KMnO4+16HCl(浓)===5Cl2↑+2MnCl2+2KCl+8H2O
(1)用双线桥法表示此反应的电子转移的方向及数目_____________
(2)该反应的氧化剂是______ ,还原剂是________ 。HCl表现 ___________ 性和 ____ 性。
(3)若消耗0.2 mol氧化剂,转移电子的物质的量是________ mol。生成氯气在标准状况下的体积是__________
(1)用双线桥法表示此反应的电子转移的方向及数目
(2)该反应的氧化剂是
(3)若消耗0.2 mol氧化剂,转移电子的物质的量是
更新时间:2018/11/17 21:43:34
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】以下有水参与的化学反应都属于氧化还原反应,但水既不做氧化剂又不做还原剂的有_______ 。
①2Na2O2+2H2O=4NaOH+O2↑
②Cl2+H2O=HCl+HClO
③C+H2O=CO+H2
④3NO2+H2O=2HNO3+NO
⑤2Na+2H2O=2NaOH+H2↑
⑥2F2+2H2O=4HF+O2
①2Na2O2+2H2O=4NaOH+O2↑
②Cl2+H2O=HCl+HClO
③C+H2O=CO+H2
④3NO2+H2O=2HNO3+NO
⑤2Na+2H2O=2NaOH+H2↑
⑥2F2+2H2O=4HF+O2
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】(Ⅰ)如图为一“铁链”图案,小明在图案上分别写了H2、CO2、Na2O、NaCl、FeCl3五种物质,图中相连的两种物质均可归属为一类,相交部分A、B、C、D为其相应的分类依据代号。请回答下列问题:
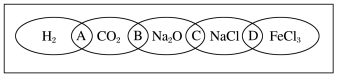
(1)请将分类依据代号填入相应的括号内:
( ) 两种物质都不是电解质
( ) 两种物质都是盐
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入饱和的图中某种物质M的溶液加热至呈红褐色。
①物质M的化学式为________________ 。
②证明有红褐色胶体生成的实验操作是____ 。
(Ⅱ)反应:
A.2F2+2H2O=4HF+O2↑; B.2Na+2H2O=2NaOH+H2↑;
C.CaO+H2O=Ca(OH)2; D.2H2O=2H2↑+O2↑。
其中水只是氧化剂的是______ (填序号),反应B中被氧化的元素名称是________ 。
(Ⅲ)反应:3Cu + 8HNO3 = 3Cu(NO3)2+2NO↑+4H2O, 硝酸在该反应中的作用是______ 还原剂与氧化剂的物质的量之比:__________

(1)请将分类依据代号填入相应的括号内:
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入饱和的图中某种物质M的溶液加热至呈红褐色。
①物质M的化学式为
②证明有红褐色胶体生成的实验操作是
(Ⅱ)反应:
A.2F2+2H2O=4HF+O2↑; B.2Na+2H2O=2NaOH+H2↑;
C.CaO+H2O=Ca(OH)2; D.2H2O=2H2↑+O2↑。
其中水只是氧化剂的是
(Ⅲ)反应:3Cu + 8HNO3 = 3Cu(NO3)2+2NO↑+4H2O, 硝酸在该反应中的作用是
您最近一年使用:0次
【推荐1】高铁酸钠(化学式为 Na2FeO4)是一种新型净水剂,工业上常通过如下化学反应制取:用双线桥在氧化还原方程式中标出电子转移的方向和数目___________ Fe2O3+3NaNO3+4NaOH=2Na2FeO4+3NaNO2+2H2O,该生成物 Na2FeO4 中 Fe 元素的化合价为___________ ,被氧化的元素为___________ ,氧化剂为___________ ,氧化产物为___________ ,
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】已知铜和浓硫酸可以在加热条件下发生反应(已配平):Cu+2H2SO4 CuSO4+A↑+2H2O。试通过计算和推理完成下面的问题
CuSO4+A↑+2H2O。试通过计算和推理完成下面的问题
(1)此反应中,硫酸体现了________ 性和________ 性。
(2)A物质可以导致酸雨的形成。A应该属于________ 。(用字母代号填写)
a.酸 b.碱 c.盐 d.酸性氧化物 e.碱性氧化物
(3)A可使紫红色的酸性KMnO4溶液褪色,此褪色反应中(填写化学式,下同)______ 失去电子,氧化剂是______ 。
(4)足量的铜片与浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,生成的CuSO4的物质的量为________ mol,生成的A气体在标准状况下体积为_____ L(假设气体全部逸出)
 CuSO4+A↑+2H2O。试通过计算和推理完成下面的问题
CuSO4+A↑+2H2O。试通过计算和推理完成下面的问题(1)此反应中,硫酸体现了
(2)A物质可以导致酸雨的形成。A应该属于
a.酸 b.碱 c.盐 d.酸性氧化物 e.碱性氧化物
(3)A可使紫红色的酸性KMnO4溶液褪色,此褪色反应中(填写化学式,下同)
(4)足量的铜片与浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,生成的CuSO4的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】现有①KMnO4②H2③O2④CL2⑤CO ⑥Al 六种物质,从氧化性、还原性的角度分类,若将常用的氧化剂放入甲中,常用的还原剂放入乙中,则:
⑴甲中有_______ ;乙中有______ 。(填序号)
___________________________________
⑷一氧化氮是工业制硝酸的中间产物,生成一氧化氮的化学方程式为:
⑴甲中有
⑵由Fe 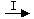 Fe3O4 ,Fe2O3
Fe3O4 ,Fe2O3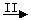 Fe 可知,欲实现I反应过程应从
Fe 可知,欲实现I反应过程应从
⑷一氧化氮是工业制硝酸的中间产物,生成一氧化氮的化学方程式为:
4X+5O2 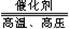 4NO+6H2O,则根据质量守恒定律可以推出X的化学式为
4NO+6H2O,则根据质量守恒定律可以推出X的化学式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)《天工开物》记载:每炉甘石十斤,装载入一泥罐内,发火煅红,罐中炉甘石熔化成团,冷定毁罐取出,即倭铅也。该过程主反应为:ZnCO3+2C Zn+3CO↑。其中,做氧化剂的物质是
Zn+3CO↑。其中,做氧化剂的物质是______ ,被氧化的物质是_____
(2)在反应2KMnO4 + 16HCl = 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O 中,氧化剂是_______ ,还原剂是_________ ,氧化产物是__________ 。
 Zn+3CO↑。其中,做氧化剂的物质是
Zn+3CO↑。其中,做氧化剂的物质是(2)在反应2KMnO4 + 16HCl = 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O 中,氧化剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】如图是一块用FeCl3溶液与Cu反应制作的印刷电路板,其制作原理可用2FeCl3+Cu=CuCl2+2X表示。

(1)上式中X的化学式为________ 。
(2)在上述反应中,氧化剂为________ ,氧化产物为________ ,将两者的氧化性相比较,________ 的氧化性更强。
(3)若有32 g铜被氧化,则参与反应的FeCl3的质量为________ g。
(4)该反应的离子方程式为________________________________________________ 。

(1)上式中X的化学式为
(2)在上述反应中,氧化剂为
(3)若有32 g铜被氧化,则参与反应的FeCl3的质量为
(4)该反应的离子方程式为
您最近一年使用:0次
【推荐1】法医常用“马氏试砷法”检验是否砒霜(As2O3)中毒,其原理是用锌和盐酸与试样混合,若试样中含有砒霜,则会发生反应生成砷化氢(AsH3,H为+1价)气体,砷化氢再受热分解生成砷(As)单质,砷单质积聚而成亮黑色的“砷镜”,以此现象作为判断。涉及的化学反应如下:
② 2AsH3
 2As + 3H2↑
2As + 3H2↑回答下列有关问题:
(1)反应①中物质X的化学式为
(2)用
As2O3 + 6Zn + 12HCl = 2AsH3↑+ 6ZnCl2 + 3X
(3)还原性强弱:Zn
(4)反应②中被还原的元素是
(5)若反应①中产生的AsH3在反应②中全部被分解,则当反应②生成6个H2,反应①转移
您最近一年使用:0次
【推荐2】回答下列问题:
(1)下列粒子:①SO ②H2O③Na2O2④S2-⑤Fe⑥Al3+。在化学反应中可能被氧化也可能被还原的是
②H2O③Na2O2④S2-⑤Fe⑥Al3+。在化学反应中可能被氧化也可能被还原的是_______ (填写序号);若少量的②与③充分反应,固体物质增重了0.6g,则生成的气体在标准状况下的体积为_______ mL。
(2)在一定条件下,实验室分别用过氧化氢、高锰酸钾、氯酸钾、过氧化钠为原料制取氧气,当制得同温同压下相同体积的氧气时,四个反应中转移的电子的数之比为_______ 。
(3)H2O2被称为绿色消毒剂,可用于消除采矿业废液中的KCN,发生反应为KCN+H2O2+H2O=A+NH3↑,则A的化学式为_______ 。
(4)某反应体系中有六种粒子:H2O、S2-、S、H+、Mn2+、MnO ,其中S作氧化产物。写出并配平该反应的离子方程式
,其中S作氧化产物。写出并配平该反应的离子方程式_______ 。
(1)下列粒子:①SO
 ②H2O③Na2O2④S2-⑤Fe⑥Al3+。在化学反应中可能被氧化也可能被还原的是
②H2O③Na2O2④S2-⑤Fe⑥Al3+。在化学反应中可能被氧化也可能被还原的是(2)在一定条件下,实验室分别用过氧化氢、高锰酸钾、氯酸钾、过氧化钠为原料制取氧气,当制得同温同压下相同体积的氧气时,四个反应中转移的电子的数之比为
(3)H2O2被称为绿色消毒剂,可用于消除采矿业废液中的KCN,发生反应为KCN+H2O2+H2O=A+NH3↑,则A的化学式为
(4)某反应体系中有六种粒子:H2O、S2-、S、H+、Mn2+、MnO
 ,其中S作氧化产物。写出并配平该反应的离子方程式
,其中S作氧化产物。写出并配平该反应的离子方程式
您最近一年使用:0次

 受热分解的化学方程式为
受热分解的化学方程式为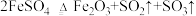 ,被氧化的元素为
,被氧化的元素为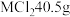 ,含有
,含有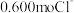 ,则金属M的相对原子质量为
,则金属M的相对原子质量为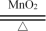 2KCl+3O2↑
2KCl+3O2↑ 2P2O5
2P2O5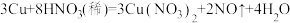
 与起酸性作用的
与起酸性作用的

