某同学在用锌与稀硫酸反应制氢气的实验中,发现加入少量硫酸铜溶液可以加快氢气的生成速率,请回答问题:
(1)上述实验中,发生反应的离子方程式是:_______________ ;________________________ 。
(2)少量硫酸铜溶液可以加快氢气的生成速率的原因是_______ 。
(3)实验室有Na2SO4、MgSO4、Ag2SO4等三种溶液,可与实验中的硫酸铜溶液起相似作用的是___________ 。
(4)为进一步研究硫酸铜的量对锌与硫酸反应生成氢气速率的影响,该同学设计了如下一系列的实验,将表中混合溶液加到6个盛有过量锌粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需要的时间:
请完成此实验设计:V2 =_________ V5=_________
(5)要加快锌与氢气的生成速率还可以采取的措施是________ (至少写两点)。
(1)上述实验中,发生反应的离子方程式是:
(2)少量硫酸铜溶液可以加快氢气的生成速率的原因是
(3)实验室有Na2SO4、MgSO4、Ag2SO4等三种溶液,可与实验中的硫酸铜溶液起相似作用的是
(4)为进一步研究硫酸铜的量对锌与硫酸反应生成氢气速率的影响,该同学设计了如下一系列的实验,将表中混合溶液加到6个盛有过量锌粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需要的时间:
| 混合溶液 | A | B | C | D | E | F |
| 4mol/LH2SO4/mL | 40 | 40 | V1 | 40 | 40 | V2 |
| 饱和CuSO4溶液/mL | 0 | 1 | 5 | V5 | V6 | 25 |
| H2O/mL | V3 | V4 | 20 | 15 | 5 | 0 |
请完成此实验设计:V2 =
(5)要加快锌与氢气的生成速率还可以采取的措施是
更新时间:2020-09-20 11:22:44
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.某实验小组对H2O2的分解做了如下探究。下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同的粉末状和块状的MnO2分别加入盛有15 ml 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
(1)写出上述实验中发生反应的化学方程式:______ 。
(2)实验结果表明,催化剂的催化效果与_____ 有关。
(3)某同学在10 mL H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的反应速率最慢的是_____ 。
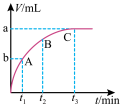
Ⅱ.某反应在体积为5L的恒容密闭容器中进行, 在0-3分钟内各物质的量的变化情况如图所示(A,B,C均为气体,且A气体有颜色)。
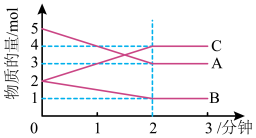
(4)该反应的的化学方程式为__________ 。
(5)反应开始至2分钟时,B的平均反应速率为____ 。
(6)能说明该反应已达到平衡状态的是____ 。
a.v(A)= 2v(B) b.容器内各物质的物质的量相等
c.v逆(A)=v正(C) d.容器内气体的颜色保持不变
(7)由图求得平衡时A的体积分数______ 。
| MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5min |
| 块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30min |
(1)写出上述实验中发生反应的化学方程式:
(2)实验结果表明,催化剂的催化效果与
(3)某同学在10 mL H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的反应速率最慢的是

Ⅱ.某反应在体积为5L的恒容密闭容器中进行, 在0-3分钟内各物质的量的变化情况如图所示(A,B,C均为气体,且A气体有颜色)。
(4)该反应的的化学方程式为
(5)反应开始至2分钟时,B的平均反应速率为
(6)能说明该反应已达到平衡状态的是
a.v(A)= 2v(B) b.容器内各物质的物质的量相等
c.v逆(A)=v正(C) d.容器内气体的颜色保持不变
(7)由图求得平衡时A的体积分数

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】草酸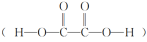 在工业上可作漂白剂、鞣革剂,也是实验室常用试剂。室温下利用H2C2O4溶液和酸性KMnO4溶液的反应探究外界条件对反应速率的影响,设计方案如下:
在工业上可作漂白剂、鞣革剂,也是实验室常用试剂。室温下利用H2C2O4溶液和酸性KMnO4溶液的反应探究外界条件对反应速率的影响,设计方案如下:
(1)上述反应的离子方程式为__ 。
(2)分析数据可得到的结论是__ 。
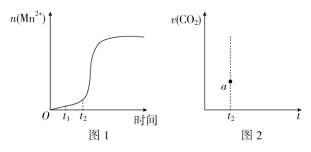
(3)该实验中若n(Mn2+)随时间变化趋势如图1所示,请于图2中画出t2后生成CO2的速率图象(从a点开始作图)___ ,并说明理由:__ 。
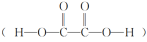 在工业上可作漂白剂、鞣革剂,也是实验室常用试剂。室温下利用H2C2O4溶液和酸性KMnO4溶液的反应探究外界条件对反应速率的影响,设计方案如下:
在工业上可作漂白剂、鞣革剂,也是实验室常用试剂。室温下利用H2C2O4溶液和酸性KMnO4溶液的反应探究外界条件对反应速率的影响,设计方案如下:| 实验编号 | 所加试剂及用量/mL | 溶液颜色褪至无色所需时间/min | |||
| 0.6mol/L H2C2O4溶液 | H2O | 0.01mol/L KMnO4溶液 | 3moL/L稀H2SO4 | ||
| 1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
| 2 | 2.0 | 3.0 | 3.0 | 2.0 | 5.2 |
| 3 | 1.0 | 4.0 | 3.0 | 2.0 | 6.4 |
(1)上述反应的离子方程式为
(2)分析数据可得到的结论是
(3)该实验中若n(Mn2+)随时间变化趋势如图1所示,请于图2中画出t2后生成CO2的速率图象(从a点开始作图)

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】我们可以通过实验探究来研究化学反应速率的影响因素,
(1)为探讨反应物浓度对化学反应速率的影响,已知:
反应Ⅰ S2O82-+2I-=2SO42-+I2(慢)反应Ⅱ I2+2S2O32-=2I-+S4O62-(快)
反应S2O82-+ 2S2O32-= 2SO42-+ S4O62-的反应速率由______________ 决定(填“反应Ⅰ”、“反应Ⅱ”),I-是此反应的___________________________ 。
浓度c(S2O82-)〜反应时间t的变化曲线如下图,若保持其他条件不变,请在答题卡坐标图中,分别画出降低反应温度和加入催化剂时c(S2O82-)〜t的变化曲线示意图(进行相应的标注)____________
(2)草酸与高锰酸钾在酸性条件下可以发生化学反应。请补全并配平下面方程式
______ H2C2O3+MnO4-+=Mn2++CO2+
现有0.00lmol/L的酸性KMnO4溶液和0.0lmol/L的草酸溶液,为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表:
通过实验①、③可探究草酸的浓度对反应速率的影响,表中Vx=_________ mL,理由是_________________ 。
对比实验①、②的实验现象是___________________________________ 。
(1)为探讨反应物浓度对化学反应速率的影响,已知:
反应Ⅰ S2O82-+2I-=2SO42-+I2(慢)反应Ⅱ I2+2S2O32-=2I-+S4O62-(快)
反应S2O82-+ 2S2O32-= 2SO42-+ S4O62-的反应速率由
浓度c(S2O82-)〜反应时间t的变化曲线如下图,若保持其他条件不变,请在答题卡坐标图中,分别画出降低反应温度和加入催化剂时c(S2O82-)〜t的变化曲线示意图(进行相应的标注)

(2)草酸与高锰酸钾在酸性条件下可以发生化学反应。请补全并配平下面方程式
现有0.00lmol/L的酸性KMnO4溶液和0.0lmol/L的草酸溶液,为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表:
实验序号 | 体积V/mL | 温度/℃ | ||
KMnO4溶液 | 水 | H2C2O4溶液 | ||
① | 4.0 | 0.0 | 2.0 | 25 |
② | 4.0 | 0.0 | 2.0 | 60 |
③ | 4.0 | Vx | 1.0 | 25 |
通过实验①、③可探究草酸的浓度对反应速率的影响,表中Vx=
对比实验①、②的实验现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.回答下列问题
(1)现有下列物质:①K2SO4晶体;②液态SO3;③冰醋酸;④铜;⑤小苏打;⑥蔗糖;⑦乙醇;⑧熔融的氯化钠;⑨NaOH溶液。其中:能导电的是___________ (填序号,下同);属于非电解质的是___________ ;属于强电解质的是___________ ;向③溶液中加入②,电离平衡___________ 移动;写出⑤在溶液中的电离方程式___________ ,写出③在溶液中电离方程式___________
Ⅱ.锌粉与稀硫酸反应产生氢气的体积时间关系如下图所示,选择正确的选项填空。
A.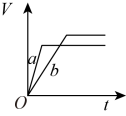 B.
B.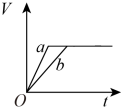 C.
C.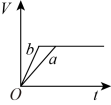 D.
D.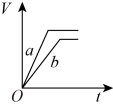
(2)将等质量的两份锌粉a、b分别加入过量的稀硫酸中,同时向a中加入少量的CuSO4溶液,产生H2的体积V(L)与时间t(min)的关系是___________ 。
(3)将过量的两份锌粉a、b分别加入定量的稀硫酸,同时向a中加入少量的CuSO4溶液,产生H2的体积V(L)与时间t(min)的关系是___________ 。
(4)将(3)中的CuSO4溶液改成CH3COONa溶液,其他条件不变,则图象是___________ 。
(1)现有下列物质:①K2SO4晶体;②液态SO3;③冰醋酸;④铜;⑤小苏打;⑥蔗糖;⑦乙醇;⑧熔融的氯化钠;⑨NaOH溶液。其中:能导电的是
Ⅱ.锌粉与稀硫酸反应产生氢气的体积时间关系如下图所示,选择正确的选项填空。
A.
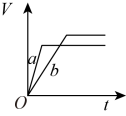 B.
B.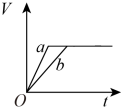 C.
C.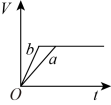 D.
D.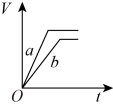
(2)将等质量的两份锌粉a、b分别加入过量的稀硫酸中,同时向a中加入少量的CuSO4溶液,产生H2的体积V(L)与时间t(min)的关系是
(3)将过量的两份锌粉a、b分别加入定量的稀硫酸,同时向a中加入少量的CuSO4溶液,产生H2的体积V(L)与时间t(min)的关系是
(4)将(3)中的CuSO4溶液改成CH3COONa溶液,其他条件不变,则图象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的项重大贡献。
(1)某课外实验小组欲探究铝和铜的金属性(原子失电子能力)强弱,同学们提出了如下实验方案:
A.比较铝和铜的硬度和熔点
B.比较二者在稀硫酸中的表现
C.用铝片、铜片、硫酸铝溶液、硫酸铜溶液,比较二者的活动性
D.分别做铝片、铜片与NaOH溶液反应的实验
E.将铝片、铜片用导线连接后共同投入稀盐酸中接入电流计,观察电流方向
上述方案中能达到实验目的的是_________________ 。
(2)现有如下两个反应:A.NaOH+HCl=NaCl+H2O B.Zn+H2SO4=ZnSO4+H2↑。上述反应中能设计成原电池的是________ (填字母代号),作负极的物质发生了________ 反应(填“氧化”或“还原”)。
(3)将纯锌片和纯铜片按如图所示方式插入100mL相同浓度的稀硫酸一段时间,回答下列问题:
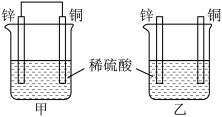
①下列说法正确的是________ (填字母代号)。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的酸性均减弱
②在相同时间内,两烧杯中产生气泡的速度:甲________ 乙(填“>”、“<”或“=”)。原因是________ 。
③当甲中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1L,测得溶液中c(H+)=0.1mol/L(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为____________ 。
(1)某课外实验小组欲探究铝和铜的金属性(原子失电子能力)强弱,同学们提出了如下实验方案:
A.比较铝和铜的硬度和熔点
B.比较二者在稀硫酸中的表现
C.用铝片、铜片、硫酸铝溶液、硫酸铜溶液,比较二者的活动性
D.分别做铝片、铜片与NaOH溶液反应的实验
E.将铝片、铜片用导线连接后共同投入稀盐酸中接入电流计,观察电流方向
上述方案中能达到实验目的的是
(2)现有如下两个反应:A.NaOH+HCl=NaCl+H2O B.Zn+H2SO4=ZnSO4+H2↑。上述反应中能设计成原电池的是
(3)将纯锌片和纯铜片按如图所示方式插入100mL相同浓度的稀硫酸一段时间,回答下列问题:

①下列说法正确的是
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的酸性均减弱
②在相同时间内,两烧杯中产生气泡的速度:甲
③当甲中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1L,测得溶液中c(H+)=0.1mol/L(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据要求回答下列问题:
反应 的能量变化趋势如图所示。
的能量变化趋势如图所示。
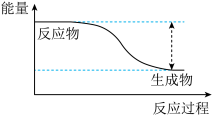
(1)该反应为___________ (填“吸热”或“放热”)反应。
(2)若要使该反应的反应速率加快,下列措施不可行的是___________(填字母)。
(3)欲区分葡萄糖和淀粉,可选用___________(填字母,下同)。
(4)氮的化合物常用作制冷剂的是___________ (填名称),向蔗糖中滴加少量浓硫酸并搅拌,出现“黑色面包”,并产生刺激性无色气体,这一现象显示浓硫酸的___________ (填性质)。
(5)燃煤排放的尾气中含有二氧化硫、氮的氧化物(主要为 )等污染物,工业上采用
)等污染物,工业上采用 碱性溶液作为吸收剂可同时对烟气进行脱硫、脱硝。脱硫的离子方程式为
碱性溶液作为吸收剂可同时对烟气进行脱硫、脱硝。脱硫的离子方程式为___________ ,实验证明相对于 ,
, 更难脱除,其原因可能是
更难脱除,其原因可能是___________ 。
反应
 的能量变化趋势如图所示。
的能量变化趋势如图所示。
(1)该反应为
(2)若要使该反应的反应速率加快,下列措施不可行的是___________(填字母)。
| A.将铁片改为铁粉 |
B.滴加少量 溶液 溶液 |
| C.升高温度 |
| D.将稀硫酸改为98%的浓硫酸 |
| A.碘水 | B.银氨溶液 | C.盐酸 | D. 溶液 溶液 |
(5)燃煤排放的尾气中含有二氧化硫、氮的氧化物(主要为
 )等污染物,工业上采用
)等污染物,工业上采用 碱性溶液作为吸收剂可同时对烟气进行脱硫、脱硝。脱硫的离子方程式为
碱性溶液作为吸收剂可同时对烟气进行脱硫、脱硝。脱硫的离子方程式为 ,
, 更难脱除,其原因可能是
更难脱除,其原因可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】以含钴废催化剂(主要成分为Co、Fe、SiO2)为原料制取复合氧化钴的流程如下:
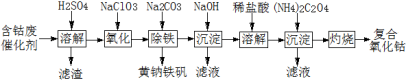
(1)用H2SO4溶解后过滤,得到的滤渣是____ (填化学式)。将滤渣洗涤2~3次,再将洗液与滤液合并的目的是____ 。
(2)在加热搅拌条件下加入NaClO3,将Fe2+氧化成Fe3+,反应的离子方程式是____ 。
(3)已知:铁氰化钾的化学式为K3[Fe(CN)6];亚铁氰化钾的化学式为K4[Fe(CN)6]。
3Fe2++2[Fe(CN)6]3− =Fe3[Fe(CN)6]2↓(蓝色沉淀)
4Fe3++3[Fe(CN)6]4− = Fe4[Fe(CN)6]3↓(蓝色沉淀)
确定Fe2+是否氧化完全的方法是____ 。(仅供选择的试剂:铁氰化钾溶液、亚铁氰化钾溶液、铁粉、KSCN溶液)
(4)向氧化后的溶液中加入适量的Na2CO3调节酸度,使之生成黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,写出该反应的离子方程式:____ 。
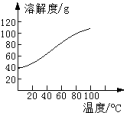
(5)已知CoCl2的溶解度曲线如图所示。向碱式碳酸钴沉淀中加入足量稀盐酸边加热边搅拌至完全溶解后,需趁热过滤的原因是____ 。

(1)用H2SO4溶解后过滤,得到的滤渣是
(2)在加热搅拌条件下加入NaClO3,将Fe2+氧化成Fe3+,反应的离子方程式是
(3)已知:铁氰化钾的化学式为K3[Fe(CN)6];亚铁氰化钾的化学式为K4[Fe(CN)6]。
3Fe2++2[Fe(CN)6]3− =Fe3[Fe(CN)6]2↓(蓝色沉淀)
4Fe3++3[Fe(CN)6]4− = Fe4[Fe(CN)6]3↓(蓝色沉淀)
确定Fe2+是否氧化完全的方法是
(4)向氧化后的溶液中加入适量的Na2CO3调节酸度,使之生成黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,写出该反应的离子方程式:
(5)已知CoCl2的溶解度曲线如图所示。向碱式碳酸钴沉淀中加入足量稀盐酸边加热边搅拌至完全溶解后,需趁热过滤的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示的初中化学中的一些重要实验,请回答下列问题:
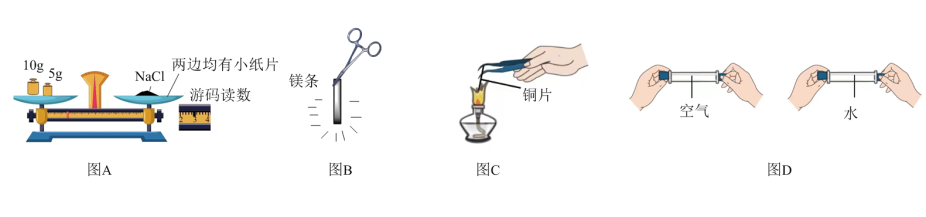
(1)图A称量NaCl的实际质量是___ 。
(2)图B反应的实验现象是__ 。
(3)图C反应的表达式为__ 。
(4)图D实验目的是__ 。

(1)图A称量NaCl的实际质量是
(2)图B反应的实验现象是
(3)图C反应的表达式为
(4)图D实验目的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】有5瓶白色固体试剂,分别是BaCl2、NaOH、Na2SO4、(NH4)2 SO4、无水CuSO4,现只提供蒸馏水,通过下面的步骤就可以鉴别它们。请填写下列空白:
(1)各取适量固体试剂分别加入5支试管中,加入适量蒸馏水,振荡试管,观察到5种固体全部溶解,1支试管中得到蓝色溶液,被检出物质的化学式是______________ 。
(2)分别取四种未检出的溶液,往其中加入上述已检出的溶液,观察到1支试管中有白色沉淀生成,则被检出物质的化学式是_________________ 和相应的化学方程式是_____________________ ;另1支试管中有蓝色沉淀生成,则被检出物质的化学式是___________ 和相应的化学方程式是___________ 。
(3)最后可利用已检出的_____________ (填化学式)溶液,来鉴别余下未检出的物质。相应的化学方程式是_________ 。
(1)各取适量固体试剂分别加入5支试管中,加入适量蒸馏水,振荡试管,观察到5种固体全部溶解,1支试管中得到蓝色溶液,被检出物质的化学式是
(2)分别取四种未检出的溶液,往其中加入上述已检出的溶液,观察到1支试管中有白色沉淀生成,则被检出物质的化学式是
(3)最后可利用已检出的
您最近一年使用:0次



