KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:______KClO3+______HCl(浓)===______KCl+______ClO2↑+______Cl2↑+______H2O
(1) 请配平上述化学方程式____________________________________ 。
(2) 浓盐酸在反应中显示出来的性质是__________ (填编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3) 产生0.1 mol Cl2,则转移的电子的物质的量为__________ mol。
(4) 氧化剂是__________ ,氧化产物是__________ 。
(1) 请配平上述化学方程式
(2) 浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3) 产生0.1 mol Cl2,则转移的电子的物质的量为
(4) 氧化剂是
更新时间:2018-12-05 20:22:11
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)有下列三个在溶液中发生的氧化还原反应:
Ⅰ.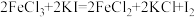
Ⅱ.
Ⅲ.
请根据上述反应分析推断后回答下列问题:
① 的氧化性由强到弱依次是
的氧化性由强到弱依次是___________ 。
②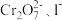 在强酸性溶液中能否大量共存?
在强酸性溶液中能否大量共存?___________ (请先回答“能”或“否”,“能”不用解释,“否”需要加以解释)
③在酸性溶液中存在大量的 ,则
,则 中能与
中能与 大量共存的离子有
大量共存的离子有___________
(2)草酸是一种常见的厕所清洁剂,它能与高锰酸钾溶液发生反应:
①补上产物并配平方程式;___________
②氧化剂与还原剂的物质的量之比为___________ 。
(1)有下列三个在溶液中发生的氧化还原反应:
Ⅰ.
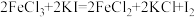
Ⅱ.

Ⅲ.

请根据上述反应分析推断后回答下列问题:
①
 的氧化性由强到弱依次是
的氧化性由强到弱依次是②
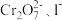 在强酸性溶液中能否大量共存?
在强酸性溶液中能否大量共存?③在酸性溶液中存在大量的
 ,则
,则 中能与
中能与 大量共存的离子有
大量共存的离子有(2)草酸是一种常见的厕所清洁剂,它能与高锰酸钾溶液发生反应:

①补上产物并配平方程式;
②氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】一个体重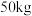 的健康人含铁
的健康人含铁 ,这
,这 铁在人体中不是以金属单质的形式存在,而是以
铁在人体中不是以金属单质的形式存在,而是以 和
和 的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。
的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。
(1)工业盐的主要成分是 ,以前有许多起因误食
,以前有许多起因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有___________ 性。工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有___________ 性。
(2)在 的反应中,还原剂是
的反应中,还原剂是___________ ,每有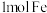 参加反应,被还原的
参加反应,被还原的 为
为___________  。
。
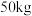 的健康人含铁
的健康人含铁 ,这
,这 铁在人体中不是以金属单质的形式存在,而是以
铁在人体中不是以金属单质的形式存在,而是以 和
和 的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。
的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。(1)工业盐的主要成分是
 ,以前有许多起因误食
,以前有许多起因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有(2)在
 的反应中,还原剂是
的反应中,还原剂是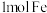 参加反应,被还原的
参加反应,被还原的 为
为 。
。
您最近一年使用:0次
【推荐3】回答下列问题
(1)某化学反应的反应物和产物如下:KMnO4+KI+H2SO4→MnSO4+I2+KIO3+K2SO4+H2O。
①该反应的氧化剂是_______ 。
②如果该反应方程式中I2和KIO3的化学计量数都是5。则KMnO4的化学计量数是_______ 。
(2)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4(Cr元素的化合价为+6)、Cr(OH)3(Cr元素的化合价为+3)、H2O、H2O2,已知该反应中H2O2只发生如下过程:H2O2→O2。
①该反应中的还原剂是_______ 。
②该反应中,发生还原反应的过程是_______→_______。_____
③写出该反应的化学方程式:_______ 。
(1)某化学反应的反应物和产物如下:KMnO4+KI+H2SO4→MnSO4+I2+KIO3+K2SO4+H2O。
①该反应的氧化剂是
②如果该反应方程式中I2和KIO3的化学计量数都是5。则KMnO4的化学计量数是
(2)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4(Cr元素的化合价为+6)、Cr(OH)3(Cr元素的化合价为+3)、H2O、H2O2,已知该反应中H2O2只发生如下过程:H2O2→O2。
①该反应中的还原剂是
②该反应中,发生还原反应的过程是_______→_______。
③写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】硫及其化合物在工业上有着广泛的应用。完成下列填空:
(1)写出工业上以硫磺为原料生产硫酸的第一步反应方程式______
(2)工业上用过硫酸钾(K2S2O8)测定钢铁中的锰含量,主要反应如下:____ Mn2++____ S2O82﹣+____ H2O→____ MnO4﹣+____ SO42﹣+______ H+。配平该反应方程式,氧化产物是______
(3)用电解硫酸氢钾的方法制取过硫酸钾:HSO4﹣在______ (填:“阳极”或“阴极”)反应生成S2O82﹣,另一极生成氢气,生成0.1mol的S2O82﹣同时可收集到______ g氢气
(4)已知硫酸的第二级电离并不完全:HSO4﹣ H++SO42﹣(Ki=1.2×10﹣2);在0.1mol/L的硫酸氢钾溶液中大约有30%的HSO4﹣电离,则该溶液中离子浓度由大到小排列第2位的离子是
H++SO42﹣(Ki=1.2×10﹣2);在0.1mol/L的硫酸氢钾溶液中大约有30%的HSO4﹣电离,则该溶液中离子浓度由大到小排列第2位的离子是____ ,第4位的离子是____ 。往该溶液中加入硫酸氢钾固体并保持温度不变,则溶液中
____ (填:“增大”、“减小”或“不变”)
(5)已知:HSO3﹣⇌H++SO32﹣K=1.02×10﹣7,NH4++H2O⇌NH3•H2O+H+ K=5.65×10﹣10。往亚硫酸氢铵中加入一定量的氢氧化钡溶液,可能发生的反应离子方程式是____ (选填编号)
a.HSO3﹣+Ba2++OH﹣=BaSO3↓+H2O
b.NH4++2HSO3﹣+2Ba2++3OH﹣=2BaSO3↓+2H2O+NH3•H2O
c.NH4++HSO3﹣+Ba2++2OH﹣=BaSO3↓+H2O+NH3•H2O
d.2NH4++4HSO3﹣+3Ba2++6OH﹣=3BaSO3↓+4H2O+2NH3•H2O+SO32﹣
(1)写出工业上以硫磺为原料生产硫酸的第一步反应方程式
(2)工业上用过硫酸钾(K2S2O8)测定钢铁中的锰含量,主要反应如下:
(3)用电解硫酸氢钾的方法制取过硫酸钾:HSO4﹣在
(4)已知硫酸的第二级电离并不完全:HSO4﹣
 H++SO42﹣(Ki=1.2×10﹣2);在0.1mol/L的硫酸氢钾溶液中大约有30%的HSO4﹣电离,则该溶液中离子浓度由大到小排列第2位的离子是
H++SO42﹣(Ki=1.2×10﹣2);在0.1mol/L的硫酸氢钾溶液中大约有30%的HSO4﹣电离,则该溶液中离子浓度由大到小排列第2位的离子是
(5)已知:HSO3﹣⇌H++SO32﹣K=1.02×10﹣7,NH4++H2O⇌NH3•H2O+H+ K=5.65×10﹣10。往亚硫酸氢铵中加入一定量的氢氧化钡溶液,可能发生的反应离子方程式是
a.HSO3﹣+Ba2++OH﹣=BaSO3↓+H2O
b.NH4++2HSO3﹣+2Ba2++3OH﹣=2BaSO3↓+2H2O+NH3•H2O
c.NH4++HSO3﹣+Ba2++2OH﹣=BaSO3↓+H2O+NH3•H2O
d.2NH4++4HSO3﹣+3Ba2++6OH﹣=3BaSO3↓+4H2O+2NH3•H2O+SO32﹣
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)配平下列方程式
①___ FeCl3 +___ KI===____ FeCl2+____ KCl+_____ I2
②____ ClO-+_____ Fe(OH)3+_____ OH-===_____ Cl-+____ FeO +
+____ H2O
(2)用浓硫酸配制稀硫酸的过程中,下列操作会使配制的稀硫酸溶液浓度偏高的是___ (填序号)。
①量取浓硫酸的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③溶解后未经冷却就移液并定容
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
①
②
 +
+(2)用浓硫酸配制稀硫酸的过程中,下列操作会使配制的稀硫酸溶液浓度偏高的是
①量取浓硫酸的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③溶解后未经冷却就移液并定容
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】根据提供的情境书写指定反应的方程式
(1)轻质碳酸镁是广泛应用于橡胶、塑料、食品和医药工业的化工产品,以卤块(主要成分为MgCl2,含Fe2+、Fe3+、Mn2+等杂质离子)为原料制备轻质碳酸镁的工艺流程如图:
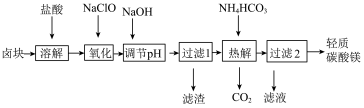
①“氧化”一步中发生反应的离子方程式为___ 。
②轻质碳酸镁的成分为碱式碳酸镁[MgCO3·Mg(OH)2·3H2O],则“热解”一步发生反应的离子方程式为___ 。
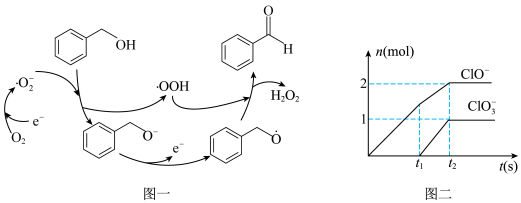
(2)双氧水是重要的化学试剂,一定条件下,O2得电子转化为超氧自由基(·O2-),并实现如图一所示的转化:写出图示转化总反应的化学方程式:___ 。
(3)在一定量的石灰乳中通入一定量的Cl2,二者恰好完全反应(反应均放热)。生成物中含Cl-、ClO-、ClO 三种含氯元素的离子,其中ClO-、ClO
三种含氯元素的离子,其中ClO-、ClO 两种离子的物质的量(n)与反应时间(t)的曲线如图二所示。t2时,Ca(OH)2与Cl2发生反应的总化学方程式为:
两种离子的物质的量(n)与反应时间(t)的曲线如图二所示。t2时,Ca(OH)2与Cl2发生反应的总化学方程式为:___ 。
(1)轻质碳酸镁是广泛应用于橡胶、塑料、食品和医药工业的化工产品,以卤块(主要成分为MgCl2,含Fe2+、Fe3+、Mn2+等杂质离子)为原料制备轻质碳酸镁的工艺流程如图:

①“氧化”一步中发生反应的离子方程式为
②轻质碳酸镁的成分为碱式碳酸镁[MgCO3·Mg(OH)2·3H2O],则“热解”一步发生反应的离子方程式为
(2)双氧水是重要的化学试剂,一定条件下,O2得电子转化为超氧自由基(·O2-),并实现如图一所示的转化:写出图示转化总反应的化学方程式:
(3)在一定量的石灰乳中通入一定量的Cl2,二者恰好完全反应(反应均放热)。生成物中含Cl-、ClO-、ClO
 三种含氯元素的离子,其中ClO-、ClO
三种含氯元素的离子,其中ClO-、ClO 两种离子的物质的量(n)与反应时间(t)的曲线如图二所示。t2时,Ca(OH)2与Cl2发生反应的总化学方程式为:
两种离子的物质的量(n)与反应时间(t)的曲线如图二所示。t2时,Ca(OH)2与Cl2发生反应的总化学方程式为:
您最近一年使用:0次
【推荐1】根据所学知识回答下列问题:
(1)在一定条件下,实现以下物质间转化,下列说法错误的是________
Ca CaO
CaO Ca(OH)2
Ca(OH)2 CaCO3
CaCO3 Ca(HCO3)2
Ca(HCO3)2
(2)在S2-、Fe2+、Cu2+、Na+中,既有氧化性又有还原性的是___________ 。
(3)某同学写出以下三个化学方程式(未配平)。
① NO + HNO3→ N2O3 + H2O
②N2O4 + H2O → HNO3 + HNO2
③ NH3 + NO → HNO2 + H2O
其中你认为一定不能实现的是___________ (填序号)。
(4)根据反应Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
①氧化剂是___________ (填化学式)。
②该反应中硝酸的作用是___________ (填字母)。
A.氧化剂 B.还原剂 C.酸性作用
③上述反应的离子方程式为___________ 。
④参加反应的HNO3与作为氧化剂的HNO3的个数之比为___________ 。
⑤配平反应________
___________ I2 + ___________ H2O +___________Cl2=___________ HIO3 + ___________ HCl
(1)在一定条件下,实现以下物质间转化,下列说法错误的是________
Ca
 CaO
CaO Ca(OH)2
Ca(OH)2 CaCO3
CaCO3 Ca(HCO3)2
Ca(HCO3)2| A.实现反应③只能向澄清石灰水中通入CO2气体 |
| B.反应①是氧化还原反应 |
| C.Ca→CaO的反应发生了化合反应 |
| D.CaCO3属于盐类物质,但是Ca(HCO3)2不属于盐类物质 |
(3)某同学写出以下三个化学方程式(未配平)。
① NO + HNO3→ N2O3 + H2O
②N2O4 + H2O → HNO3 + HNO2
③ NH3 + NO → HNO2 + H2O
其中你认为一定不能实现的是
(4)根据反应Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
①氧化剂是
②该反应中硝酸的作用是
A.氧化剂 B.还原剂 C.酸性作用
③上述反应的离子方程式为
④参加反应的HNO3与作为氧化剂的HNO3的个数之比为
⑤配平反应
___________ I2 + ___________ H2O +___________Cl2=___________ HIO3 + ___________ HCl
您最近一年使用:0次
【推荐2】氧化还原反应是一类重要的反应,请按要求完成下列题目。
(1)对反应2FeCl3+2KI═2FeCl2+2KCl+I2作分析,并用双线桥法标出电子转移的方向和数目:___ 。该反应中,__ 是还原剂,___ 是还原产物,被还原的物质是___ 。
(2)在一定条件下,反应2NH3+3CuO 3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是
3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是__ (填序号)。
A.该反应是置换反应
B.反应中NH3被氧化为N2
C.在反应中体现了金属铜的还原性
D.在反应中每生成1molH2O转移1mol电子
(3)在反应H2SO3+2H2S=3H2O+3S↓中被氧化的元素与被还原的元素的质量比为___ 。
(1)对反应2FeCl3+2KI═2FeCl2+2KCl+I2作分析,并用双线桥法标出电子转移的方向和数目:
(2)在一定条件下,反应2NH3+3CuO
 3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是
3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是A.该反应是置换反应
B.反应中NH3被氧化为N2
C.在反应中体现了金属铜的还原性
D.在反应中每生成1molH2O转移1mol电子
(3)在反应H2SO3+2H2S=3H2O+3S↓中被氧化的元素与被还原的元素的质量比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求书写下列反应的方程式:
(1)往澄清石灰水中通入少量二氧化碳,请写出此反应的离子方程式:___________ 。
(2)工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,则NH3与NO2反应的化学方程式:___________ 。
(3)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液中的H+恰好完全反应,请写出发生反应的离子方程式:___________ 。
(4)①Ca(HCO3)2与少量NaOH溶液的反应的离子方程式:___________ 。
②NaOH与少量Ca(HCO3)2溶液的反应的离子方程式:___________ 。
(1)往澄清石灰水中通入少量二氧化碳,请写出此反应的离子方程式:
(2)工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,则NH3与NO2反应的化学方程式:
(3)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液中的H+恰好完全反应,请写出发生反应的离子方程式:
(4)①Ca(HCO3)2与少量NaOH溶液的反应的离子方程式:
②NaOH与少量Ca(HCO3)2溶液的反应的离子方程式:
您最近一年使用:0次



