如图是甲醛分子的模型,根据该图和所学化学知识回答下列问题:
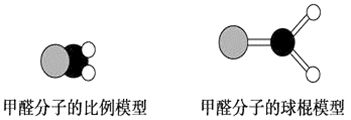
(1)甲醛分子中碳原子的杂化方式是__________ ,作出该判断的主要理由是__________________________ 。
(2)下列是对甲醛分子中碳氧键的判断,其中正确的是________ (填序号)。
①单键 ②双键 ③σ键 ④π键 ⑤σ键和π键
(3)甲醛分子中C—H键与C—H键间的夹角________ (填“=”、“>”或“<”)120°,出现该现象的主要原因是____________________________________________ 。

(1)甲醛分子中碳原子的杂化方式是
(2)下列是对甲醛分子中碳氧键的判断,其中正确的是
①单键 ②双键 ③σ键 ④π键 ⑤σ键和π键
(3)甲醛分子中C—H键与C—H键间的夹角
18-19高二上·云南红河·期中 查看更多[8]
(已下线)2.2.2 杂化轨道理论简介-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)高二选择性必修2(人教版2019)第二章 分子结构与性质 第二节综合训练鲁科版2019选择性必修2阶段性综合评估测试卷(一)(人教版2019)选择性必修2 阶段性综合评估测试卷(一)(已下线)专题11.2 分子结构与性质(练)-《2020年高考一轮复习讲练测》贵州省从江县第一民族中学2018-2019学年高二上学期期末考试化学试题云南省昭通市彝良县第一中学2018-2019学年高二上学期12月考试化学试题云南省河口县一中2018-2019学年高二上学期期中考试化学试题
更新时间:2018-12-15 07:41:48
|
相似题推荐
【推荐1】CuSCN是一种生物防腐涂料,可用CuSO4、NaSCN、Na2SO3作原料,并用乙二醇或DMF作分散剂进行制备。
(1) Cu+基态核外电子排布式为____________ 。
(2) NaSCN中元素S、C、N的第一电离能由大到小的顺序为____________ ;Na2SO3中SO32-的空间构型为____________ (用文字描述)。
(3) 乙二醇(HOCH2CH2OH)与H2O可以任意比例互溶,除因为它们都是极性分子外,还因为____________________ 。
(4) DMF(OHCNCH3CH3)分子中碳原子的轨道杂化类型为____________ ;1 mol DMF分子中含有σ键的数目为____________ 。
(1) Cu+基态核外电子排布式为
(2) NaSCN中元素S、C、N的第一电离能由大到小的顺序为
(3) 乙二醇(HOCH2CH2OH)与H2O可以任意比例互溶,除因为它们都是极性分子外,还因为
(4) DMF(OHCNCH3CH3)分子中碳原子的轨道杂化类型为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)以基态硅原子为例,如果电子排布式写作ls22s22p63s13p3则违反了_______ 原理,如写作ls22s22p63s33p1则违反了_______ 原理;
(2)已知H、C、Si三种元素的电负性依次为2.1、2.5、1.8,则CH4、SiH4中C、Si的化合价依次为_______ 、_______ ;
(3)在我们现今使用的元素周期表中,元素种类最多的族是_______ 族,共_______ 种元素;元素种类最多的周期是第_______ 周期,共_______ 种元素;
(4)熔点: F2_______ Cl2(填“<”或“=”“或>”,下同),沸点:HF_______ HCl,一定压强下HF和HCl的混合气体降温时_______ (填HF或HCl)先液化;
(5)前三周期元素中,基态原子中未成对电子数与其所在周期序数相同的元素:_______ (用元素符号按原子序数由小到大排列)。
(2)已知H、C、Si三种元素的电负性依次为2.1、2.5、1.8,则CH4、SiH4中C、Si的化合价依次为
(3)在我们现今使用的元素周期表中,元素种类最多的族是
(4)熔点: F2
(5)前三周期元素中,基态原子中未成对电子数与其所在周期序数相同的元素:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】完成下列问题。
(1)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为_______ ,下列对XeF2中心原子杂化方式推断合理的是_______ (填标号)。
A.sp B.sp2 C.sp3 D.sp3d
(2)SiCl4可发生水解反应,机理如下:

含s、p、d轨道的杂化类型有:①dsp2;②sp3d;③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为_______ (填标号)。
(1)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为
A.sp B.sp2 C.sp3 D.sp3d
(2)SiCl4可发生水解反应,机理如下:

含s、p、d轨道的杂化类型有:①dsp2;②sp3d;③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】写出(1)~(4)原子的电子排布式,用价层电子对互斥模型推测(5)~(8)分子的空间构型。
(1)Li_______________ ;(2)K _______________ ;(3)Mg ________________ ;(4)Cl ______________ ;(5)CO2_______________ ;(6)SO2______________ ;(7)NH3_________________ ;(8)CH4_______________ 。
(1)Li
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】回答下列问题
(1)在 分子中,CO
分子中,CO 的价层电子对的空间构型为
的价层电子对的空间构型为___________ ,以极性键相结合,具有正四面体结构的分子是___________ ,以极性键相结合,具有三角锥形结构的分子是___________ ,以极性键相结合,具有V形结构的分子是___________ 。
(2)元素As与N同族。预测As的氢化物分子的空间结构为___________ ,其沸点比NH3的___________ (填“高”或“低”),其判断理由是___________ 。
(1)在
 分子中,CO
分子中,CO 的价层电子对的空间构型为
的价层电子对的空间构型为(2)元素As与N同族。预测As的氢化物分子的空间结构为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】回答下列问题:
(1)常温常压下 为无色液体,
为无色液体, 空间结构为
空间结构为_______ ,其固体的晶体类型为_______ 。
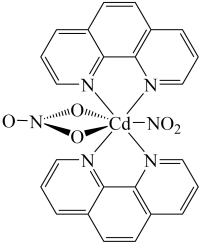
(2)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种 配合物的结构如图所示,
配合物的结构如图所示, 该配合物中通过螯合作用形成的配位键有
该配合物中通过螯合作用形成的配位键有_______  ,该螯合物中N的杂化方式有
,该螯合物中N的杂化方式有_______ 种。
(1)常温常压下
 为无色液体,
为无色液体, 空间结构为
空间结构为(2)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种
 配合物的结构如图所示,
配合物的结构如图所示, 该配合物中通过螯合作用形成的配位键有
该配合物中通过螯合作用形成的配位键有 ,该螯合物中N的杂化方式有
,该螯合物中N的杂化方式有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题
(1)用VSEPR 理论判断:
(2)基态Fe原子有___________ 个未成对电子,Fe3+的价电子排布式为___________ 。Fe在周期表中位于___________ 列。
(3)Cl的核外电子排布式为___________ 。
(4)22Ti的原子结构示意图___________ 。
(5)Sn为ⅣA族元素,单质Sn与干燥 反应生成
反应生成 。常温常压下
。常温常压下 为无色液体,
为无色液体, 空间构型为
空间构型为___________ 。
(1)用VSEPR 理论判断:
| 物质 | 孤对电子对数 | 轨道杂化方式 | 分子或离子的空间结构 |
PO | |||
| COCl2 |
(3)Cl的核外电子排布式为
(4)22Ti的原子结构示意图
(5)Sn为ⅣA族元素,单质Sn与干燥
 反应生成
反应生成 。常温常压下
。常温常压下 为无色液体,
为无色液体, 空间构型为
空间构型为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】合成氨有助于解决地球上粮食不足问题,是化学和技术对社会发展与进步的巨大贡献。
(1)基态N原子中,能量最高的电子的电子云在空间有_______ 个伸展方向,原子轨道呈_______ 形。
(2)我国科研人员研制出了“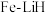 ”催化剂,使得合成氨温度和压强分别降到了350℃,
”催化剂,使得合成氨温度和压强分别降到了350℃, ,这是近年来合成氨反应研究中心的重要突破。
,这是近年来合成氨反应研究中心的重要突破。
①第三电离能
_______ 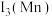 (填“>”或“<”),原因是
(填“>”或“<”),原因是_______ 。
②比较 与
与 的半径大小关系:
的半径大小关系: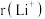
_______  (填“>”或“<”)。
(填“>”或“<”)。
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H2,将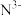 转化为NH2,反应过程如图所示:
转化为NH2,反应过程如图所示:
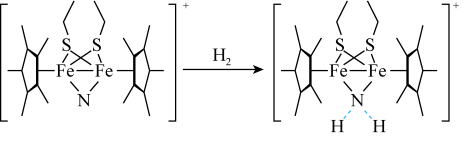
产物中 原于的杂化轨道类型为
原于的杂化轨道类型为_______ 。
(1)基态N原子中,能量最高的电子的电子云在空间有
(2)我国科研人员研制出了“
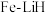 ”催化剂,使得合成氨温度和压强分别降到了350℃,
”催化剂,使得合成氨温度和压强分别降到了350℃, ,这是近年来合成氨反应研究中心的重要突破。
,这是近年来合成氨反应研究中心的重要突破。①第三电离能

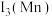 (填“>”或“<”),原因是
(填“>”或“<”),原因是②比较
 与
与 的半径大小关系:
的半径大小关系: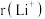
 (填“>”或“<”)。
(填“>”或“<”)。(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H2,将
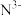 转化为NH2,反应过程如图所示:
转化为NH2,反应过程如图所示:
产物中
 原于的杂化轨道类型为
原于的杂化轨道类型为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】完成下列表格
| 粒子 | 空间结构 | 杂化类型 |
 | ||
 |
您最近一年使用:0次

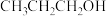 ②
② ③
③ ④
④ ⑤
⑤






