有X、Y、Z、Q、T五种元素,X原子的M层p轨道有2个未成对电子,Y原子的外围电子构型为3d64s2,Z原子的L电子层的p能级上有一空轨道,Q原子的L电子层的p能级上只有1对成对电子,T原子的M电子层上p轨道半充满。试回答下列问题:
(1)X的元素符号__________ ,Y的元素符号________ 。
(2)Z元素原子的电子排布式_______ ,Q元素原子的电子排布图__________ ,T元素原子的电子排布图_______________________________ 。
(3)Y的单质在Q的单质中燃烧的化学方程式:_________________________ 。
(1)X的元素符号
(2)Z元素原子的电子排布式
(3)Y的单质在Q的单质中燃烧的化学方程式:
更新时间:2018-12-18 07:03:23
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下图是元素周期表的一部分,针对表中的①~⑩中元素,填写下列空格:
(1)在这10种元素中,原子半径较小的是_____ (填元素符号,稀有气体除外),化学性质最不活泼的元素是__ (填“元素名称”)。
(2)元素⑧的离子结构示意图为________ ,请用电子式表示化合物④和⑧的形成过程________ 。
(3)元素⑤的单质与氢氧化钠溶液反应的化学方程式为:_______________________ 。
(4)元素⑧单质能溶于水,称为氯水,溶液黄绿色,在其中通入元素⑦的某种氧化物,溶液颜色褪去,用化学方程式表示原因_______________ 。
| ① | ⑩ | ② | ③ | ||||||||||||||
| ④ | ⑤ | ⑦ | ⑧ | ⑨ | |||||||||||||
| ⑥ | |||||||||||||||||
(1)在这10种元素中,原子半径较小的是
(2)元素⑧的离子结构示意图为
(3)元素⑤的单质与氢氧化钠溶液反应的化学方程式为:
(4)元素⑧单质能溶于水,称为氯水,溶液黄绿色,在其中通入元素⑦的某种氧化物,溶液颜色褪去,用化学方程式表示原因
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】用元素符号或化学式填空.
(1)2 个氢氧根离子_____ ;
(2)干冰_____ ;
(3)硅元素_____ ;
(4)两个五氧化二磷分子_____ .
(1)2 个氢氧根离子
(2)干冰
(3)硅元素
(4)两个五氧化二磷分子
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用_______________ 形象化描述, 基态磷原子的核外电子排布式为______________ ,有__________________ 个未成对电子, 白磷(P4)的立体构型为__________________ ,其键角为__________________ 。
(2) [Cu(NH3)4]SO4的配体为__________________ ,[Cu(H2O)4]2+中提供孤电子对的是__________________ 原子。(填元素符号)
(3)有下列六种物质:①MgCl2晶体 ②石墨 ③ SiC ④白磷(P4)晶体 ⑤金刚石 ⑥铁,其中属于离子晶体的是__________________ ,属于分子晶体的是__________________ ,属于原子晶体的化合物是__________________ 。(填序号)
(4)肼(N2H4)又称联氨,是一种可燃性液体,可用作火箭燃料。已知在25℃,101 kPa时,16.0 g N2H4在氧气中完全燃烧生成氮气和水,放出热量312 kJ,N2H4完全燃烧的热化学方程式是__________________ 。
(2) [Cu(NH3)4]SO4的配体为
(3)有下列六种物质:①MgCl2晶体 ②石墨 ③ SiC ④白磷(P4)晶体 ⑤金刚石 ⑥铁,其中属于离子晶体的是
(4)肼(N2H4)又称联氨,是一种可燃性液体,可用作火箭燃料。已知在25℃,101 kPa时,16.0 g N2H4在氧气中完全燃烧生成氮气和水,放出热量312 kJ,N2H4完全燃烧的热化学方程式是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】硫、氯、氮是三种常见的非金属元素。
完成下列填空:
(1)我们祖先的四大发明之一黑火药的爆炸反应为:S+2KNO3+3C A+N2↑+3CO2↑(已配平)。氮原子核外电子排布式为______________ ,生成物固体 A属于_____ 晶体。
(2)工业合成氨可以实现大规模固氮,氨可用于生产氯化铵、硫酸铵等化学肥料,等物质的量浓度的两溶液相同温度下pH大小为:氯化铵___________ 硫酸铵(选填>、=或<)。
(3)工业上在催化剂条件下,用NH3作为还原剂将烟气中的NO2还原成无害的氮气和水,反应方程式可表示为:8NH3(g)+6NO2(g) 7N2(g)+12H2O(g),用单线桥标出该反应电子转移的方向和数目
7N2(g)+12H2O(g),用单线桥标出该反应电子转移的方向和数目______ ,若该反应氧化产物比还原产物多0.1mol,被吸收的NO2在标准状况下的体积为_________ 。
(4)氯水成分的多样性决定了其性质的复杂性,氯气可用作自来水生产过程中的消毒剂,写出其中主要的化学反应方程式______________________________ ,在硝酸银溶液中滴加氯水,可以看到有白色沉淀产生,起作用的微粒是___________ 。
完成下列填空:
(1)我们祖先的四大发明之一黑火药的爆炸反应为:S+2KNO3+3C A+N2↑+3CO2↑(已配平)。氮原子核外电子排布式为
(2)工业合成氨可以实现大规模固氮,氨可用于生产氯化铵、硫酸铵等化学肥料,等物质的量浓度的两溶液相同温度下pH大小为:氯化铵
(3)工业上在催化剂条件下,用NH3作为还原剂将烟气中的NO2还原成无害的氮气和水,反应方程式可表示为:8NH3(g)+6NO2(g)
 7N2(g)+12H2O(g),用单线桥标出该反应电子转移的方向和数目
7N2(g)+12H2O(g),用单线桥标出该反应电子转移的方向和数目(4)氯水成分的多样性决定了其性质的复杂性,氯气可用作自来水生产过程中的消毒剂,写出其中主要的化学反应方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】依据原子结构知识回答下列问题。
(1)基态Cr原子的电子排布式是___________ 。
(2)下列有关微粒性质的排列顺序错误的是___________。
(3)下列硼原子电子排布图表示的状态中,能量最高的为___________(填选项字母)。
(4)O的基态原子核外电子空间运动状态有___________ 种,其原子半径___________  (填“大于”或“小于”)。
(填“大于”或“小于”)。
(1)基态Cr原子的电子排布式是
(2)下列有关微粒性质的排列顺序错误的是___________。
A.元素的电负性: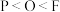 | B.元素的第一电离能: |
C.离子半径: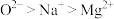 | D.原子的未成对电子数: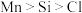 |
(3)下列硼原子电子排布图表示的状态中,能量最高的为___________(填选项字母)。
A. | B.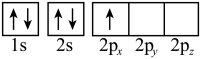 |
C.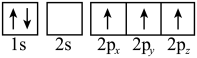 | D.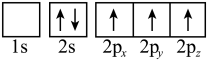 |
(4)O的基态原子核外电子空间运动状态有
 (填“大于”或“小于”)。
(填“大于”或“小于”)。
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)基态Fe原子价层电子的轨道表示式(电子排布图)为______ 。
(2) 基态核外电子排布式为
基态核外电子排布式为______ 。
(3)基态Ge原子的核外电子排布式为[Ar]______ ,有______ 个未成对电子。
(4)镍元素基态原子的电子排布式为______ ,3d能级上的未成对电子数为______ 。
(5) 基态核外电子排布式为
基态核外电子排布式为______ 。
(2)
 基态核外电子排布式为
基态核外电子排布式为(3)基态Ge原子的核外电子排布式为[Ar]
(4)镍元素基态原子的电子排布式为
(5)
 基态核外电子排布式为
基态核外电子排布式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】铁和硒(Se)都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用。回答下列问题:
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:___________ ,其价电子轨道表示式为___________ 。
②比较键角大小:气态SeO3分子___________ Se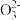 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是___________ 。
(2)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H2,将N3-转化为N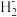 ,反应过程如图所示:
,反应过程如图所示:___________ 。
②与N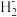 互为等电子体的一种分子为
互为等电子体的一种分子为___________ (填化学式)。
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:

②比较键角大小:气态SeO3分子
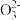 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是(2)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H2,将N3-转化为N
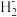 ,反应过程如图所示:
,反应过程如图所示: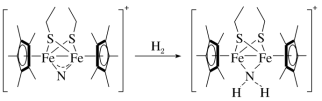
②与N
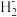 互为等电子体的一种分子为
互为等电子体的一种分子为
您最近半年使用:0次



