2012年10月29日,超强飓风“桑迪”登陆美国东海岸,给人们的生命财产造成巨大损失。灾区人们的饮水必须用漂白粉等药品消毒后才能饮用,以防止传染病发生。
(1)试用化学方程式表示工业制取漂白粉的过程______________________________ ;
(2)若用KMnO4氧化盐酸。其反应方程式如下:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,该反应中,氧化剂是____ ,1mol氧化剂在反应中_______ (填“得到”或“失去”)______ mol电子。当有1molKMnO4恰好和盐酸全部完全反应,反应后溶液的体积为2L,则所得溶液中Cl—的物质的量浓度为_______ ,此时产生的Cl2在标准状况下的体积为_______ ,被氧化的HCl的物质的量为________ 。
(1)试用化学方程式表示工业制取漂白粉的过程
(2)若用KMnO4氧化盐酸。其反应方程式如下:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,该反应中,氧化剂是
更新时间:2018-12-21 22:14:05
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】胶体金(Au)免疫层析法可用于快速检测新型冠状病毒抗体。利用柠檬酸钠溶液与氯金酸(HAuCl4)即可制备得到胶体金。研究发现:柠檬酸钠的用量不同会导致胶体金粒径和颜色的不同。
(1)柠檬酸钠的主要作用是提供___________
(2)一般的金原子直径约为0.288nm,而德国化学家席格蒙迪研制出超显微镜,观察到胶体金颗粒的形态,胶体金分散质粒子的直径大致范围在___________ nm之间。
(3)1molHAuCl4经过反应后可制备得到的胶体金胶粒的个数___________ 个。
个。
(1)柠檬酸钠的主要作用是提供___________
| A.氧化性 | B.还原性 | C.酸性 | D.碱性 |
(3)1molHAuCl4经过反应后可制备得到的胶体金胶粒的个数___________
 个。
个。| A.大于 | B.小于 | C.等于 | D.无法确定 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】按照要求回答下列问题。
(1)已知下列七种物质:①NaCl②Cu③SO2④氯化铁溶液⑤稀硫酸⑥硫酸钡⑦熔融KNO3,其中属于电解质的是____ 。
(2)工业中常将钠块加入正己烷中,除去微量的水,反应的化学方程式为____ ;若将23g钠与一定量的水发生上述反应,最终形成1L的溶液,其溶液的物质的量浓度为____ ,同时生成的气体在标准状况下的体积为____ 。
(3)利用焰色试验的原理既可制作五彩缤纷的节日烟花,也可定性鉴别某些金属盐,立德粉ZnS·BaSO4(也称锌钡白),是一种常用白色颜料。灼烧立德粉样品时,钡的焰色为____ 。
(4)工业废水中含有的重铬酸根离子(Cr2O )有毒,必须处理达标后才能排放,工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O
)有毒,必须处理达标后才能排放,工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O +14H+=6Fe3++2Cr3++7H2O。
+14H+=6Fe3++2Cr3++7H2O。
①在该反应中还原产物是____ (填离子符号);
②用单线桥标出该反应电子转移的方向和数目____ 。
(1)已知下列七种物质:①NaCl②Cu③SO2④氯化铁溶液⑤稀硫酸⑥硫酸钡⑦熔融KNO3,其中属于电解质的是
(2)工业中常将钠块加入正己烷中,除去微量的水,反应的化学方程式为
(3)利用焰色试验的原理既可制作五彩缤纷的节日烟花,也可定性鉴别某些金属盐,立德粉ZnS·BaSO4(也称锌钡白),是一种常用白色颜料。灼烧立德粉样品时,钡的焰色为
| A.黄色 | B.砖红色 | C.紫色 | D.黄绿色 |
(4)工业废水中含有的重铬酸根离子(Cr2O
 )有毒,必须处理达标后才能排放,工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O
)有毒,必须处理达标后才能排放,工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O +14H+=6Fe3++2Cr3++7H2O。
+14H+=6Fe3++2Cr3++7H2O。①在该反应中还原产物是
②用单线桥标出该反应电子转移的方向和数目
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】在工业上次磷酸 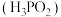 常用于化学镀银,发生的反应如下:
常用于化学镀银,发生的反应如下: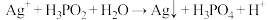 (未配平),已知
(未配平),已知 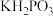 是次磷酸的正盐,请回答下列问题:
是次磷酸的正盐,请回答下列问题:
(1) 中,
中, 元素的化合价为
元素的化合价为_______ ;该反应中, 被
被_______ (填“氧化”或“还原”)。
(2)若该反应有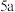 个电子转移,则镀件上银的质量为
个电子转移,则镀件上银的质量为_______  (已知每个银原子质量为
(已知每个银原子质量为 克)。
克)。
(3) 与足量
与足量  溶液反应的离子方程式:
溶液反应的离子方程式:_______ 。
(4)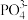 中
中 的价层电子对数为
的价层电子对数为_______ , 采取
采取_______ 杂化方式, 的空间结构为
的空间结构为_______ 。
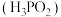 常用于化学镀银,发生的反应如下:
常用于化学镀银,发生的反应如下: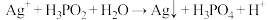 (未配平),已知
(未配平),已知 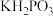 是次磷酸的正盐,请回答下列问题:
是次磷酸的正盐,请回答下列问题:(1)
 中,
中, 元素的化合价为
元素的化合价为 被
被(2)若该反应有
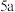 个电子转移,则镀件上银的质量为
个电子转移,则镀件上银的质量为 (已知每个银原子质量为
(已知每个银原子质量为 克)。
克)。(3)
 与足量
与足量  溶液反应的离子方程式:
溶液反应的离子方程式:(4)
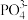 中
中 的价层电子对数为
的价层电子对数为 采取
采取 的空间结构为
的空间结构为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】按要求填空。
(1)3.01 ×1023个 CH4分子的物质的量是_______ ,在标准状况下的体积为_______ 。
(2)某物质X的质量为6.4g,含有6.02 ×1022个分子,则X的摩尔质量为_______
(3)配平方程式:_______Cu+_______HNO3=_______Cu(NO3)2+_______NO↑+_______H2O
______
(4)书写钠与水反应的离子方程式:_______
(5)在一定条件下, RO 和Cl2可发生如下反应: RO
和Cl2可发生如下反应: RO +Cl2+2OH-=RO
+Cl2+2OH-=RO +2Cl-+H2O, 由以上反应可知在上述过程中RO
+2Cl-+H2O, 由以上反应可知在上述过程中RO 被
被_______ (填“氧化”或“还原”) RO 中元素R的化合价是
中元素R的化合价是_______ 。
(1)3.01 ×1023个 CH4分子的物质的量是
(2)某物质X的质量为6.4g,含有6.02 ×1022个分子,则X的摩尔质量为
(3)配平方程式:_______Cu+_______HNO3=_______Cu(NO3)2+_______NO↑+_______H2O
(4)书写钠与水反应的离子方程式:
(5)在一定条件下, RO
 和Cl2可发生如下反应: RO
和Cl2可发生如下反应: RO +Cl2+2OH-=RO
+Cl2+2OH-=RO +2Cl-+H2O, 由以上反应可知在上述过程中RO
+2Cl-+H2O, 由以上反应可知在上述过程中RO 被
被 中元素R的化合价是
中元素R的化合价是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】Cu能与稀硝酸反应生成无色气体NO,其变化可表述为:___ Cu+______ HNO3(稀)=______ Cu(NO3)2+______ NO↑+______ H2O
(1)请配平上述化学方程式。
(2)稀硝酸在反应中显示出来的性质是__________ (填编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)产生2 mol NO,则转移的电子的物质的量为__________ mol。
(4)该反应中氧化剂与还原剂物质的量之比为____________ 。
(1)请配平上述化学方程式。
(2)稀硝酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)产生2 mol NO,则转移的电子的物质的量为
(4)该反应中氧化剂与还原剂物质的量之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】硒(Se)是人体必需的微量元素。从铜阳极泥中制备Se涉及的部分化学反应如下:
①2CuAgSe+O2+2H2SO4=Se+ Ag2Se+2CuSO4+2H2O
②SeO2 +4KI+2H2SO4=Se +2I2 +2K2SO4+2H2O
③Se+2H2SO4(浓)=2SO2 ↑+SeO2 +2H2O
④Se+4HNO3(浓)=SeO2 +4NO2↑+2H2O
⑤H2SeO3+2SO2+H2O=Se+2H2SO4
回答下列问题:
(1)反应①的离子方程式为________________ 。
(2)反应②中氧化剂与还原剂的物质的量之比为_______________ 。
(3)反应⑤中转移0.6NA电子,消耗标准状况下SO2的体积为______________ L。
(4)反应③④中等量的Se消耗H2SO4和HNO3的物质的量之比为________________ 。
(5) SeO2、H2SO4(浓) 、I2的氧化性由强到弱的顺序是________________ 。
(6)制备反应之一为5H2SeO3+2KMnO4+3H2SO4=5H2SeO4+ K2SO4+2MnSO4+3H2O,反应后,溶液中的离子浓度如下表:
则SO 的浓度为
的浓度为_______ mol/L。
①2CuAgSe+O2+2H2SO4=Se+ Ag2Se+2CuSO4+2H2O
②SeO2 +4KI+2H2SO4=Se +2I2 +2K2SO4+2H2O
③Se+2H2SO4(浓)=2SO2 ↑+SeO2 +2H2O
④Se+4HNO3(浓)=SeO2 +4NO2↑+2H2O
⑤H2SeO3+2SO2+H2O=Se+2H2SO4
回答下列问题:
(1)反应①的离子方程式为
(2)反应②中氧化剂与还原剂的物质的量之比为
(3)反应⑤中转移0.6NA电子,消耗标准状况下SO2的体积为
(4)反应③④中等量的Se消耗H2SO4和HNO3的物质的量之比为
(5) SeO2、H2SO4(浓) 、I2的氧化性由强到弱的顺序是
(6)制备反应之一为5H2SeO3+2KMnO4+3H2SO4=5H2SeO4+ K2SO4+2MnSO4+3H2O,反应后,溶液中的离子浓度如下表:
| 离子 | H+ | SeO | SO | K+ | Mn2+ |
| 浓度/(mol/L) | 0.2 | 0.15 | ? | 0.3 | 0.3 |
 的浓度为
的浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】氮在自然界中的循环如图所示。
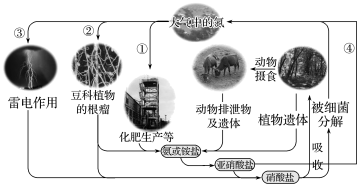
(1)过程①称为___ ,写出合成氨反应的化学方程式:___ ,该反应中氮气显____ 性(填“氧化”或“还原”,下同)。
(2)过程②中能通过____ 的作用将空气中的氮气固定下来,写出③中固氮反应的化学方程式:___ ,该反应中氮气显____ 性。
(3)过程④中的亚硝酸盐有毒,工业上若直接排放将造成对环境的污染。已知NaNO2遇到还原性较强的NH 会被还原为N2,在废液中加入下列物质不能使NaNO2无害化排放的是
会被还原为N2,在废液中加入下列物质不能使NaNO2无害化排放的是___ (填字母)。
a.H2O2 b.NH4Cl c.KNO3 d.NaOH

(1)过程①称为
(2)过程②中能通过
(3)过程④中的亚硝酸盐有毒,工业上若直接排放将造成对环境的污染。已知NaNO2遇到还原性较强的NH
 会被还原为N2,在废液中加入下列物质不能使NaNO2无害化排放的是
会被还原为N2,在废液中加入下列物质不能使NaNO2无害化排放的是a.H2O2 b.NH4Cl c.KNO3 d.NaOH
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】在氯氧化法处理含CN-的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质。
(1)某厂废水中含KCN,其浓度为650mg/L。现用氯氧化法处理,发生如下反应(其中N均为-3价):KCN+2KOH+Cl2=KOCN+2KCl+H2O,被氧化的元素是_______ 。
(2)投入过量液氯,可将氰酸盐进一步氧化为氮气。请配平下列化学方程式,并标出电子转移方向和数目_______________________________ :
KOCN+KOH+Cl2→CO2+N2+KCl+H2O
(3)若处理上述废水100L,使KCN完全转化为无毒物质,至少需液氯_______ g。
(1)某厂废水中含KCN,其浓度为650mg/L。现用氯氧化法处理,发生如下反应(其中N均为-3价):KCN+2KOH+Cl2=KOCN+2KCl+H2O,被氧化的元素是
(2)投入过量液氯,可将氰酸盐进一步氧化为氮气。请配平下列化学方程式,并标出电子转移方向和数目
KOCN+KOH+Cl2→CO2+N2+KCl+H2O
(3)若处理上述废水100L,使KCN完全转化为无毒物质,至少需液氯
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题:
(1)①Fe3O4的俗称为______ ;②HCN的电子式______ 。
(2)①工业制漂白粉的化学方程式______ 。
②Al2O3与NaOH溶液反应的离子方程式______ 。
(1)①Fe3O4的俗称为
(2)①工业制漂白粉的化学方程式
②Al2O3与NaOH溶液反应的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为___________________
(2)漂白粉的有效成分是(填化学式)_______________________ 。
(3)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式_______________________________
(4)实验室制氯气的化学方程式为____________________________ ,如果想收集到纯净干燥的Cl2,应将该混合气体依次通入盛有_____ 和________ 的洗气瓶中。
(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为
(2)漂白粉的有效成分是(填化学式)
(3)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式
(4)实验室制氯气的化学方程式为
您最近一年使用:0次