钠、铝、铁是三种重要的金属。请回答:
(1)钠元素的金属性比铝的________ (填“强”或“弱”)。
(2)将一小块金属钠投入水中,发生反应的离子方程式为______________ ;可观察到的实验现象是________ (填序号)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3)呼吸面具的原理:________________ ,_______________________ 。
(4)Fe跟Cl2在一定条件下反应,所得产物的化学式是________ 。将该产物溶于水配成溶液,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成________ 色。
b.向另一支试管中滴加NaOH溶液,现象为___________________________ ,反应的离子方程式是________________________________________________ 。
(1)钠元素的金属性比铝的
(2)将一小块金属钠投入水中,发生反应的离子方程式为
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3)呼吸面具的原理:
(4)Fe跟Cl2在一定条件下反应,所得产物的化学式是
a.若向其中一支试管中滴加KSCN溶液,则溶液变成
b.向另一支试管中滴加NaOH溶液,现象为
更新时间:2018-12-21 22:14:05
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】钠与水反应的实验过程如图①、②、③所示。

(1)将图②中的现象与解释用线连接起来。______________
(2)图③中滴加酚酞试液后,观察到的现象是______ ;
(3)钠与水反应的化学方程式是________ 。

(1)将图②中的现象与解释用线连接起来。
| 实验现象 | 解释 |
| a. 钠熔成小球 | A. 产生了气体 |
| b. 钠四处游动,嘶嘶作响 | B. 钠的密度比水小 |
| c. 钠浮在水面上 | C. 钠与水反应放热且钠的熔点低 |
(3)钠与水反应的化学方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】在探究金属钠与水反应(如图)的实验过程中,某课外小组同学记录了实验现象和实验结论:

①有碱生成 ②溶液变红 ③钠四处游动 ④钠浮在水面上 ⑤有气体产生 ⑥钠的密度比水小 ⑦钠熔成光亮的小球 ⑧反应放热,钠熔点低
(1)补齐表格(从①~⑧中选择,填序号):
(2)钠与水反应的离子方程式是_______ 。
(3)钠在空气中燃烧生成的淡黄色固体与 CO2 反应的化学方程式是_______ 。

①有碱生成 ②溶液变红 ③钠四处游动 ④钠浮在水面上 ⑤有气体产生 ⑥钠的密度比水小 ⑦钠熔成光亮的小球 ⑧反应放热,钠熔点低
(1)补齐表格(从①~⑧中选择,填序号):
| 实验现象 | | ④ | ③ | ② |
| 实验结论 | ⑧ | ⑥ | | ① |
(3)钠在空气中燃烧生成的淡黄色固体与 CO2 反应的化学方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】2011年是国际化学年,中国的宣传口号是“化学——我们的生活,我们的未来”。生活中处处有化学。钠是一种极活泼的金属,其化合物种类繁多,在生活中应用非常广泛,请回答下列问题:
(1)生理盐水的主要成分_______ (写化学式)。
(2)下列说法正确的是_______
a.将Na2O2投入紫色石蕊溶液中,溶液变蓝
b.Na2O2中阴、阳离子的个数比为1:2
c.质量相等的NaHCO3与Na2CO3分别与足量盐酸完全反应时,产生CO2的个数相等
d.将一小块钠投入装有硫酸铜溶液的试管中,试管底部有红色物质生成
e.区别NaHCO3与Na2CO3溶液,可用Ca(OH)2溶液
f.NaHCO3固体可以做干粉灭火剂,金属钠着火可以用它来灭火
g.NaHCO3粉末中混有Na2CO3杂质,可配制成溶液,然后通入过量的CO2,再降温结晶得NaHCO3固体
(3)纯碱属于_______ 类物质(填“酸”“碱”或“盐”,后同),其水溶液呈_______ 性。
(4)汽车安全气囊中气体发生剂主要成分是NaN3等物质,当汽车发生较严重的碰撞时,引发NaN3分解:2NaN3 = 2Na + 3N2↑。从氧化还原反应的角度分析该反应中Na是_______ 。
(1)生理盐水的主要成分
(2)下列说法正确的是
a.将Na2O2投入紫色石蕊溶液中,溶液变蓝
b.Na2O2中阴、阳离子的个数比为1:2
c.质量相等的NaHCO3与Na2CO3分别与足量盐酸完全反应时,产生CO2的个数相等
d.将一小块钠投入装有硫酸铜溶液的试管中,试管底部有红色物质生成
e.区别NaHCO3与Na2CO3溶液,可用Ca(OH)2溶液
f.NaHCO3固体可以做干粉灭火剂,金属钠着火可以用它来灭火
g.NaHCO3粉末中混有Na2CO3杂质,可配制成溶液,然后通入过量的CO2,再降温结晶得NaHCO3固体
(3)纯碱属于
(4)汽车安全气囊中气体发生剂主要成分是NaN3等物质,当汽车发生较严重的碰撞时,引发NaN3分解:2NaN3 = 2Na + 3N2↑。从氧化还原反应的角度分析该反应中Na是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去):

(1)若A是一种金属,C是淡黄色固体,则A的化学式为_______ B的化学式为_______ 。
(2)A→C反应的化学方程式为_______ 。
(3)A与水反应的化学方程式_______ 。
(4)C可用于呼吸面具或潜水艇中氧气的来源,写出所发生的化学方程式_______ 。从氧化剂和还原剂的角度分析,在这个反应中C的作用是_______ 。

(1)若A是一种金属,C是淡黄色固体,则A的化学式为
(2)A→C反应的化学方程式为
(3)A与水反应的化学方程式
(4)C可用于呼吸面具或潜水艇中氧气的来源,写出所发生的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】化学与生活密切相关。用方程式回答下列问题:
(1)氯气可用于饮用水的消毒,其原因是(用离子方程式)_______ 。
(2)Na2O2常用于解决潜艇的供氧问题,Na2O2降低潜艇内CO2浓度的原因是_______ 。
(3)NaHCO3可用于治疗胃酸(胃酸主要是盐酸)过多,其原因是(用离子方程式)_______ 。
(4)用双线桥标出下列反应电子转移的方向和数目_______ 。
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
并指出氧化产物与还原产物的物质的量之比是_______ 。
(1)氯气可用于饮用水的消毒,其原因是(用离子方程式)
(2)Na2O2常用于解决潜艇的供氧问题,Na2O2降低潜艇内CO2浓度的原因是
(3)NaHCO3可用于治疗胃酸(胃酸主要是盐酸)过多,其原因是(用离子方程式)
(4)用双线桥标出下列反应电子转移的方向和数目
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
并指出氧化产物与还原产物的物质的量之比是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】铝和铝合金是一类重要的金属材料。回答下列问题:
(1)除去镁粉中混有少量铝粉,应加入的试剂为___________ ,发生反应的离子方程式为___________ ,然后经过滤、洗涤、干燥。
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得 在同温同压下的体积之比是
在同温同压下的体积之比是___________ 。
(3)某同学在实验室用铝土矿(含有 和
和 ,不考虑其他杂质)制取金属铝的流程如下:
,不考虑其他杂质)制取金属铝的流程如下: 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为___________ 。
②滤液Ⅱ中溶质的用途之一是___________ 。
(1)除去镁粉中混有少量铝粉,应加入的试剂为
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得
 在同温同压下的体积之比是
在同温同压下的体积之比是(3)某同学在实验室用铝土矿(含有
 和
和 ,不考虑其他杂质)制取金属铝的流程如下:
,不考虑其他杂质)制取金属铝的流程如下: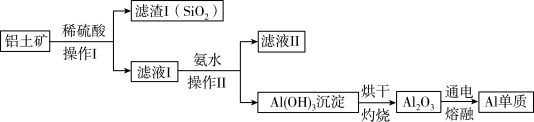
 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为②滤液Ⅱ中溶质的用途之一是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】请按要求回答下列问题:
(1)盛放烧碱液的试剂瓶不能用玻璃塞,是为了防止发生_______________________________ 反应(用化学方程式表示),而使瓶塞与瓶口粘在一起;
(2)铝热反应在工业生产中的重要用途之一是_____________________ ;
(3)“ 硅材料”又被称为信息材料。其中广泛用于光导纤维的材料是______________ (填化学式,下同);广泛用于制造集成电路的材料是________________ ;
(1)盛放烧碱液的试剂瓶不能用玻璃塞,是为了防止发生
(2)铝热反应在工业生产中的重要用途之一是
(3)“ 硅材料”又被称为信息材料。其中广泛用于光导纤维的材料是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】下表中有三组物质,每组均有甲、乙、丙三种物质(酸、碱、盐均为溶液)。
(1)第二组中________ (填化学式,下同)与第一组中所有物质都不反应,但与第三组中所有物质都能反应。
(2)第三组中有一种物质能与第一组中的所有物质反应,这种物质是________ 。
| 第一组 | 第二组 | 第三组 | |
| 甲 | BaCl2 | HCl | Cu(NO3)2 |
| 乙 | Fe2O3 | K2SO4 | H2SO4 |
| 丙 | Fe | NaOH | MgCl2 |
(1)第二组中
(2)第三组中有一种物质能与第一组中的所有物质反应,这种物质是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】铁及其化合物在生产和生活中起到重要的作用。请回答下列问题:
(1)下列微粒中,既有氧化性又有还原性的是_____________________ (填字母)。
A.Fe B.Fe2+ C.Fe3+
(2)维生素C可使食物中的Fe3+转化为Fe2+,在此过程中_______ 是还原剂(填“维生素C”或“Fe3+”)。
(3)向FeSO4溶液中滴加NaOH溶液时的现象是:生成的白色絮状沉淀迅速变成___________ 色,最后变成_________ 色。
(4)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”将铜箔腐蚀,反应原理_____________________________ (用离子方程式表示)。
(1)下列微粒中,既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)维生素C可使食物中的Fe3+转化为Fe2+,在此过程中
(3)向FeSO4溶液中滴加NaOH溶液时的现象是:生成的白色絮状沉淀迅速变成
(4)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”将铜箔腐蚀,反应原理
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】完成下列问题。
(1)按要求写出方程式:
①Fe2(SO4)3的电离方程式___________ 。
②用一种试剂除去BaCl2(HCl)中的杂质(括号内的物质为杂质),写出反应的离子方程式___________
③过量的二氧化碳通入澄清石灰水中的离子方程式___________ 。
(2)写出下列反应方程式。
①铁在氯气中燃烧___________ ;
②钠和水的反应___________ ;
(3)用单线桥法表示反应2H2S+SO2=3S↓+2H2O电子得失的方向和数目:___________ 。
(1)按要求写出方程式:
①Fe2(SO4)3的电离方程式
②用一种试剂除去BaCl2(HCl)中的杂质(括号内的物质为杂质),写出反应的离子方程式
③过量的二氧化碳通入澄清石灰水中的离子方程式
(2)写出下列反应方程式。
①铁在氯气中燃烧
②钠和水的反应
(3)用单线桥法表示反应2H2S+SO2=3S↓+2H2O电子得失的方向和数目:
您最近一年使用:0次

 、②
、② 固体、③
固体、③ 、④冰水混合物、⑤
、④冰水混合物、⑤ 、⑥稀硫酸、⑦
、⑥稀硫酸、⑦ 、⑧
、⑧ ,属于氧化物的有
,属于氧化物的有 与
与
 与
与 与
与
 与盐酸、
与盐酸、 与盐酸
与盐酸 溶液、
溶液、 与硫酸
与硫酸 与稀硫酸、
与稀硫酸、

