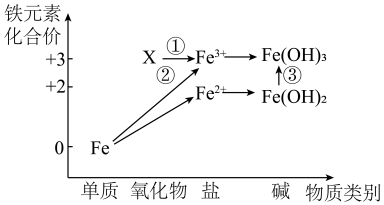
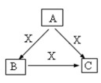
A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示。请针对以下三种不同情况回答:
(1)若A、B、C均为化合物且焰色反应均为黄色,水溶液均为碱性。则C物质的化学式是_____________ 。
(2)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,将A、C的水溶液混合可得B的白色胶状沉淀。
①A中含有的金属元素为___________ 。(写元素符号)
②该金属元素的单质与某红棕色粉末在高温下反应,可用于焊接铁轨,反应的化学反应方程式为__________ 。
若A为固态非金属单质,A与X同周期,常温常压下C为白色固体,B分子中各原子最外层均为8e-结构。C与水剧烈反应,生成两种常见酸,反应的化学方程式为_______________________ 。

(1)若A、B、C均为化合物且焰色反应均为黄色,水溶液均为碱性。则C物质的化学式是
(2)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,将A、C的水溶液混合可得B的白色胶状沉淀。
①A中含有的金属元素为
②该金属元素的单质与某红棕色粉末在高温下反应,可用于焊接铁轨,反应的化学反应方程式为
若A为固态非金属单质,A与X同周期,常温常压下C为白色固体,B分子中各原子最外层均为8e-结构。C与水剧烈反应,生成两种常见酸,反应的化学方程式为
更新时间:2018-12-24 11:11:18
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】甲是一种可用于净水的盐,由A、B、C、D、E五种短周期元素组成。甲溶于水后可电离出三种离子,其中一种是由A、B形成的五核10电子阳离子。A元素原子的核内质子数比E的少1,D、E位于同主族。用甲进行如下实验:
①取少量甲的固体溶于蒸馏水配成溶液。
②取少量甲溶液于试管中,向其中加入稀盐酸,再加入 BaCl2溶液, 出现白色沉淀。
③另取少量甲溶液于试管中,逐滴滴入NaOH 溶液,生成沉淀的质量与滴入NaOH 溶液的体积的关系如图所示。
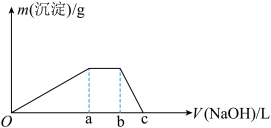
④取少量甲溶液于试管中,加入过量 NaOH 溶液并加热。回答下列问题:
(1)C的元素符号是__________ ,D在元素周期表中位于___________ 。
(2)经测定甲固体的摩尔质量为453 g/mol,其中阳离子和阴离子的物质的量之比为1∶1,则甲的化学式为____________________ 。
(3)实验③中根据图像得V(oa)∶V(ab)∶V(bc)=______________ 。
(4)实验④中发生反应的离子方程式是________________________________ 。
①取少量甲的固体溶于蒸馏水配成溶液。
②取少量甲溶液于试管中,向其中加入稀盐酸,再加入 BaCl2溶液, 出现白色沉淀。
③另取少量甲溶液于试管中,逐滴滴入NaOH 溶液,生成沉淀的质量与滴入NaOH 溶液的体积的关系如图所示。

④取少量甲溶液于试管中,加入过量 NaOH 溶液并加热。回答下列问题:
(1)C的元素符号是
(2)经测定甲固体的摩尔质量为453 g/mol,其中阳离子和阴离子的物质的量之比为1∶1,则甲的化学式为
(3)实验③中根据图像得V(oa)∶V(ab)∶V(bc)=
(4)实验④中发生反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】短周期元素的单质X、Y、Z在通常状况下均为气态,并有如图转化关系(反应条件略去):

已知:a.常见双原子单质分子中,X分子含共价键最多。b.甲分子中含10个电子,乙分子含有18个电子。
(1)X的电子式是_______ 。
(2)实验室可用如图所示装置(缺少收集装置,夹持固定装置略去)制备并收集甲。

①在图中方框内绘出用烧瓶收集甲的仪器装置简图_______ 。
②试管中的试剂是_______ (填写化学式)。
③烧杯中溶液由无色变为红色,其原因是_______ (用电离方程式表示)
(3)磷在Z中燃烧可生成两种产物,其中一种产物丁分子中各原子最外层不全是8电子结构,丁的化学式是_______ 。
(4)单质Z与过量的共价化合物甲反应有白烟生成,写出反应的化学方程式:_______ 。
(5)n mol丁与n mol丙在一定条件下反应,生成4n mol乙和另一化合物,该化合物蒸气的密度是相同状况下氢气的174倍,其化学式是_______ 。

已知:a.常见双原子单质分子中,X分子含共价键最多。b.甲分子中含10个电子,乙分子含有18个电子。
(1)X的电子式是
(2)实验室可用如图所示装置(缺少收集装置,夹持固定装置略去)制备并收集甲。

①在图中方框内绘出用烧瓶收集甲的仪器装置简图
②试管中的试剂是
③烧杯中溶液由无色变为红色,其原因是
(3)磷在Z中燃烧可生成两种产物,其中一种产物丁分子中各原子最外层不全是8电子结构,丁的化学式是
(4)单质Z与过量的共价化合物甲反应有白烟生成,写出反应的化学方程式:
(5)n mol丁与n mol丙在一定条件下反应,生成4n mol乙和另一化合物,该化合物蒸气的密度是相同状况下氢气的174倍,其化学式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】“套管实验”是将一支较小的试管装入另一试管中,经组装来完成原来需要两只或更多试管进行的实验。因其有许多优点,近年来被广泛开发并应用于化学实验中。下面这个实验为“套管实验”,实验装置如下图,小试管中部有沾上无水硫酸铜粉末的脱脂棉。请观察实验装置,分析实验原理,并回答下列问题:

(1)整个实验过程中,能观察到的现象为
①烧杯A中________ ;②小试管中________ ;
③烧杯B中____________________________ ;
(2)实验结束时,在操作上要特别注意的问题是
____________________________________________________________________
(3)写出实验过程中发生反应的化学方程式____________________________

(1)整个实验过程中,能观察到的现象为
①烧杯A中
③烧杯B中
(2)实验结束时,在操作上要特别注意的问题是
(3)写出实验过程中发生反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】I.在常温下,某兴趣小组模拟“侯氏制碱法”制取碳酸钠,流程如下:

在常温下,有关物质的溶解度为:
(1)纯碱样品中阳离子的焰色是:_______ 。操作Ⅲ中的实验操作名称为:_______ 。操作I和II_______ (“能”或“不能”)颠倒。
(2)操作I和操作II总反应的化学方程式为_______ 。
II.制得的纯碱( )中常含有少置氯化钠。某化学兴趣小组的同学拟测定某纯碱样品中
)中常含有少置氯化钠。某化学兴趣小组的同学拟测定某纯碱样品中 的质量分数。
的质量分数。

(3)确定 溶液是否过量的方法是:向溶液M中滴加
溶液是否过量的方法是:向溶液M中滴加 溶液,如果
溶液,如果_______ (填“有”或“无”)沉淀,则过量。
(4)若沉淀A没有洗涤烘干,导致 的质量分数
的质量分数_______ (填“偏大”、“偏小”或“不变”)。

在常温下,有关物质的溶解度为:
| 物质 |  |  |  | NaCl |
| 溶解度/g | 37.2 | 9.6 | 21.5 | 36.0 |
(1)纯碱样品中阳离子的焰色是:
(2)操作I和操作II总反应的化学方程式为
II.制得的纯碱(
 )中常含有少置氯化钠。某化学兴趣小组的同学拟测定某纯碱样品中
)中常含有少置氯化钠。某化学兴趣小组的同学拟测定某纯碱样品中 的质量分数。
的质量分数。
(3)确定
 溶液是否过量的方法是:向溶液M中滴加
溶液是否过量的方法是:向溶液M中滴加 溶液,如果
溶液,如果(4)若沉淀A没有洗涤烘干,导致
 的质量分数
的质量分数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】现有含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如图所示的实验装置,通过测量反应产生的CO2和H2O的质量,来确定该混合物中各组分的质量分数。
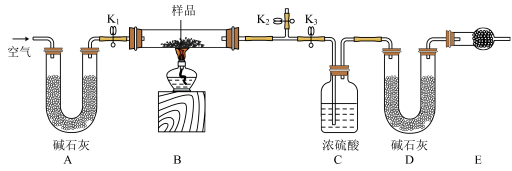
(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是___________ 。
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟,其目的是___________ 。
④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体。装置B中NaHCO3发生反应的化学方程式为___________ 。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是___________ 。
②E处干燥管中盛放的药品是___________ ,其作用是___________ ,如果实验中没有该装置,则会导致测得的NaHCO3的质量___________ (填“偏大”“偏小”或“无影响”)。

(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟,其目的是
④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体。装置B中NaHCO3发生反应的化学方程式为
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是
②E处干燥管中盛放的药品是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D均为中学化学中常见的物质,它们之间的转化关系如下图(部分产物已略去):

试回答:
(1)若D是金属,C溶液在储存时应加入少量D;D在潮湿的空气中易被腐蚀,写出常见腐蚀形式的正极反应式:_______ 。
(2)若A、B、C为含同一种金属元素的无机物,在溶液中A和C反应生成B,请写出在溶液中A和C反应生成B可能的离子方程式(写出两个即可):_______ 、_______ 。

试回答:
(1)若D是金属,C溶液在储存时应加入少量D;D在潮湿的空气中易被腐蚀,写出常见腐蚀形式的正极反应式:
(2)若A、B、C为含同一种金属元素的无机物,在溶液中A和C反应生成B,请写出在溶液中A和C反应生成B可能的离子方程式(写出两个即可):
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下图为各单质与化合物之间的转化关系,单质及化合物的组成元素均为常见的短周期元素。请回答:

(1)若沉淀丁不溶于过量的盐酸,单质A为_______ 。若沉淀丁能溶于过量的盐酸,化合物甲为_______ 。
(2)单质B的化学式为_______ ,丙的电子式为_______ 。
(3)若沉淀丁不溶于过量的盐酸,写出A和NaOH溶液反应的化学方程式:_______ 。
(4)KMnO4是重要的氧化剂,在双氧水中滴加少量用稀硫酸酸化的KMnO4溶液,溶液迅速变为无色,同时生成单质B。写出该反应的离子方程式_______ 。
(5)单质B的同素异体与Na2FeO4同是良好的消毒剂,在新冠疫情防控中作用巨大。在碱性条件下,利用NaClO氧化硝酸铁,制得Na2FeO4,该反应的离子反应方程式为_______ 。

(1)若沉淀丁不溶于过量的盐酸,单质A为
(2)单质B的化学式为
(3)若沉淀丁不溶于过量的盐酸,写出A和NaOH溶液反应的化学方程式:
(4)KMnO4是重要的氧化剂,在双氧水中滴加少量用稀硫酸酸化的KMnO4溶液,溶液迅速变为无色,同时生成单质B。写出该反应的离子方程式
(5)单质B的同素异体与Na2FeO4同是良好的消毒剂,在新冠疫情防控中作用巨大。在碱性条件下,利用NaClO氧化硝酸铁,制得Na2FeO4,该反应的离子反应方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】某化学兴趣小组用含A、B两种金属单质的粉末状混合物进行如下实验,其转化关系如下图所示(部分反应物和生成物未列出,所用试剂均足量),其中E为白色沉淀,I为红褐色沉淀。

(1)写出下列物质的化学式:F_______ ,G_______ 。
(2)D→E的转化中,加入过量X可能是_______。
(3)A→C的化学方程式为_______ 。
(4)请写出鉴别G溶液中金属阳离子的实验操作及现象_______ 。
(5)现有D和G的混合溶液,在隔绝空气的条件下,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如下图所示。试求出原粉末状混合物中A,B的物质的量之比_______ 。


(1)写出下列物质的化学式:F
(2)D→E的转化中,加入过量X可能是_______。
| A.饱和NaCl溶液 | B.NaOH溶液 | C.氨水 | D.Ba(OH)2溶液 |
(4)请写出鉴别G溶液中金属阳离子的实验操作及现象
(5)现有D和G的混合溶液,在隔绝空气的条件下,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如下图所示。试求出原粉末状混合物中A,B的物质的量之比

您最近一年使用:0次