医学上常用酸性高锰酸钾溶液和草酸溶液的反应用于测定血钙的含量回答下列问题:
(1)配平以下离子方程式,并用单线桥表示电子转移的方向和数目:
______ +_____MnO4-+_____H2C2O4=_____CO2↑+_____Mn2++____。
(2)该反应中的还原剂是______ 。
(3)反应转移了0.4mol电子,则消耗KMnO4的物质的量为______ mol。
(4)将一定质量的镁、铝合金投入100 mL一定物质的量浓度的HCl中,合金全部溶解,向所得溶液中滴加5 mol·L-1NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液体积关系如下图。
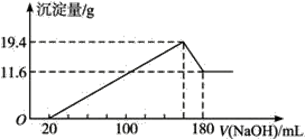
①原合金中铝的质量分数是___________ 。
②盐酸的物质的量浓度是_____________ 。
(1)配平以下离子方程式,并用单线桥表示电子转移的方向和数目:
(2)该反应中的还原剂是
(3)反应转移了0.4mol电子,则消耗KMnO4的物质的量为
(4)将一定质量的镁、铝合金投入100 mL一定物质的量浓度的HCl中,合金全部溶解,向所得溶液中滴加5 mol·L-1NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液体积关系如下图。

①原合金中铝的质量分数是
②盐酸的物质的量浓度是
更新时间:2018-12-24 09:35:04
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)含10.8gAl3+的Al2(SO4)3中所含的SO42-的物质的量是________ 。
(2)已知16g A与20g B恰好完全反应生成0.04 mol C和31.76g D,则C的摩尔质量为___________ 。
(3)0.1 mol Na中含______ mol e-,在跟足量水反应中失去________ mol e-。
(4)标准状况下V L氨气溶解在1L水中,所得溶液的密度为ρg/mL,质量分数为ω,物质的量浓度为c mol/L,则ω=_________________________ 。
(2)已知16g A与20g B恰好完全反应生成0.04 mol C和31.76g D,则C的摩尔质量为
(3)0.1 mol Na中含
(4)标准状况下V L氨气溶解在1L水中,所得溶液的密度为ρg/mL,质量分数为ω,物质的量浓度为c mol/L,则ω=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化合物(mMgO·nAl2O3·pH2O)可作环保型阻燃材料。为分析其组成,某同学进行了如下实验:称取14.900g样品,灼烧至恒重后称量,固体质量减轻了6.075g,将冷却后的固体溶入足量的NH4Cl溶液中,MgO溶解,然后过滤、洗涤、干燥、称重,得到的固体恰好能溶入150mL0.5 mol/L的氢氧化钠溶液。回答下列问题:
(1)写出该化合物作阻燃剂的一条理由:________________________ 。
(2)检验最后得到的固体洗涤干净的操作及现象是________________________ 。
(3)写出固体与氢氧化钠溶液反应的离子方程式:________________________ 。
(4)该化合物的化学式为________________________ 。
(1)写出该化合物作阻燃剂的一条理由:
(2)检验最后得到的固体洗涤干净的操作及现象是
(3)写出固体与氢氧化钠溶液反应的离子方程式:
(4)该化合物的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】车用安全气囊中含有叠氮化钠(NaN3)、硝酸钾(KNO3)、二氧化硅(SiO2)粉等。其工作原理如下:
①车辆强碰撞后,激活特定的电路,放电使NaN3迅速分解,生成Na并放出N2
②生成的Na与KNO3发生二次反应:10Na+2KNO3=K2O+5Na2O+N2↑
③SiO2与K2O、Na2O反应生成盐,消除两种碱性氧化物的腐蚀性。
(1)关于KNO3,下列分析正确的是___________。
(2)写出NaN3分解反应中氧化产物和还原产物的物质的量之比为___________ 。
(3)标出二次反应电子转移的数目和方向:___________ 。
(4)能保护司机不受伤害的气囊需要65L的N2.在2个大气压和40℃的条件下,
①65L N2是___________ 摩N2。
②得到这些N2,需要NaN3___________ 克?
(已知2个大气压和40℃气体摩尔体积约为12.84L/mol。列式计算,结果保留一位小数)
①车辆强碰撞后,激活特定的电路,放电使NaN3迅速分解,生成Na并放出N2
②生成的Na与KNO3发生二次反应:10Na+2KNO3=K2O+5Na2O+N2↑
③SiO2与K2O、Na2O反应生成盐,消除两种碱性氧化物的腐蚀性。
(1)关于KNO3,下列分析正确的是___________。
| A.KNO3电离需要通电 |
| B.KNO3是强电解质,其水溶液的导电性一定强 |
C.熔融状态的KNO3中含自由移动的K+和 |
D.固态KNO3不导电,因其中不含K+和 |
(3)标出二次反应电子转移的数目和方向:
(4)能保护司机不受伤害的气囊需要65L的N2.在2个大气压和40℃的条件下,
①65L N2是
②得到这些N2,需要NaN3
(已知2个大气压和40℃气体摩尔体积约为12.84L/mol。列式计算,结果保留一位小数)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】汽车尾气中的氮氧化物是形成酸雨、酸雾的有毒气体之一,汽车尾气中的NO主要来自N2和O2在汽车气缸内高温环境下的反应,为了减少污染需使用汽车尾气净化装置,其原理如图所示。
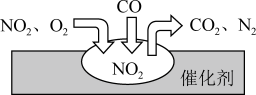
回答下列问题:
(1)净化过程中总反应的化学方程式为___________ 。其中还原剂为___________ , 被氧化的元素___________ 。
(2)选择性催化还原技术(SCR)是目前最成熟的烟气脱硝技术,原理是在金属催化下,用还原剂(如NH3)选择性与NOX反应生成N2。写出NH3还原NO2的化学方程式,并用单线桥标出电子转移的方向和数目___________ 。
(3)消除汽车尾气中的NO时,可用尿素[CO(NH2)2]还原NO2既安全又高效,且产物都是空气的成分。与SCR法相比,等物质的量的尿素与氨气可消除的NO物质的量之比为___________ (不考虑副反应)。
(4)工业制HNO3的尾气中含有NO2和NO。用NaOH溶液吸收时反应的化学方程式如下:
NO+NO2+2NaOH=2NaNO2+H2O 2NO2 + 2NaOH = NaNO2 + NaNO3 + H2O
现有平均组成为NOx的NO、NO2混合气体,通入足量NaOH溶液中,充分反应后无气体剩余,则x的取值范围为___________ 。

回答下列问题:
(1)净化过程中总反应的化学方程式为
(2)选择性催化还原技术(SCR)是目前最成熟的烟气脱硝技术,原理是在金属催化下,用还原剂(如NH3)选择性与NOX反应生成N2。写出NH3还原NO2的化学方程式,并用单线桥标出电子转移的方向和数目
(3)消除汽车尾气中的NO时,可用尿素[CO(NH2)2]还原NO2既安全又高效,且产物都是空气的成分。与SCR法相比,等物质的量的尿素与氨气可消除的NO物质的量之比为
(4)工业制HNO3的尾气中含有NO2和NO。用NaOH溶液吸收时反应的化学方程式如下:
NO+NO2+2NaOH=2NaNO2+H2O 2NO2 + 2NaOH = NaNO2 + NaNO3 + H2O
现有平均组成为NOx的NO、NO2混合气体,通入足量NaOH溶液中,充分反应后无气体剩余,则x的取值范围为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
(1)用双线桥 法分析上述反应___ (只需标出电子得失的方向和数目)。
(2)上述反应中氧化剂是___ ,氧化产物是___ 。
(3)反应中还原剂与氧化剂的物质的量之比为___ 。
(4)若反应中转移了0.3mol电子,则生成标准状况下NO的体积为___ 。
(1)用
(2)上述反应中氧化剂是
(3)反应中还原剂与氧化剂的物质的量之比为
(4)若反应中转移了0.3mol电子,则生成标准状况下NO的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):

(1)“碱浸”中NaOH的两个作用分别是_______ ;为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀,写出该反应的离子方程式:_______ 。
(2)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH,写出该反应的离子方程式:_______ 。

(1)“碱浸”中NaOH的两个作用分别是
(2)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH,写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素铬(Cr)为钢灰色金属,是自然界硬度最大的金属,可溶于水的化合物有 和
和 ,回答下列问题:
,回答下列问题:
(1)写出 溶于水电离方程式
溶于水电离方程式_______ 。
(2)水溶液中发生的化学反应: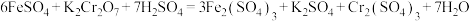 ,该反应中共有
,该反应中共有_______ 种盐,其中氧化剂是_______ ,氧化产物是_______ ,氧化剂和还原剂的物质的量之比为_______ ,用双线桥法标出该反应电子转移的方向和数目:_______ 。
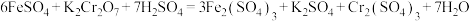
将该化学方程式改为离子方程式_______ 。
(3)铬元素的化合价有+6、+3,在下图所示步骤中,发生氧化反应的是_______ (填序号,下同),发生还原反应的是_______ ,既没发生氧化反应又没发生还原反应的是_______ 。

(4)向橙色的酸性 溶液通入足量的
溶液通入足量的 气体,溶液变为绿色的
气体,溶液变为绿色的 溶液,此反应中利用
溶液,此反应中利用 的
的_______ (填“漂白性”“酸性”“氧化性”或“还原性”)。
 和
和 ,回答下列问题:
,回答下列问题:(1)写出
 溶于水电离方程式
溶于水电离方程式(2)水溶液中发生的化学反应:
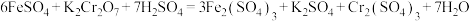 ,该反应中共有
,该反应中共有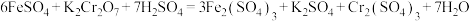
将该化学方程式改为离子方程式
(3)铬元素的化合价有+6、+3,在下图所示步骤中,发生氧化反应的是

(4)向橙色的酸性
 溶液通入足量的
溶液通入足量的 气体,溶液变为绿色的
气体,溶液变为绿色的 溶液,此反应中利用
溶液,此反应中利用 的
的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】一个氧化还原反应可以看作是由得电子和失电子的两个半反应组成。相同浓度的高锰酸钾在不同的条件下发生的半反应如下:
①MnO +5e-+8H+=Mn2+(接近无色)+4H2O
+5e-+8H+=Mn2+(接近无色)+4H2O
②MnO +3e-+2H2O=MnO2↓+4OH-
+3e-+2H2O=MnO2↓+4OH-
③MnO +e-=MnO
+e-=MnO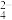 (绿色)
(绿色)
(1)从上述三个半反应中可以看出高锰酸根离子被还原的产物受溶液的___________________ 影响。
(2)将足量SO2通入高锰酸钾溶液中,观察到的实验现象是:___________________________________ ,发生还原反应的离子反应过程为_____________________ →____________________ (填离子)。
(3)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色。试判断在酸性条件下氧化性强弱:PbO2____________________ MnO (填大于、小于或等于)。
(填大于、小于或等于)。
(4)将高锰酸钾逐滴加入到硫化钾溶液中发生如下反应,其中K2SO4和S的物质的量之比为3:2。完成下列化学方程式: KMnO4+ K2S+ = K2MnO4+ K2SO4+ S↓+ 。_______________ 。
①MnO
 +5e-+8H+=Mn2+(接近无色)+4H2O
+5e-+8H+=Mn2+(接近无色)+4H2O②MnO
 +3e-+2H2O=MnO2↓+4OH-
+3e-+2H2O=MnO2↓+4OH-③MnO
 +e-=MnO
+e-=MnO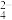 (绿色)
(绿色)(1)从上述三个半反应中可以看出高锰酸根离子被还原的产物受溶液的
(2)将足量SO2通入高锰酸钾溶液中,观察到的实验现象是:
(3)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色。试判断在酸性条件下氧化性强弱:PbO2
 (填大于、小于或等于)。
(填大于、小于或等于)。(4)将高锰酸钾逐滴加入到硫化钾溶液中发生如下反应,其中K2SO4和S的物质的量之比为3:2。完成下列化学方程式: KMnO4+ K2S+ = K2MnO4+ K2SO4+ S↓+ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】元素周期表的一部分如图,表中每一序号分别代表一种元素.回答下列问题。
(1)⑧元素的简单离子的结构示意图为________ ,⑨元素在周期表中的位置为________ 。
(2)④元素和⑤元素形成的某种化合物A可以做供氧剂,A与②元素的最高价氧化物反应的化学方程式为________________ 。
(3)⑤元素的焰色为________ 色,⑨元素最高价氧化物对应的水化物溶液与⑥元素形成的单质反应的离子方程式为________________ 。
(4)③元素、⑧元素的最简单气态氢化物接触时会有白烟产生,该白烟为________ (填化学式),加热该物质会分解产生两种气体,反应的化学方程式为________________ 。
(5)⑦元素和⑧元素中的最高价氧化物对应水化物的酸性更强的为________ (填化学式).
① | ||||||||||
② | ③ | ④ | ||||||||
⑤ | ⑥ | ⑦ | ⑧ | |||||||
⑨ | …… | |||||||||
(1)⑧元素的简单离子的结构示意图为
(2)④元素和⑤元素形成的某种化合物A可以做供氧剂,A与②元素的最高价氧化物反应的化学方程式为
(3)⑤元素的焰色为
(4)③元素、⑧元素的最简单气态氢化物接触时会有白烟产生,该白烟为
(5)⑦元素和⑧元素中的最高价氧化物对应水化物的酸性更强的为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如图:

(1)气体A中的大气污染物可选用下列试剂中的__ 吸收。
a.浓H2SO4 b.稀HNO3 c.NaOH溶液 d.氨水
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在__ (填离子符号),检验溶液中还存在Fe2+的方法是__ (注明试剂、现象)。
(3)由泡铜冶炼粗铜的化学反应方程式为__ 。
(4)利用反应2Cu+O2+2H2SO4═2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为__ 。

(1)气体A中的大气污染物可选用下列试剂中的
a.浓H2SO4 b.稀HNO3 c.NaOH溶液 d.氨水
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在
(3)由泡铜冶炼粗铜的化学反应方程式为
(4)利用反应2Cu+O2+2H2SO4═2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为
您最近一年使用:0次

 (假设HCl全部参加反应,杂质不参与反应)。
(假设HCl全部参加反应,杂质不参与反应)。

