(1)同温同压下,同体积的N2和SO2分子数之比为__________________ ,物质的量之比为____________ ,原子总数之比为____________ ,摩尔质量之比为__________ ,质量之比为________________ ,密度之比为______________ 。
(2)现有质量比为11:14的CO2和CO的混合气体,则该混合气体中的CO2和CO物质的量之比为________ ,碳原子和氧原子的个数比为________ ,该混合气体的摩尔质量为________ 。
(3)12.4gNa2X中含Na+0.4mol,则Na2X的摩尔质量是________ ,X的相对原子质量是________ 。
(4)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比是______ ,氧气的质量是_______ 。
(5)某元素的一个原子的质量为ag,一个12C原子的质量为bg,阿伏伽德罗常数为NA,则该原子的相对原子质量数值可表示为____________ 或____________ 。
(2)现有质量比为11:14的CO2和CO的混合气体,则该混合气体中的CO2和CO物质的量之比为
(3)12.4gNa2X中含Na+0.4mol,则Na2X的摩尔质量是
(4)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比是
(5)某元素的一个原子的质量为ag,一个12C原子的质量为bg,阿伏伽德罗常数为NA,则该原子的相对原子质量数值可表示为
18-19高一上·四川遂宁·阶段练习 查看更多[4]
(已下线)第三节 物质的量(一)-2020-2021学年高一化学必修第一册课时同步练(新人教)四川省成都市双流棠湖中学2019-2020学年高一下学期第一次在线月考化学试题(已下线)2019年9月1日 《每日一题》 必修1 每周一测四川省遂宁二中2018-2019学年高一上学期半期考试化学试题
更新时间:2019-01-03 10:14:07
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】已知1.28g某气体氧化物(化学式为RO2)在标准状况下的体积为448mL。
(1)该氧化物的摩尔质量为____________ 。
(2)与3.6g水含有相同数目氧原子的该气体在标准状况下的体积为_______ 。
(3)同温同压下,同体积的甲烷(CH4)和二氧化碳物质的量之比为________ 。密度之比为_____________ 。
(1)该氧化物的摩尔质量为
(2)与3.6g水含有相同数目氧原子的该气体在标准状况下的体积为
(3)同温同压下,同体积的甲烷(CH4)和二氧化碳物质的量之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)在一密闭容器中充入a mol NO和b mol O2,可发生如下反应:2NO+O2=2NO2,充分反应后容器中氮原子和氧原子的个数之比为________ 。
(2)按体积比为1:2:3所组成的N2、O2、CO2的混合气体100g,在标准状况下的总体积为_____ L。
(2)按体积比为1:2:3所组成的N2、O2、CO2的混合气体100g,在标准状况下的总体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)与16g氧气所含有分子数相同的氨气是__________ g,与16g氧气所含原子总数相同的氨气是________ g;
(2)在相同条件下,在5.6g氮气中应添加________ g氨气所组成的混合气体与16g氧气所占的体积相等。
(2)在相同条件下,在5.6g氮气中应添加
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】填空。
(1)8.4gN2与9.6g某单质Rx所含原子数相同,且分子数之比为3:2,则R的相对原子质量是_______ ,x值是_______ 。
(2)相同质量的SO2和SO3所含硫原子的个数之比为_______ 。
(3)将0.1mol·L-1的Al2(SO4)3溶液由a mL稀释至b mL,稀释后溶液中SO 的物质的量浓度是
的物质的量浓度是_______ mol·L-1。
(4)现用Zn与实验室中的盐酸反应制取6.72LH2(标准状况)。
①如果选用所贴标签为3.0mol·L-1的盐酸,至少需该盐酸_______ mL。
②该盐酸密度为1.052g·mL-1,则该盐酸溶质的质量分数是_______ (保留三位有效数字)。
(1)8.4gN2与9.6g某单质Rx所含原子数相同,且分子数之比为3:2,则R的相对原子质量是
(2)相同质量的SO2和SO3所含硫原子的个数之比为
(3)将0.1mol·L-1的Al2(SO4)3溶液由a mL稀释至b mL,稀释后溶液中SO
 的物质的量浓度是
的物质的量浓度是(4)现用Zn与实验室中的盐酸反应制取6.72LH2(标准状况)。
①如果选用所贴标签为3.0mol·L-1的盐酸,至少需该盐酸
②该盐酸密度为1.052g·mL-1,则该盐酸溶质的质量分数是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】实验室用14gFe与足量稀盐酸混合充分反应,消耗多少克氯化氢?生成FeCl2的物质的量为多少?标准状况下可以收集到多少升气体_______ ?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】24.5gH2SO4的物质的量是______ ,1.5molNa2CO3的质量是______ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)______ mol CO2中含有氧原子数跟1.806×1024个H2O分子含有的氧原子数相同。
(2)0.4 mol SiH4分子中所含原子数与_________ g HCl分子中所含原子数相等。
(3)标准状况下的甲烷和一氧化碳的混合气体8.96 L,其质量为7.60 g,则混合气体中甲烷的体积为______ 。
(4)等物质的量O2和臭氧(O3),其质量之比为_____ 。若O2和O3质量相等,则其原子数之比为______ 。
(5)200毫升含MgCl2、KCl、Na2SO4三种溶质的混合液中,已知其中含Cl-1.5 mol,K+和Na+共1.5mol,Mg2+为0.5mol,则SO42-的物质的量浓度为___________ 。
(2)0.4 mol SiH4分子中所含原子数与
(3)标准状况下的甲烷和一氧化碳的混合气体8.96 L,其质量为7.60 g,则混合气体中甲烷的体积为
(4)等物质的量O2和臭氧(O3),其质量之比为
(5)200毫升含MgCl2、KCl、Na2SO4三种溶质的混合液中,已知其中含Cl-1.5 mol,K+和Na+共1.5mol,Mg2+为0.5mol,则SO42-的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】向1L恒容密闭容器中加入12g活性炭和NO,发生反应: ∆H。在
∆H。在 下,反应进行到不同时刻测得各物质浓度的部分数据如下:
下,反应进行到不同时刻测得各物质浓度的部分数据如下:
(1)10min时,混合气体的平均摩尔质量为_______ 。
(2)T1℃时,该反应的平衡常数K=_______ 。
(3)30min后,若只改变一个条件,反应重新达到平衡时各物质的浓度如上表所示,则改变的条件可能是_______ (填字母)。
a.加入一定量的活性炭 b.改变反应体系的温度
c.缩小容器的体积 d.通入一定量的NO
(4)若30min后升高温度至 ,重新达到平衡时,容器中NO、
,重新达到平衡时,容器中NO、 、
、 的浓度之比为7:3:3,则该反应的∆H
的浓度之比为7:3:3,则该反应的∆H______ (填“<”、“=”或“>”)0
 ∆H。在
∆H。在 下,反应进行到不同时刻测得各物质浓度的部分数据如下:
下,反应进行到不同时刻测得各物质浓度的部分数据如下:
(1)10min时,混合气体的平均摩尔质量为
(2)T1℃时,该反应的平衡常数K=
(3)30min后,若只改变一个条件,反应重新达到平衡时各物质的浓度如上表所示,则改变的条件可能是
a.加入一定量的活性炭 b.改变反应体系的温度
c.缩小容器的体积 d.通入一定量的NO
(4)若30min后升高温度至
 ,重新达到平衡时,容器中NO、
,重新达到平衡时,容器中NO、 、
、 的浓度之比为7:3:3,则该反应的∆H
的浓度之比为7:3:3,则该反应的∆H
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)同温同压下的两个相同容器中分别装有O2和O3气体,则两瓶气体中分子数之比是______ ,原子数之比是______ ,质量之比是______ ,密度之比是______
(2)下列所给出的几组物质中:含有分子数最多的是_________ ;含有原子数最多的是_________ ;标准状况下体积最大的是____________ 。
① 1gH2; ② 2.408×1023个CH4 ;③ 10.8gH2O; ④ 标准状况下6.72LCO2
(3)设NA表示阿伏伽德罗常数,如果ag某气体含有的分子数是b,则cg该气体在标准状况下的体积是_________________ (用含NA的式子表示)。
(4)配制100 mL 1mol/L的的稀H2SO4溶液,需要用量筒量取质量分数为98%的浓H2SO4(密度为1.84g/cm3)的体积为______________ 。
(2)下列所给出的几组物质中:含有分子数最多的是
① 1gH2; ② 2.408×1023个CH4 ;③ 10.8gH2O; ④ 标准状况下6.72LCO2
(3)设NA表示阿伏伽德罗常数,如果ag某气体含有的分子数是b,则cg该气体在标准状况下的体积是
(4)配制100 mL 1mol/L的的稀H2SO4溶液,需要用量筒量取质量分数为98%的浓H2SO4(密度为1.84g/cm3)的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)在标准状况下,CO 和 CO2 的混合气体共 39.2 L,质量为 61 g。则两种气体的物质的量之和为_________ mol,其中 CO2 _________ mol,CO 占总体积的_________ %。
(2)0.5 mol H2SO4的质量是_________ g,含_________ 个H2SO4分子,含_________ 个氧原子,能与_________ mol NaOH 完全反应,该硫酸所含氢元素的质量与_________ g H3PO4 或_________ mol HCl 中所含氢元素的质量相同。
(3)12.8g氧气与_________ L(标准状况)的CO气体所含氧原子数相同,与_________ mol SO2所含的分子数相同。
(4)2 mol SO3和3 mol SO2其原子数之比为_________ ;相同状况下(均为气体)体积之比为_________ ;氧原子数之比为_________ 。
(1)在标准状况下,CO 和 CO2 的混合气体共 39.2 L,质量为 61 g。则两种气体的物质的量之和为
(2)0.5 mol H2SO4的质量是
(3)12.8g氧气与
(4)2 mol SO3和3 mol SO2其原子数之比为
您最近一年使用:0次

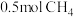 的分子个数为
的分子个数为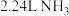 中所含的氢原子数与
中所含的氢原子数与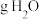 中所含的氢原子数相等。
中所含的氢原子数相等。 由二氧化碳和一氧化碳组成的混合气体,其体积为
由二氧化碳和一氧化碳组成的混合气体,其体积为 ,若将此混合气体通入足量的澄清石灰水中,则生成沉淀的质量为
,若将此混合气体通入足量的澄清石灰水中,则生成沉淀的质量为

