卤素指周期表中倒数第二列的元素,它们的化合物在生活生产中都有很重要的作用.氯化钾是临床常用的电解质平衡调节药,广泛用于临床各科,也常用于无机工业,是制造各种钾盐或碱如氢氧化钾、硫酸钾、硝酸钾、氯酸钾、红矾钾等的基本原料.
Ⅰ.老卤中主要含KCl和少量MgCl2、CaCl2、MgSO4等,需要分离提纯得到KCl.现有几种试剂:①盐酸;②K2CO3;③Na2CO3;④NaOH;⑤KOH;⑥Ba(OH)2;⑦BaCl2;⑧Ba(NO3)2 .
(1)为有效除去老卤中的杂质,加入试剂的合理顺序为_________ .
A.先加NaOH,后加Na2CO3,再加BaCl2
B.先加BaCl2,后加NaOH,再加Na2CO3
C.先加K2CO3,后加KOH,再加Ba(NO3)2
D.先加Ba(NO3)2,后加K2CO3,再加KOH
E.先加Ba(OH)2,后加K2CO3
(2)过滤除去沉淀后还需要加入的试剂为______ (填序号),还需要进行的实验为_____ .
A.蒸发结晶 B.降温结晶
Ⅱ.现有如下图仪器:
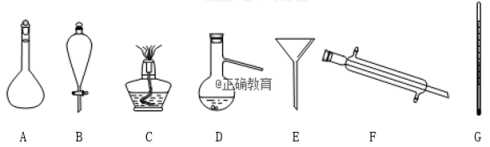
(1)仪器F的名称是_________ .
(2)在实验室组成一套蒸馏装置肯定需要所给仪器中的一部分,按照实验仪器由下到上、从左到右的顺序,这些仪器依次是____________ (填字母).
Ⅲ.小明同学将16.0 g NaOH固体溶于水配成100 mL溶液,其密度为1.60 g/mL,小明计划用配好的NaOH溶液制取简易消毒液。回答下列问题:
(1)用量筒取小明同学所配的NaOH溶液________ mL才能与标准状况下2.24 L氯气恰好完全反应.
(2)该消毒液即市面上的“84消毒液”,小明将(2)所取体积的NaOH溶液吸收好氯气后的溶液稀释到5 L使用,稀释后溶液中c(Na+)=___________
(3)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员需要520 mL 2.3 mol/L的稀硫酸,拟采用98%(密度为1.84 g/cm3)的浓硫酸进行配制.
①需取用的浓硫酸的体积为________ mL.
②取上述配好的硫酸溶液50 g与50 g 水混合,所得溶液的物质的量浓度________
A.等于1.15 mol/L B.小于2.30 mol/L 大于1.15 mol/L
C.小于1.15 mol/L D.大于2.30 mol/L
Ⅰ.老卤中主要含KCl和少量MgCl2、CaCl2、MgSO4等,需要分离提纯得到KCl.现有几种试剂:①盐酸;②K2CO3;③Na2CO3;④NaOH;⑤KOH;⑥Ba(OH)2;⑦BaCl2;⑧Ba(NO3)2 .
(1)为有效除去老卤中的杂质,加入试剂的合理顺序为
A.先加NaOH,后加Na2CO3,再加BaCl2
B.先加BaCl2,后加NaOH,再加Na2CO3
C.先加K2CO3,后加KOH,再加Ba(NO3)2
D.先加Ba(NO3)2,后加K2CO3,再加KOH
E.先加Ba(OH)2,后加K2CO3
(2)过滤除去沉淀后还需要加入的试剂为
A.蒸发结晶 B.降温结晶
Ⅱ.现有如下图仪器:

(1)仪器F的名称是
(2)在实验室组成一套蒸馏装置肯定需要所给仪器中的一部分,按照实验仪器由下到上、从左到右的顺序,这些仪器依次是
Ⅲ.小明同学将16.0 g NaOH固体溶于水配成100 mL溶液,其密度为1.60 g/mL,小明计划用配好的NaOH溶液制取简易消毒液。回答下列问题:
(1)用量筒取小明同学所配的NaOH溶液
(2)该消毒液即市面上的“84消毒液”,小明将(2)所取体积的NaOH溶液吸收好氯气后的溶液稀释到5 L使用,稀释后溶液中c(Na+)=
(3)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员需要520 mL 2.3 mol/L的稀硫酸,拟采用98%(密度为1.84 g/cm3)的浓硫酸进行配制.
①需取用的浓硫酸的体积为
②取上述配好的硫酸溶液50 g与50 g 水混合,所得溶液的物质的量浓度
A.等于1.15 mol/L B.小于2.30 mol/L 大于1.15 mol/L
C.小于1.15 mol/L D.大于2.30 mol/L
更新时间:2019-01-06 13:30:08
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】如下图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
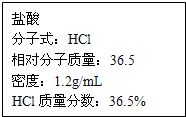
(1)该浓盐酸的物质的量浓度为___________ mol/L。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_________ 。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生现需450 mL物质的量浓度为0.3 mol/L稀盐酸。
①该学生需要量取___________ mL上述浓盐酸进行配制。
②配制时正确的操作顺序是(用字母表示)________ ;
A.用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量水(约30mL)的烧杯中, 用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1—2cm处
③在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏高”或“偏低”或“无影响”)。
I、用量筒量取浓盐酸时俯视观察凹液面____________ ;
II、用量筒量取浓盐酸后,洗涤量筒2~3次,洗涤液也转移到容量瓶_________ ;
III、溶液注入容量瓶前没有恢复到室温就进行定容____________ 。
(4)若在标准状况下,将V LHCl气体溶于1L水中,所得溶液密度为d g/mL,则此溶液的物质的量浓度为________ mol/L。(填字母)(2分)


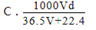
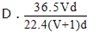
(5)现将100mL 0.5mol/L的盐酸与200mL 0.1mol/LCuCl2溶液混合,体积变化忽略不计,所得溶液中Cl-的物质的量浓度是_________________ 。

(1)该浓盐酸的物质的量浓度为
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生现需450 mL物质的量浓度为0.3 mol/L稀盐酸。
①该学生需要量取
②配制时正确的操作顺序是(用字母表示)
A.用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量水(约30mL)的烧杯中, 用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1—2cm处
③在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏高”或“偏低”或“无影响”)。
I、用量筒量取浓盐酸时俯视观察凹液面
II、用量筒量取浓盐酸后,洗涤量筒2~3次,洗涤液也转移到容量瓶
III、溶液注入容量瓶前没有恢复到室温就进行定容
(4)若在标准状况下,将V LHCl气体溶于1L水中,所得溶液密度为d g/mL,则此溶液的物质的量浓度为


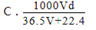
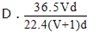
(5)现将100mL 0.5mol/L的盐酸与200mL 0.1mol/LCuCl2溶液混合,体积变化忽略不计,所得溶液中Cl-的物质的量浓度是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】I.神舟十九号载人航天飞船运载火箭用偏二甲肼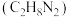 作燃料,四氧化二氮
作燃料,四氧化二氮 作推进剂,点燃后两者反应生成3种常见无污染物质。已知:常温下,
作推进剂,点燃后两者反应生成3种常见无污染物质。已知:常温下, 为无色液体,易溶于水;
为无色液体,易溶于水; 有剧毒,熔点为
有剧毒,熔点为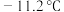 ,沸点为21.2℃,设NA为阿伏伽德罗常数的值。
,沸点为21.2℃,设NA为阿伏伽德罗常数的值。
(1)写出 和
和 发生反应的化学方程式:
发生反应的化学方程式:___________ 。
(2)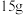
 中含有的N原子数为
中含有的N原子数为________ ,与_______ g 中含有的N原子数相同。
中含有的N原子数相同。
(3)将 a%的
a%的 水溶液跟
水溶液跟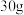 b%的
b%的 水溶液混合,得到的溶液密度为
水溶液混合,得到的溶液密度为 ,设
,设 的摩尔质量为
的摩尔质量为 ,则混合后溶液的物质的量浓度为
,则混合后溶液的物质的量浓度为___________ 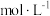 (用含字母的式子表示)。
(用含字母的式子表示)。
Ⅱ.化学工业为医疗等提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。某同学购买了一瓶“84”消毒液,部分标签如图所示。
净含量:1000 mL 密度:1.19 g·cm-3主要成分:25%NaClO
注意事项:密封保存,易吸收空气中的CO2变质,稀释100倍(体积比)后使用,回答下列问题:
(4)该同学取100 mL该“84”消毒液稀释后用于消毒(假设稀释后溶液密度为1 g·cm-3),稀释后的溶液中c(Na+)=___________ mol·L-1(保留一位有效数字)。
(5)“84”消毒液的稀溶液在浸泡餐具过程中,因吸收空气中 使消毒杀菌能力增强,产物中有小苏打,请用离子方程式说明原因:
使消毒杀菌能力增强,产物中有小苏打,请用离子方程式说明原因:___________ 。一瓶“84”消毒液最多能吸收空气中___________ L CO2(标准状况下)。
(6)该同学参阅“84”消毒液的配方,欲用NaClO固体配制480 mL 0.2 mol·L-1的消毒液。
①需要的仪器有托盘天平、烧杯、玻璃棒、量筒、______ 。
②需要用托盘天平称量的NaClO固体质量为______ g。
③下列关于容量瓶的使用操作,正确的是______ 。 反应可制得一种在生产生活中常用于漂白、消毒的物质,同时有
反应可制得一种在生产生活中常用于漂白、消毒的物质,同时有 生成,该反应的化学方程式是
生成,该反应的化学方程式是________ 。
(8)下列操作可能导致所配溶液浓度偏低的是______ (填字母)。
A.移液时,未洗涤烧杯和玻璃棒B.溶解后未经冷却就移液
C.移液时,有少量液体溅出D.定容时,俯视刻度线
E.容量瓶用蒸馏水洗净后,没烘干就直接使用
(9)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。NaClO的有效氯含量为______ (计算结果保留两位小数)。
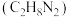 作燃料,四氧化二氮
作燃料,四氧化二氮 作推进剂,点燃后两者反应生成3种常见无污染物质。已知:常温下,
作推进剂,点燃后两者反应生成3种常见无污染物质。已知:常温下, 为无色液体,易溶于水;
为无色液体,易溶于水; 有剧毒,熔点为
有剧毒,熔点为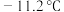 ,沸点为21.2℃,设NA为阿伏伽德罗常数的值。
,沸点为21.2℃,设NA为阿伏伽德罗常数的值。(1)写出
 和
和 发生反应的化学方程式:
发生反应的化学方程式:(2)
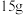
 中含有的N原子数为
中含有的N原子数为 中含有的N原子数相同。
中含有的N原子数相同。(3)将
 a%的
a%的 水溶液跟
水溶液跟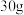 b%的
b%的 水溶液混合,得到的溶液密度为
水溶液混合,得到的溶液密度为 ,设
,设 的摩尔质量为
的摩尔质量为 ,则混合后溶液的物质的量浓度为
,则混合后溶液的物质的量浓度为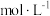 (用含字母的式子表示)。
(用含字母的式子表示)。Ⅱ.化学工业为医疗等提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。某同学购买了一瓶“84”消毒液,部分标签如图所示。
净含量:1000 mL 密度:1.19 g·cm-3主要成分:25%NaClO
注意事项:密封保存,易吸收空气中的CO2变质,稀释100倍(体积比)后使用,回答下列问题:
(4)该同学取100 mL该“84”消毒液稀释后用于消毒(假设稀释后溶液密度为1 g·cm-3),稀释后的溶液中c(Na+)=
(5)“84”消毒液的稀溶液在浸泡餐具过程中,因吸收空气中
 使消毒杀菌能力增强,产物中有小苏打,请用离子方程式说明原因:
使消毒杀菌能力增强,产物中有小苏打,请用离子方程式说明原因:(6)该同学参阅“84”消毒液的配方,欲用NaClO固体配制480 mL 0.2 mol·L-1的消毒液。
①需要的仪器有托盘天平、烧杯、玻璃棒、量筒、
②需要用托盘天平称量的NaClO固体质量为
③下列关于容量瓶的使用操作,正确的是
A.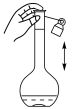 B.
B.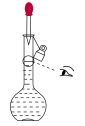 C.
C.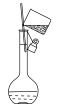 D.
D.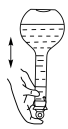
 反应可制得一种在生产生活中常用于漂白、消毒的物质,同时有
反应可制得一种在生产生活中常用于漂白、消毒的物质,同时有 生成,该反应的化学方程式是
生成,该反应的化学方程式是(8)下列操作可能导致所配溶液浓度偏低的是
A.移液时,未洗涤烧杯和玻璃棒B.溶解后未经冷却就移液
C.移液时,有少量液体溅出D.定容时,俯视刻度线
E.容量瓶用蒸馏水洗净后,没烘干就直接使用
(9)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。NaClO的有效氯含量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
(1)该“84消毒液”的物质的量浓度约为___________ mol·L-1。(保留一位小数)
(2)取用任意体积的该盐溶液时,下列物理量中会随所取体积的多少而变化的是___________ (填字母)。
A.溶液中NaClO的摩尔质量
B.溶液的浓度
C.溶液中NaClO的物质的量
D.溶液的密度
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。回答下列问题。
①配制上述溶液需要如图所示的仪器中___________ (填仪器编号)还需要还需要玻璃仪器___________ (填仪器名称)
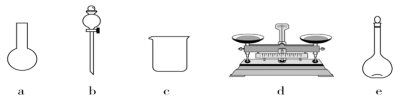
②需要称取NaClO固体的质量为___________ g
(4)若所配制的次氯酸钠溶液浓度偏小,则下列可能的原因分析中正确的是___________ 。
A.配制前,容量瓶中有少量蒸馏水B.洗涤液未转移到容量瓶中
C.未冷却,立即转移至容量瓶定容D.定容时,仰视溶液的凹液面
| 84消毒液 (有效成分)NaClO (规格)1000mL (质量分数)25% (密度)1.19g/cm3 |
(2)取用任意体积的该盐溶液时,下列物理量中会随所取体积的多少而变化的是
A.溶液中NaClO的摩尔质量
B.溶液的浓度
C.溶液中NaClO的物质的量
D.溶液的密度
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。回答下列问题。
①配制上述溶液需要如图所示的仪器中

②需要称取NaClO固体的质量为
(4)若所配制的次氯酸钠溶液浓度偏小,则下列可能的原因分析中正确的是
A.配制前,容量瓶中有少量蒸馏水B.洗涤液未转移到容量瓶中
C.未冷却,立即转移至容量瓶定容D.定容时,仰视溶液的凹液面
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验:某学生欲用18 mol/L的硫酸配制6.0 mol/L的H2SO4 1 000 mL,实验室有三种规格的容量瓶:250 mL、500 mL、1 000 mL。请回答下列问题:
(1)配制该硫酸溶液应选用容量瓶的规格为________ mL
(2)配制时,该同学的操作顺序如下,请将操作步骤A、C补充完整。
a.用量筒准确量取所需的18 mol/L的浓硫酸________ mL,沿玻璃棒倒入烧杯中,并用玻璃棒搅拌,使其混合均匀;
b.将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中;
c.___________________ ;
d.振荡,继续向容量瓶中加水,直到液面接近刻度线1 cm~2 cm处;
e.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
f.将容量瓶盖紧,振荡,摇匀。
(3)如果省略操作c,对所配溶液浓度有何影响?______ (填“偏大”、“偏小”或“无影响”)。
(4)进行操作b前还需注意__________________ 。
(1)配制该硫酸溶液应选用容量瓶的规格为
(2)配制时,该同学的操作顺序如下,请将操作步骤A、C补充完整。
a.用量筒准确量取所需的18 mol/L的浓硫酸
b.将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中;
c.
d.振荡,继续向容量瓶中加水,直到液面接近刻度线1 cm~2 cm处;
e.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
f.将容量瓶盖紧,振荡,摇匀。
(3)如果省略操作c,对所配溶液浓度有何影响?
(4)进行操作b前还需注意
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】次实验中需要0.1 mol·L-1 的CuSO4 溶液 450 mL,实验老师用蓝矾(CuSO4·5H2O)配制该浓度的溶液。请你协助老师完成下列问题:
(1)配制硫酸铜溶液时需要的主要仪器有托盘天平、烧杯、药匙、玻璃棒、胶头滴管、_______ 。
(2)该实验的第一步是计算,称取_______ g 蓝矾晶体。
(3)配制溶液时,一般可以分为以下几个主要步骤:①量取;②计算;③溶解(或稀释);④定容;⑤转移;⑥洗涤;⑦装瓶。其正确的操作顺序的第五步是_____ 。(填序号)
(4)写出下列操作对所配制的溶液浓度造成的影响(填“偏大”“偏小”或“不变”)。
①转移溶液时容量瓶内有少量的水:_______ 。
②未洗涤烧杯及玻璃棒:_______ 。
③定容摇匀后,发现液面低于刻度线,重新加水至刻度线:_______ 。
④溶液未冷却至室温就转移至容量瓶内:_______ 。
(5)取50 mL上述配制准确的硫酸铜溶液,加水稀释至100 mL,所得硫酸铜溶液的物质的量浓度为_______ mol·L-1。
(1)配制硫酸铜溶液时需要的主要仪器有托盘天平、烧杯、药匙、玻璃棒、胶头滴管、
(2)该实验的第一步是计算,称取
(3)配制溶液时,一般可以分为以下几个主要步骤:①量取;②计算;③溶解(或稀释);④定容;⑤转移;⑥洗涤;⑦装瓶。其正确的操作顺序的第五步是
(4)写出下列操作对所配制的溶液浓度造成的影响(填“偏大”“偏小”或“不变”)。
①转移溶液时容量瓶内有少量的水:
②未洗涤烧杯及玻璃棒:
③定容摇匀后,发现液面低于刻度线,重新加水至刻度线:
④溶液未冷却至室温就转移至容量瓶内:
(5)取50 mL上述配制准确的硫酸铜溶液,加水稀释至100 mL,所得硫酸铜溶液的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某学生需要用烧碱固体配制1 mol•L﹣1的NaOH溶液450 mL。请回答下列问题:
(1)计算:需要称取NaOH固体___________ g。
(2)配制时,必须使用的仪器有托盘天平(带砝码)、药匙、烧杯、玻璃棒,还缺少的仪器是_____________ 、_________________ 。(填仪器名称)
(3)实验两次用到玻璃棒,其作用分别是:先用于_______________ 、后用于___________________ 。
(4)若出现如下情况,其中将引起所配溶液浓度偏高_____________ (填字母)。
A.容量瓶实验前用蒸馏水洗干净,但未烘干 B.天平砝码生锈
C.配制过程中遗漏了洗涤步骤 D.未冷却到室温就注入容量瓶
E.加蒸馏水时不慎超过了刻度线 F.定容观察液面时俯视
(1)计算:需要称取NaOH固体
(2)配制时,必须使用的仪器有托盘天平(带砝码)、药匙、烧杯、玻璃棒,还缺少的仪器是
(3)实验两次用到玻璃棒,其作用分别是:先用于
(4)若出现如下情况,其中将引起所配溶液浓度偏高
A.容量瓶实验前用蒸馏水洗干净,但未烘干 B.天平砝码生锈
C.配制过程中遗漏了洗涤步骤 D.未冷却到室温就注入容量瓶
E.加蒸馏水时不慎超过了刻度线 F.定容观察液面时俯视
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
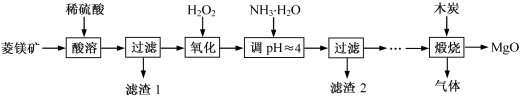
(1)MgCO3与稀硫酸反应的离子方程式为__________________________ 。
(2)加入H2O2氧化时,发生反应的离子方程式为__________________________ 。
(3)滤渣2 的成分是____________ (填化学式),过滤分离需要的玻璃仪器有 __________________ 。
(4)煅烧过程存在以下反应:
2MgSO4+C=2MgO+2SO2↑+CO2↑
MgSO4+C=MgO+SO2↑+CO↑
MgSO4+3C=MgO+S↑+3CO↑
利用图装置对煅烧产生的气体进行分步吸收或收集。
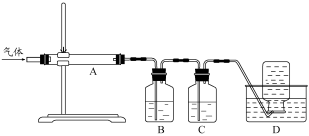
D中通过排水法收集的气体可以是___________ (填化学式)。C中溶液用于吸收CO2,B中盛放的溶液可以是___________ (填字母)。
a.NaOH 溶液 b.Na2CO3 溶液 c.稀硝酸 d.KMnO4溶液
(5)A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:______________________________ 。

(1)MgCO3与稀硫酸反应的离子方程式为
(2)加入H2O2氧化时,发生反应的离子方程式为
(3)滤渣2 的成分是
(4)煅烧过程存在以下反应:
2MgSO4+C=2MgO+2SO2↑+CO2↑
MgSO4+C=MgO+SO2↑+CO↑
MgSO4+3C=MgO+S↑+3CO↑
利用图装置对煅烧产生的气体进行分步吸收或收集。

D中通过排水法收集的气体可以是
a.NaOH 溶液 b.Na2CO3 溶液 c.稀硝酸 d.KMnO4溶液
(5)A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】海洋资源的利用具有广阔前景。
I.海带中含有丰富的碘元素。灼烧海带获取的海带灰中碘元素主要以I-形式存在。在实验室中,从海带灰中提取碘的流程如图:
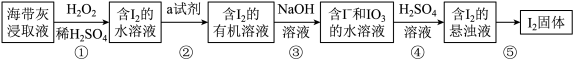
回答下列问题:
(1)实验室灼烧海带的主要仪器有酒精灯、三脚架、泥三角、玻璃棒、____ (填名称)。
(2)上述流程②主要操作步骤如图,不正确的是____ (填“甲”、“乙”或“丙”)。
甲.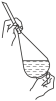 加入萃取剂后振荡
加入萃取剂后振荡
乙. 静置分层
静置分层
丙.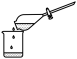 分离
分离
(3)步骤④中反应的离子方程式为____ ,在此反应中,每生成38.1gI2转移____ mol电子。
(4)上述流程中,含I2的水溶液经3步转化为含I2的悬浊液,主要目的是____ 。
II.如图是某工厂对海水资源进行综合利用的示意图。
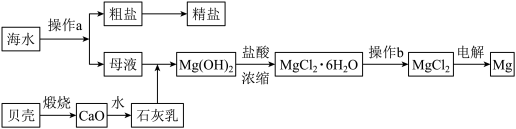
回答下列问题:
(5)流程图中操作a的名称为_____ 。(填序号)
(6)从离子反应的角度思考,往海水中加入石灰乳的作用是____ ,反应的离子方程式为____ 。
(7)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是____ 。
②操作b是在____ 氛围中进行,若在空气中加热,则会生成Mg(OH)2,写出有关反应的化学方程式:_____ 。
(8)金属镁的制备方程式为____ ,从考虑成本和废物循环利用的角度,副产物氯气可以用于____ 。
I.海带中含有丰富的碘元素。灼烧海带获取的海带灰中碘元素主要以I-形式存在。在实验室中,从海带灰中提取碘的流程如图:

回答下列问题:
(1)实验室灼烧海带的主要仪器有酒精灯、三脚架、泥三角、玻璃棒、
(2)上述流程②主要操作步骤如图,不正确的是
甲.
 加入萃取剂后振荡
加入萃取剂后振荡乙.
 静置分层
静置分层丙.
 分离
分离(3)步骤④中反应的离子方程式为
(4)上述流程中,含I2的水溶液经3步转化为含I2的悬浊液,主要目的是
II.如图是某工厂对海水资源进行综合利用的示意图。

回答下列问题:
(5)流程图中操作a的名称为
| A.蒸发结晶 | B.降温结晶 | C.过滤 | D.萃取 |
(7)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是
②操作b是在
(8)金属镁的制备方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】某合金废料经分析含有20.7%的Pb、64%的Cu和13.4%的Ag。某化学研究小组以该合金废料为原料,设计了如下工艺流程制备PbO2、Ag和CuSO4·5H2O。 回答下列问题:

(1)铅与稀HNO3发生反应的化学方程式是___________ 。
(2)氧化酸溶时Ag发生反应的离子方程式:___________ 。
(3)操作2所得滤液的成分是___________ (填化学式),要想得到CuSO4·5H2O,需要在滤液中加入足量的氢氧化钠溶液,经过滤、洗涤,在沉淀物中加入稀硫酸,经___________ 、 过滤、低温干燥得到CuSO4·5H2O。
(4)100 g合金,经过上述流程处理后得到10.05gAg和250gCuSO4·5H2O计算银的回收率是___________ ,合金废料中的铜___________ (填“是”或“不是”)全部被回收,原因是___________ 。

(1)铅与稀HNO3发生反应的化学方程式是
(2)氧化酸溶时Ag发生反应的离子方程式:
(3)操作2所得滤液的成分是
(4)100 g合金,经过上述流程处理后得到10.05gAg和250gCuSO4·5H2O计算银的回收率是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】我国科学家屠呦呦因成功从黄花蒿中提取抗疟药物青蒿素而获得2015年诺贝尔奖。从黄花蒿中提取青蒿素的流程如下:
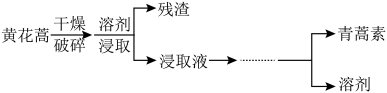
已知:青蒿素为白色针状晶体,易溶于乙醇、乙醚、苯和汽油等有机溶剂,不溶于水,熔点为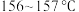 ,沸点为
,沸点为 ,热稳定性差。屠呦呦团队经历了使用不同溶剂和不同温度的探究过程,实验结果如下:
,热稳定性差。屠呦呦团队经历了使用不同溶剂和不同温度的探究过程,实验结果如下:
(1)对黄花蒿进行破碎的目的是___________ ;用水作溶剂,提取无效的原因可能是___________ 。
(2)研究发现,青蒿素分子中的某个基团对热不稳定。分析用乙醚作溶剂,提取效率高于乙醇的原因是___________ 。
(3)从青蒿(粉末)中提取青蒿素的方法以萃取原理为基础,乙醚浸提法的具体操作如下:
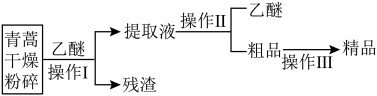
①乙醚浸提法涉及到的操作中,不会用到的装置是___________ 。
A.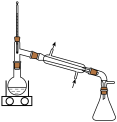 B.
B.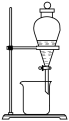 C.
C.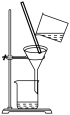 D.
D.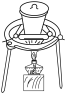
②操作Ⅲ的主要过程可能是___________ 。
A.加水溶解,蒸发浓缩、冷却结晶 B.加 的乙醇,浓缩、结晶、过滤
的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液 D.加入乙醇后,再加入苯或汽油进行萃取
(4)某科研小组通过控制其他实验条件不变,来研究原料的粒度、提取时间和提取温度对青蒿素提取速率的影响,其结果如下图所示:

由上图可知控制其他实验条件不变,采用的最佳粒度、时间和温度为___________ 。
(5)由上可知,在提取青蒿素的过程中,应充分考虑物质的___________ 等性质(写出两点即可)。

已知:青蒿素为白色针状晶体,易溶于乙醇、乙醚、苯和汽油等有机溶剂,不溶于水,熔点为
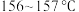 ,沸点为
,沸点为 ,热稳定性差。屠呦呦团队经历了使用不同溶剂和不同温度的探究过程,实验结果如下:
,热稳定性差。屠呦呦团队经历了使用不同溶剂和不同温度的探究过程,实验结果如下:| 溶剂 | 水 | 乙醇 | 乙醚 |
沸点/ | 100 | 78 | 35 |
| 提取效率 | 几乎为0 |  |  |
(2)研究发现,青蒿素分子中的某个基团对热不稳定。分析用乙醚作溶剂,提取效率高于乙醇的原因是
(3)从青蒿(粉末)中提取青蒿素的方法以萃取原理为基础,乙醚浸提法的具体操作如下:

①乙醚浸提法涉及到的操作中,不会用到的装置是
A.
 B.
B. C.
C. D.
D.
②操作Ⅲ的主要过程可能是
A.加水溶解,蒸发浓缩、冷却结晶 B.加
 的乙醇,浓缩、结晶、过滤
的乙醇,浓缩、结晶、过滤C.加入乙醚进行萃取分液 D.加入乙醇后,再加入苯或汽油进行萃取
(4)某科研小组通过控制其他实验条件不变,来研究原料的粒度、提取时间和提取温度对青蒿素提取速率的影响,其结果如下图所示:

由上图可知控制其他实验条件不变,采用的最佳粒度、时间和温度为
(5)由上可知,在提取青蒿素的过程中,应充分考虑物质的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】分已知某工业废水中含有大量CuSO4,少量的Ag+、Hg2+以及部分污泥,通过下述过程可从该废水中回收硫酸铜晶体及其它物质.
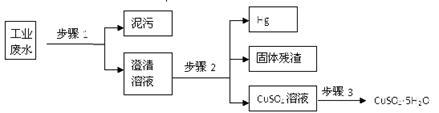
(1)步骤1的主要操作需用到的玻璃仪器除烧杯外有_____________ .
(2)步骤2中需加入某种试剂后再将混合物分离,该试剂是(填化学式)________________ ,固体残渣的成分是___________ (填化学式)
(3)步骤3中涉及的操作是:____________ 、____________ 、过滤、烘干。
(4)步骤2应该在通风橱中进行,原因是______________________

(1)步骤1的主要操作需用到的玻璃仪器除烧杯外有
(2)步骤2中需加入某种试剂后再将混合物分离,该试剂是(填化学式)
(3)步骤3中涉及的操作是:
(4)步骤2应该在通风橱中进行,原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】Ba(NO3)2可用于生产烟花。某主要生产BaCl2、BaCO3、BaSO4的化工厂利用某种钡泥[主要含有BaCO3、Ba(FeO2)2、极少量CuCO3等]制取Ba(NO3)2晶体,其部分工艺流程如下:
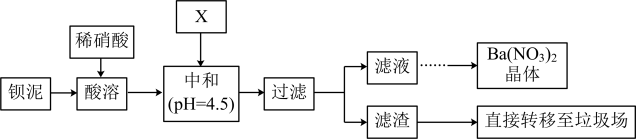
已知:Fe3+和Fe2+以氢氧化物形式沉淀完全时,溶液的pH分别为3.2和9.7。
(1)酸溶时不使用浓硝酸的原因是_______ 。
(2)酸溶后溶液中pH=1,Ba(FeO2)2与HNO3的反应化学方程式为_______ 。
(3)该厂结合本厂实际,中和选用的X为_______ (填化学式);中和使溶液中_______ (填离子符号)的浓度减少(中和引起的溶液体积变化可忽略)。
(4)滤液得到Ba(NO3)2晶体的操作依次为_______ 、_______ 、过滤。

已知:Fe3+和Fe2+以氢氧化物形式沉淀完全时,溶液的pH分别为3.2和9.7。
(1)酸溶时不使用浓硝酸的原因是
(2)酸溶后溶液中pH=1,Ba(FeO2)2与HNO3的反应化学方程式为
(3)该厂结合本厂实际,中和选用的X为
(4)滤液得到Ba(NO3)2晶体的操作依次为
您最近一年使用:0次



