氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
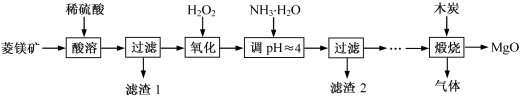
(1)MgCO3与稀硫酸反应的离子方程式为__________________________ 。
(2)加入H2O2氧化时,发生反应的离子方程式为__________________________ 。
(3)滤渣2 的成分是____________ (填化学式),过滤分离需要的玻璃仪器有 __________________ 。
(4)煅烧过程存在以下反应:
2MgSO4+C=2MgO+2SO2↑+CO2↑
MgSO4+C=MgO+SO2↑+CO↑
MgSO4+3C=MgO+S↑+3CO↑
利用图装置对煅烧产生的气体进行分步吸收或收集。
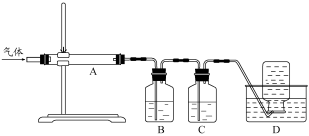
D中通过排水法收集的气体可以是___________ (填化学式)。C中溶液用于吸收CO2,B中盛放的溶液可以是___________ (填字母)。
a.NaOH 溶液 b.Na2CO3 溶液 c.稀硝酸 d.KMnO4溶液
(5)A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:______________________________ 。

(1)MgCO3与稀硫酸反应的离子方程式为
(2)加入H2O2氧化时,发生反应的离子方程式为
(3)滤渣2 的成分是
(4)煅烧过程存在以下反应:
2MgSO4+C=2MgO+2SO2↑+CO2↑
MgSO4+C=MgO+SO2↑+CO↑
MgSO4+3C=MgO+S↑+3CO↑
利用图装置对煅烧产生的气体进行分步吸收或收集。

D中通过排水法收集的气体可以是
a.NaOH 溶液 b.Na2CO3 溶液 c.稀硝酸 d.KMnO4溶液
(5)A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:
19-20高三上·甘肃庆阳·阶段练习 查看更多[2]
更新时间:2020-02-19 12:56:20
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】硫酸镁晶体(MgSO4·7H2O)是一种重要的化工原料。以菱镁矿(主要成分是MgCO3,含少量FeCO3和不溶性杂质)为原料制取硫酸镁晶体的过程如下:
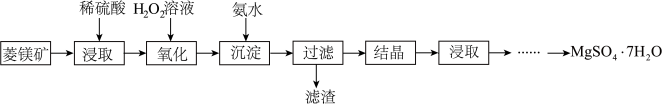
(1)MgCO3溶于稀硫酸的离子方程式是___________ 。
(2)“氧化”步骤中,加入H2O2溶液的目的是___________ (用离子方程式表示)。
(3)“沉淀”步骤中,用氨水调节溶液pH的范围是___________ 。
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(4)“过滤”所得滤液中含有的阳离子是___________ 。

(1)MgCO3溶于稀硫酸的离子方程式是
(2)“氧化”步骤中,加入H2O2溶液的目的是
(3)“沉淀”步骤中,用氨水调节溶液pH的范围是
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
阳离子 | Mg2+ | Fe2+ | Fe3+ |
开始沉淀 | 9.1 | 7.6 | 1.9 |
完全沉淀 | 11.1 | 9.7 | 3.2 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】碱式碳酸镁可用于牙膏、医药和化妆品等工业,化学式为,Mg(OH)2∙4MgCO3∙5H2O某碱式碳酸镁中含有SiO2杂质,为测定其纯度,某兴趣小组设计了如下几个方案:

方案Ⅰ
取一定质量的样品,与硫酸充分反应,通过测定生成CO2的质量计算纯度
(1)乙中发生反应的方程式为____________________________ 。
(2)仪器接口的连接顺序为(装置可以重复使用)a________ ,丁的作用是____________ 。
(3)关闭止水夹K,向样品中加入足量的稀硫酸,当样品充分反应完后,为了测定准确还应进行的操作是__________________________ 。
方案Ⅱ
①称取碱式碳酸镁样品m克;②将样品充分高温煅烧,冷却后称量;③重复操作②,测得剩余固体质量为m1克。
(4)下列仪器中,该方案不会用到的是______________________ 。

(5)判断样品完全分解的方法是_______________________ 。
(6)有同学认为方案Ⅱ高温煅烧的过程中会发生MgCO3+SiO2 MgSiO3+CO2,会导致测定结果有误,你认为这位同学的观点正确吗?
MgSiO3+CO2,会导致测定结果有误,你认为这位同学的观点正确吗?________________________ (填“正确”或“错误”)请说明自己的理由:_______________________________________________ 。
(7)求碱式碳酸镁的纯度_______________________ (用含有m,m1的式子表示)

方案Ⅰ
取一定质量的样品,与硫酸充分反应,通过测定生成CO2的质量计算纯度
(1)乙中发生反应的方程式为
(2)仪器接口的连接顺序为(装置可以重复使用)a
(3)关闭止水夹K,向样品中加入足量的稀硫酸,当样品充分反应完后,为了测定准确还应进行的操作是
方案Ⅱ
①称取碱式碳酸镁样品m克;②将样品充分高温煅烧,冷却后称量;③重复操作②,测得剩余固体质量为m1克。
(4)下列仪器中,该方案不会用到的是

(5)判断样品完全分解的方法是
(6)有同学认为方案Ⅱ高温煅烧的过程中会发生MgCO3+SiO2
 MgSiO3+CO2,会导致测定结果有误,你认为这位同学的观点正确吗?
MgSiO3+CO2,会导致测定结果有误,你认为这位同学的观点正确吗?(7)求碱式碳酸镁的纯度
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】氧化镁是优质的耐高温材料。某兴趣小组利用菱镁矿(主要成分为MgCO3,还含有少量SiO2、Al2O3等杂质)设计制备氧化镁的流程如下:

(1)步骤(Ⅰ)中分离操作的名称是_______ ,所需的玻璃仪器为_______ ;
(2)步骤(Ⅰ)分离出的滤渣中主要含有_______ ,它属于_______ (填“酸性”或“碱性”)氧化物;
(3)滤液Y中的阴离子除了含 、
、 外还有
外还有_______ ;
(4)写出步骤(Ⅲ)Mg(OH)2受热分解生成MgO和H2O的化学方程式:_______ 。

(1)步骤(Ⅰ)中分离操作的名称是
(2)步骤(Ⅰ)分离出的滤渣中主要含有
(3)滤液Y中的阴离子除了含
 、
、 外还有
外还有(4)写出步骤(Ⅲ)Mg(OH)2受热分解生成MgO和H2O的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】青花瓷胎体的原料——高岭土[Al2Si2O5(OH)x],可掺进瓷石制胎,青花瓷釉料的成分主要是钾长石(KAlSi3O8),在1300℃左右一次烧成的釉可形成精美的青花瓷。
(1)下列说法正确的是___ (填选项字母)。
(2)在“南澳一号”考古直播过程中,需用高纯度SiO2制造的光纤。如图是用海边的石英砂(含氯化钠、氧化铝等杂质)制备二氧化硅粗产品的工艺流程。

①洗涤石英砂的目的是___ 。
②在以上流程中,要将洗净的石英砂研磨成粉末,目的是___ 。
③工业上常用纯净石英砂与C在高温下发生反应制造粗硅,粗硅中含有SiC,其中Si和SiC的物质的量之比为1∶1。下列说法正确的是___ (填选项字母)。
A.SiC性质稳定,能用于制造抗高温水泥
B.制造粗硅时的反应为2SiO2+5C Si+SiC+4CO↑
Si+SiC+4CO↑
C.在以上流程中,将盐酸改为NaOH溶液,也可达到目的
D.纯净的SiO2只能用于制造光导纤维
(1)下列说法正确的是
| A.高岭土分子中x=2 |
| B.钾长石能完全溶解在盐酸中形成澄清的溶液 |
| C.烧制青花瓷过程中发生了复杂的物理变化和化学变化 |
| D.青花瓷、玻璃、水泥都属于硅酸盐产品 |

①洗涤石英砂的目的是
②在以上流程中,要将洗净的石英砂研磨成粉末,目的是
③工业上常用纯净石英砂与C在高温下发生反应制造粗硅,粗硅中含有SiC,其中Si和SiC的物质的量之比为1∶1。下列说法正确的是
A.SiC性质稳定,能用于制造抗高温水泥
B.制造粗硅时的反应为2SiO2+5C
 Si+SiC+4CO↑
Si+SiC+4CO↑C.在以上流程中,将盐酸改为NaOH溶液,也可达到目的
D.纯净的SiO2只能用于制造光导纤维
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某油脂厂废弃的油脂加氢镍催化剂主要含有NiO、Al2O3、FeO、Fe2O3,还有少量油脂。采用如下工艺流程回收其中的镍并制备硫酸镍晶体(NiSO4∙7H2O):
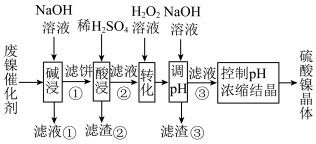
回答下列问题:
(1)写出一种可以提高“碱浸”速率的方法___________ 。
(2)“碱浸”中NaOH有两个作用,一个是溶解Al2O3,另一个是___________ 。
(3)“滤液②”中含有的金属离子是___________ 。
(4)“转化”中H2O2作用为___________ (填“氧化剂”或“还原剂”),所发生的主要反应离子方程式为___________ 。
(5)如果“转化”后的溶液中Ni2+浓度为0.01mol⋅L-1,则“调pH”应控制的pH范围是_______ 。
(6)分离出NiSO4∙7H2O晶体后的剩余母液要循环使用,其目的是___________ 。

| 金属离子 | Ni2+ | Fe3+ | Fe2+ |
| 开始沉淀时(c=0.01mol·L-1)的pH | 7.2 | 2.2 | 7.5 |
| 沉淀完全时(c=1.0×10-5mol·L-1)的pH | 8.7 | 3.2 | 9.0 |
(1)写出一种可以提高“碱浸”速率的方法
(2)“碱浸”中NaOH有两个作用,一个是溶解Al2O3,另一个是
(3)“滤液②”中含有的金属离子是
(4)“转化”中H2O2作用为
(5)如果“转化”后的溶液中Ni2+浓度为0.01mol⋅L-1,则“调pH”应控制的pH范围是
(6)分离出NiSO4∙7H2O晶体后的剩余母液要循环使用,其目的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】铝氢化钠(NaAlH4)是重要的还原剂。以铝土矿(主要成分Al2O3,含少量SiO2、Fe2O3等杂质)为原料制备NaAlH4的一种流程如图:

(1)碱浸中SiO2转化成难溶的Na2Al2Si2O8,写出生成该物质的离子方程式___ 。
(2)过滤1得滤渣的主要成分为___ ,反应1中加入NaHCO3的目的是___ 。
(3)电解2生成NaHCO3和NaOH用于循环使用,写出电解2阴极的电极反应式:___ 。
(4)反应3的化学方程式为___ 。
(5)铝氢化钠遇水发生剧烈反应产生大量气泡,其反应的化学方程式为___ 。
(6)Al与LiBH4制备的复合材料是重要制氢材料,对Al-LiBH4体系与水反应产氢的特性进行下列研究:
①如图为25℃水浴时每克不同配比的Al-LiBH4复合材料与水反应产生H2体积随时间变化关系图。由图可知,下列说法正确的是___ (填字母)。
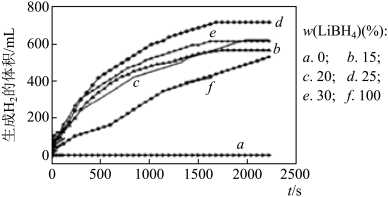
A.25℃时,纯铝与水会反应
B.25℃时,纯LiBH4与水反应产生氢气
C.25℃时,Al—LiBH4复合材料中LiBH4含量越高,1000s内产生氢气的体积越大
②如图为25℃和75℃时,Al—LiBH4复合材料[ω(LiBH4)=25%]与水反应一定时间后产物的X—射线衍射图谱(X—射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。
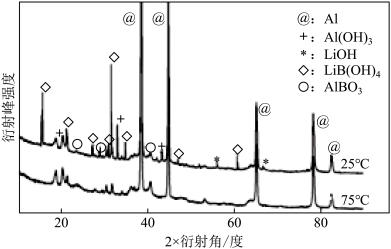
从图中分析,25℃时Al—LiBH4复合材料中与水完全反应的物质是___ (填化学式)。

(1)碱浸中SiO2转化成难溶的Na2Al2Si2O8,写出生成该物质的离子方程式
(2)过滤1得滤渣的主要成分为
(3)电解2生成NaHCO3和NaOH用于循环使用,写出电解2阴极的电极反应式:
(4)反应3的化学方程式为
(5)铝氢化钠遇水发生剧烈反应产生大量气泡,其反应的化学方程式为
(6)Al与LiBH4制备的复合材料是重要制氢材料,对Al-LiBH4体系与水反应产氢的特性进行下列研究:
①如图为25℃水浴时每克不同配比的Al-LiBH4复合材料与水反应产生H2体积随时间变化关系图。由图可知,下列说法正确的是

A.25℃时,纯铝与水会反应
B.25℃时,纯LiBH4与水反应产生氢气
C.25℃时,Al—LiBH4复合材料中LiBH4含量越高,1000s内产生氢气的体积越大
②如图为25℃和75℃时,Al—LiBH4复合材料[ω(LiBH4)=25%]与水反应一定时间后产物的X—射线衍射图谱(X—射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。

从图中分析,25℃时Al—LiBH4复合材料中与水完全反应的物质是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某学生用下图所示的装置测定镁的相对原子质量:

(1)①实验前必须对装置进行气密性检查,具体操作是:__________________ ;
(2)如果量气管的最大测量体积为50mL(假设条件为标准状况),则取金属镁条(设纯度为100%)的质量不超过______ g;(精确到0.001)
(3)实验结束,在读取数据前必须:a冷却,使温度恢复到原来状态;b_________________ ;
(4)该学生实验时称取镁条0.051g(已除去氧化膜),实验结果收集到气体48.00mL(已换算到标准状况,其他实验操作均正确),根据实验测定,镁的相对原子质量为_________ ;产生误差的原因可能是__________ (写出一点)。

(1)①实验前必须对装置进行气密性检查,具体操作是:
(2)如果量气管的最大测量体积为50mL(假设条件为标准状况),则取金属镁条(设纯度为100%)的质量不超过
(3)实验结束,在读取数据前必须:a冷却,使温度恢复到原来状态;b
(4)该学生实验时称取镁条0.051g(已除去氧化膜),实验结果收集到气体48.00mL(已换算到标准状况,其他实验操作均正确),根据实验测定,镁的相对原子质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室利用如图装置制取氧气,回答下列问题:

(1)仪器①的名称是_______ 。
(2)实验室用过氧化氢溶液和二氧化锰混合制取氧气的化学方程式为_______ 。
(3)若用B装置干燥氧气,则B中盛放的试剂为_______ (填试剂名称),若将B装置中装满水收集氧气,则气体应从导管_______ (填“a”或“b”)端通入。
(4)若直接用30%的过氧化氢溶液制取氧气,反应速率太快。为获得平稳的氧气流,图中C~F四个发生装置能达到最佳效果的是_______ (填字母)。

(1)仪器①的名称是
(2)实验室用过氧化氢溶液和二氧化锰混合制取氧气的化学方程式为
(3)若用B装置干燥氧气,则B中盛放的试剂为
(4)若直接用30%的过氧化氢溶液制取氧气,反应速率太快。为获得平稳的氧气流,图中C~F四个发生装置能达到最佳效果的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】I. 是国际公认的一种安全、低毒的绿色消毒剂。熔点为-59.5℃,沸点为11.0℃,高浓度时极易爆炸,极易溶于水,遇热水易分解。实验室可用如图所示的装置制备
是国际公认的一种安全、低毒的绿色消毒剂。熔点为-59.5℃,沸点为11.0℃,高浓度时极易爆炸,极易溶于水,遇热水易分解。实验室可用如图所示的装置制备 (装置A的酒精灯加热装置略去)。回答下列问题:
(装置A的酒精灯加热装置略去)。回答下列问题:
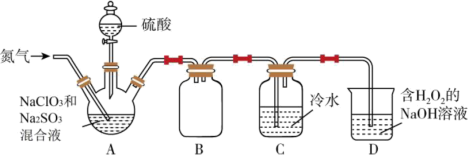
(1)下列关于ClO2分子结构和性质的说法错误的是__________ 。
A.分子中只含 键 B.分子具有极性 C.分子的空间结构为V形
键 B.分子具有极性 C.分子的空间结构为V形
(2)实验开始即向装置A中通入氮气,目的是___________ 。
(3)装置A中反应的化学方程式为___________ ,装置B的作用是___________ 。
(4)装置D中吸收尾气的反应也可用于制备NaClO2,反应的离子方程式为________ 。
II.我国科学家最近成功合成了世界上首个五氮阴离子盐 (用R代表)。经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。
(用R代表)。经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。

(5)R中阴离子 中的
中的 键总数为
键总数为___________ 个。分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为 ),则
),则 中的大
中的大 键应表示为
键应表示为____________ 。图中虚线代表氢键,其表示式为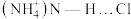 、
、________________ 、______________ 。
 是国际公认的一种安全、低毒的绿色消毒剂。熔点为-59.5℃,沸点为11.0℃,高浓度时极易爆炸,极易溶于水,遇热水易分解。实验室可用如图所示的装置制备
是国际公认的一种安全、低毒的绿色消毒剂。熔点为-59.5℃,沸点为11.0℃,高浓度时极易爆炸,极易溶于水,遇热水易分解。实验室可用如图所示的装置制备 (装置A的酒精灯加热装置略去)。回答下列问题:
(装置A的酒精灯加热装置略去)。回答下列问题:
(1)下列关于ClO2分子结构和性质的说法错误的是
A.分子中只含
 键 B.分子具有极性 C.分子的空间结构为V形
键 B.分子具有极性 C.分子的空间结构为V形(2)实验开始即向装置A中通入氮气,目的是
(3)装置A中反应的化学方程式为
(4)装置D中吸收尾气的反应也可用于制备NaClO2,反应的离子方程式为
II.我国科学家最近成功合成了世界上首个五氮阴离子盐
 (用R代表)。经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。
(用R代表)。经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。
(5)R中阴离子
 中的
中的 键总数为
键总数为 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为 ),则
),则 中的大
中的大 键应表示为
键应表示为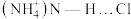 、
、
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】亚硝酰氯( )是一种红褐色液体或黄色气体,沸点为
)是一种红褐色液体或黄色气体,沸点为 ,遇水和潮气分解。请回答下列问题:
,遇水和潮气分解。请回答下列问题:
(1) 与
与 混合在通常条件下可反应得到
混合在通常条件下可反应得到 。
。
①实验室制备 的离子方程式是
的离子方程式是_______ 。
②选用如图所示的部分装置,欲用二氧化锰制备一瓶纯净且干燥的氯气,各玻璃导管接口连接顺序为_______ (气流方向从左至右,每组仪器最多使用一次)。

③实验中“先通入 ,待反应装置中充满黄绿色气体时,再将
,待反应装置中充满黄绿色气体时,再将 缓缓通入”,此操作的目的是
缓缓通入”,此操作的目的是_______ 。
(2)文献中记载的一种利用浓盐酸和 浓溶液反应制取
浓溶液反应制取 的原理及装置如图所示,反应原理:
的原理及装置如图所示,反应原理: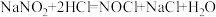 。
。

①仪器X为恒压滴液漏斗,用它代替分液漏斗优点是_______ 。
②若无干燥装置, 会与水反应产生无色气体和白雾,且该气体在试管口变为红棕色,则发生反应的化学方程式为
会与水反应产生无色气体和白雾,且该气体在试管口变为红棕色,则发生反应的化学方程式为_______ 。
(3)若用以下方法测定亚硝酰氯( )纯度:取U形管中所得液体m克溶于水,配制成
)纯度:取U形管中所得液体m克溶于水,配制成 溶液,取出
溶液,取出 ,以
,以 溶液为指示剂,用
溶液为指示剂,用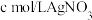 标准溶液滴定至终点,消耗标准溶液的体积为
标准溶液滴定至终点,消耗标准溶液的体积为 。已知:
。已知: 为不溶于水的砖红色沉淀;常温下
为不溶于水的砖红色沉淀;常温下 ,
,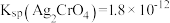 。
。
①滴定时,应使用_______ (填“酸式”或“碱式”)滴定管。
②滴定达到终点的标志是_______ 。
③亚硝酰氯( )的质量分数为
)的质量分数为_______ (用计算式表示即可)。
 )是一种红褐色液体或黄色气体,沸点为
)是一种红褐色液体或黄色气体,沸点为 ,遇水和潮气分解。请回答下列问题:
,遇水和潮气分解。请回答下列问题:(1)
 与
与 混合在通常条件下可反应得到
混合在通常条件下可反应得到 。
。①实验室制备
 的离子方程式是
的离子方程式是②选用如图所示的部分装置,欲用二氧化锰制备一瓶纯净且干燥的氯气,各玻璃导管接口连接顺序为

③实验中“先通入
 ,待反应装置中充满黄绿色气体时,再将
,待反应装置中充满黄绿色气体时,再将 缓缓通入”,此操作的目的是
缓缓通入”,此操作的目的是(2)文献中记载的一种利用浓盐酸和
 浓溶液反应制取
浓溶液反应制取 的原理及装置如图所示,反应原理:
的原理及装置如图所示,反应原理: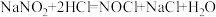 。
。
①仪器X为恒压滴液漏斗,用它代替分液漏斗优点是
②若无干燥装置,
 会与水反应产生无色气体和白雾,且该气体在试管口变为红棕色,则发生反应的化学方程式为
会与水反应产生无色气体和白雾,且该气体在试管口变为红棕色,则发生反应的化学方程式为(3)若用以下方法测定亚硝酰氯(
 )纯度:取U形管中所得液体m克溶于水,配制成
)纯度:取U形管中所得液体m克溶于水,配制成 溶液,取出
溶液,取出 ,以
,以 溶液为指示剂,用
溶液为指示剂,用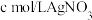 标准溶液滴定至终点,消耗标准溶液的体积为
标准溶液滴定至终点,消耗标准溶液的体积为 。已知:
。已知: 为不溶于水的砖红色沉淀;常温下
为不溶于水的砖红色沉淀;常温下 ,
,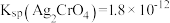 。
。①滴定时,应使用
②滴定达到终点的标志是
③亚硝酰氯(
 )的质量分数为
)的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】硫氰化钾(KSCN)是一种用途广泛的化学药品,常用于合成树脂、杀虫杀菌剂等。某实验小组用下图所示的装置制备硫氰化钾。

已知:NH3不溶于CS2,CS2不溶于水且密度比水大。
I.制备NH4SCN溶液
(1)组装仪器后应先进行的操作是_______ ,a装置为实验室制氨气的装置,所发生反应的化学方程式为_______ 。
(2)三颈烧瓶内盛放有CS2、水和固体催化剂,发生反应CS2+3NH3 NH4SCN+NH4HS。实验开始时,打开K1,水浴加热装置d,反应发生。判断CS2已反应完全的依据是
NH4SCN+NH4HS。实验开始时,打开K1,水浴加热装置d,反应发生。判断CS2已反应完全的依据是_______ 。
II.制备KSCN溶液
(3)关闭K1,将三颈烧瓶继续加热至100°C,待NH4HS完全分解后,再打开K2,继续保持水浴温度为100℃,缓缦滴入稍过量的KOH溶液,制得KSCN溶液。e中用H2SO4酸化的CuSO4吸收尾气时可以看到有黑色的沉淀生成,则生成黑色沉淀的离子方程式为_______ 。
(4)下列说法正确的是_______(填字母)。
III.制备KSCN晶体
(5)先通过_______ (填实验操作名称)除去三颈烧瓶中的固体催化剂,再通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到硫氰化钾晶体。
(6)测定产品中KSCN的含量:称取1.00g实验产品,用蒸馏水溶解后,定容于100mL容量瓶中,移取25.00mL用0.1000mol·L-1 AgNO3溶液反应,消耗AgNO3溶液的体积为24.00mL。反应时发生的离子反应为:SCN-+Ag+=AgSCN↓(白色),则产品中KSCN的质量分数为_______ (计算结果保留三位有效数字)。

已知:NH3不溶于CS2,CS2不溶于水且密度比水大。
I.制备NH4SCN溶液
(1)组装仪器后应先进行的操作是
(2)三颈烧瓶内盛放有CS2、水和固体催化剂,发生反应CS2+3NH3
 NH4SCN+NH4HS。实验开始时,打开K1,水浴加热装置d,反应发生。判断CS2已反应完全的依据是
NH4SCN+NH4HS。实验开始时,打开K1,水浴加热装置d,反应发生。判断CS2已反应完全的依据是II.制备KSCN溶液
(3)关闭K1,将三颈烧瓶继续加热至100°C,待NH4HS完全分解后,再打开K2,继续保持水浴温度为100℃,缓缦滴入稍过量的KOH溶液,制得KSCN溶液。e中用H2SO4酸化的CuSO4吸收尾气时可以看到有黑色的沉淀生成,则生成黑色沉淀的离子方程式为
(4)下列说法正确的是_______(填字母)。
| A.通过观察c中的气泡流速,控制a中产生氨气的速率 |
| B.装置b可以填充P2O5 |
| C.三颈烧瓶中长导气管可以不插入到CS2中 |
| D.d中橡皮管的作用是平衡气压,使KOH溶液能顺利滴下 |
III.制备KSCN晶体
(5)先通过
(6)测定产品中KSCN的含量:称取1.00g实验产品,用蒸馏水溶解后,定容于100mL容量瓶中,移取25.00mL用0.1000mol·L-1 AgNO3溶液反应,消耗AgNO3溶液的体积为24.00mL。反应时发生的离子反应为:SCN-+Ag+=AgSCN↓(白色),则产品中KSCN的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】氯化亚铜广泛用于有机合成、杀菌和化学分析,它是一种白色固体,难溶于水和乙醇,可溶于氯离子浓度较大的体系,在潮湿空气中易水解和氧化。学习小组在实验室中制备CuCl并测定产品纯度,进行如下实验探究。回答下列问题:
制备CuCl的反应、装置示意图和实验步骤如下。
反应:2Cu2++2Cl-+SO2+2H2O=2CuCl↓+4H++SO
溶液中存在:CuCl+2Cl- [CuCl3]2-(茶褐色)
[CuCl3]2-(茶褐色)
装置:

实验步骤:
Ⅰ.安装好装置,检验装置的气密性,添加药品;
Ⅱ.打开K,向装置中通入一段时间N2;
Ⅲ.关闭K,向三颈烧瓶中滴入70%硫酸,向B中混合溶液内通入SO2;
Ⅳ.B中充分反应后,向圆底烧瓶中加入适量水稀释,而后过滤、洗涤、干燥,制得产品
(1)步骤Ⅰ中检验装置气密性的方法为___________ 。
(2)仪器a的名称为___________ ;步骤Ⅲ中,为使70%硫酸顺利滴下,仪器a上口玻璃塞___________ (填“需要”或“不需要”)事先打开;本实验选用70%硫酸制备SO2的原因为___________ 。
(3)步骤Ⅳ中,加水稀释的目的为___________ ;洗涤包括酸洗、水洗、醇洗,其中醇洗的目的为___________ 。
(4)测定产品纯度:准确称取m g产品,加入足量FeCl3溶液;充分反应后滴加指示剂,用c mol·L-1 Ce(SO4)2标准溶液滴定生成的Fe2+(还原产物为Ce3+),达到终点时消耗V mL标准液。
①产品中加入FeCl3溶液时,发生反应的离子方程式为___________ 。
②产品中CuCl的质量分数为___________ 。
制备CuCl的反应、装置示意图和实验步骤如下。
反应:2Cu2++2Cl-+SO2+2H2O=2CuCl↓+4H++SO

溶液中存在:CuCl+2Cl-
 [CuCl3]2-(茶褐色)
[CuCl3]2-(茶褐色)装置:

实验步骤:
Ⅰ.安装好装置,检验装置的气密性,添加药品;
Ⅱ.打开K,向装置中通入一段时间N2;
Ⅲ.关闭K,向三颈烧瓶中滴入70%硫酸,向B中混合溶液内通入SO2;
Ⅳ.B中充分反应后,向圆底烧瓶中加入适量水稀释,而后过滤、洗涤、干燥,制得产品
(1)步骤Ⅰ中检验装置气密性的方法为
(2)仪器a的名称为
(3)步骤Ⅳ中,加水稀释的目的为
(4)测定产品纯度:准确称取m g产品,加入足量FeCl3溶液;充分反应后滴加指示剂,用c mol·L-1 Ce(SO4)2标准溶液滴定生成的Fe2+(还原产物为Ce3+),达到终点时消耗V mL标准液。
①产品中加入FeCl3溶液时,发生反应的离子方程式为
②产品中CuCl的质量分数为
您最近一年使用:0次



