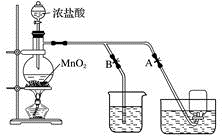
下图表示在没有通风橱时制取纯净的氯气时设计的装置图,图中A、B是可控制的弹簧铁夹。
(1)烧杯中盛放的液体是__________ ,其作用是_________ ,水槽中盛放的液体是_________ 。
(2)简述操作过程:(从氯气已经产生开始)在收集氯气之前,应__________________________ ;当氯气纯度合乎要求时,应__________________________________ ,当氯气收集完毕时,应______ 。
(3)将8.7 g二氧化锰与含氯化氢14.6 g的浓盐酸共热制氯气,甲同学认为可制得氯气 7.1 g,乙同学认为制得氯气的质量小于7.1 g,你认为________ (填“甲”或“乙”)同学正确,原因是_________ 。
(1)烧杯中盛放的液体是
(2)简述操作过程:(从氯气已经产生开始)在收集氯气之前,应
(3)将8.7 g二氧化锰与含氯化氢14.6 g的浓盐酸共热制氯气,甲同学认为可制得氯气 7.1 g,乙同学认为制得氯气的质量小于7.1 g,你认为
18-19高一上·贵州黔东南·阶段练习 查看更多[3]
(已下线)3.1.1 氯气的发现与制备 练习(1)——《高中新教材同步备课》(苏教版 必修第一册)贵州省剑河县二中2018-2019学年高二上学期期末考试化学试题贵州省剑河县第二中学2018-2019学年高一上学期12月份考试化学试题
更新时间:2019-01-12 20:40:04
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
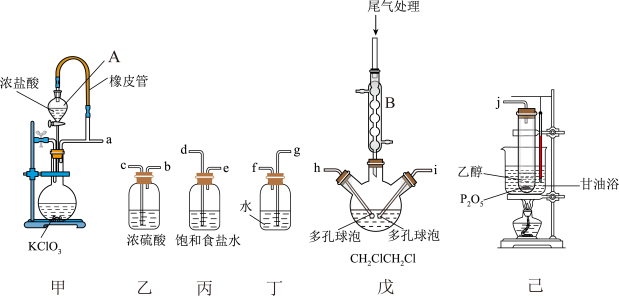
【推荐1】1,2-二氯乙烷( )是重要的有机化工原料,不溶于水,易溶于有机溶剂,沸点83.6℃;在光照下逐渐分解。实验室采用“乙烯液相直接氯化法”制备1,2-二氯乙烷,相关反应原理和实验装置图如下:
)是重要的有机化工原料,不溶于水,易溶于有机溶剂,沸点83.6℃;在光照下逐渐分解。实验室采用“乙烯液相直接氯化法”制备1,2-二氯乙烷,相关反应原理和实验装置图如下:
已知:
①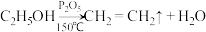 ②
②

回答下列问题:
(1)仪器B的名称是___________ ,其作用是___________ 。
(2)制取1,2-二氯乙烷的装置接口顺序为(箭头为气流方向,部分装置可重复使用):a→d→e→c→b→h-i←______←_______←_______←________←j。___________
(3)丁装置的作用是___________ 。
(4)戊装置中多孔球泡的作用是___________ 。反应开始前先向戊中装入1,2-二氯乙烷液体,其作用是___________ (填序号)。
a.溶解 和乙烯 b.作催化剂 c.促进气体反应物间的接触
和乙烯 b.作催化剂 c.促进气体反应物间的接触
(5)产品纯度的测定:量取5.5mL逐出 和乙烯后的产品,产品密度为1.2g/mL,加足量稀NaOH溶液,加热充分反应:
和乙烯后的产品,产品密度为1.2g/mL,加足量稀NaOH溶液,加热充分反应: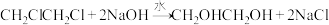 所得溶液先用稀硝酸中和至酸性,然后加入1.0000mol/L的
所得溶液先用稀硝酸中和至酸性,然后加入1.0000mol/L的 标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,则产品中l,2-二氯乙烷的纯度为
标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,则产品中l,2-二氯乙烷的纯度为___________ %。
 )是重要的有机化工原料,不溶于水,易溶于有机溶剂,沸点83.6℃;在光照下逐渐分解。实验室采用“乙烯液相直接氯化法”制备1,2-二氯乙烷,相关反应原理和实验装置图如下:
)是重要的有机化工原料,不溶于水,易溶于有机溶剂,沸点83.6℃;在光照下逐渐分解。实验室采用“乙烯液相直接氯化法”制备1,2-二氯乙烷,相关反应原理和实验装置图如下:
已知:
①
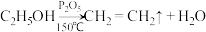 ②
②

回答下列问题:
(1)仪器B的名称是
(2)制取1,2-二氯乙烷的装置接口顺序为(箭头为气流方向,部分装置可重复使用):a→d→e→c→b→h-i←______←_______←_______←________←j。
(3)丁装置的作用是
(4)戊装置中多孔球泡的作用是
a.溶解
 和乙烯 b.作催化剂 c.促进气体反应物间的接触
和乙烯 b.作催化剂 c.促进气体反应物间的接触(5)产品纯度的测定:量取5.5mL逐出
 和乙烯后的产品,产品密度为1.2g/mL,加足量稀NaOH溶液,加热充分反应:
和乙烯后的产品,产品密度为1.2g/mL,加足量稀NaOH溶液,加热充分反应: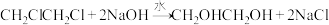 所得溶液先用稀硝酸中和至酸性,然后加入1.0000mol/L的
所得溶液先用稀硝酸中和至酸性,然后加入1.0000mol/L的 标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,则产品中l,2-二氯乙烷的纯度为
标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,则产品中l,2-二氯乙烷的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某化学兴趣小组设计了如图装置,该装置能制取 ,并进行相关性质实验,且可利用装置G储存多余的氯气。
,并进行相关性质实验,且可利用装置G储存多余的氯气。

(1)A中发生反应的化学方程式为___________ 。
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯。回答下列问题:
①在装置D中能看到的实验现象是___________ 。
②在装置E的硬质玻璃管内盛有炭粉,发生氧化还原反应,产物为 和HCl,则E中发生反应的化学方程式为
和HCl,则E中发生反应的化学方程式为___________ 。
③装置F中球形干燥管的作用是___________ 。
(3)储气瓶b内盛放的试剂是___________ 。
(4)装置B中 被
被 氧化为
氧化为 ,反应的离子方程式为
,反应的离子方程式为___________ 。
(5)装置C中反应的化学方程式为___________ 。
 ,并进行相关性质实验,且可利用装置G储存多余的氯气。
,并进行相关性质实验,且可利用装置G储存多余的氯气。
(1)A中发生反应的化学方程式为
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯。回答下列问题:
①在装置D中能看到的实验现象是
②在装置E的硬质玻璃管内盛有炭粉,发生氧化还原反应,产物为
 和HCl,则E中发生反应的化学方程式为
和HCl,则E中发生反应的化学方程式为③装置F中球形干燥管的作用是
(3)储气瓶b内盛放的试剂是
(4)装置B中
 被
被 氧化为
氧化为 ,反应的离子方程式为
,反应的离子方程式为(5)装置C中反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】在实验室中利用二氧化锰与浓盐酸反应制备干燥、纯净的氯气,所用装置如图所示:
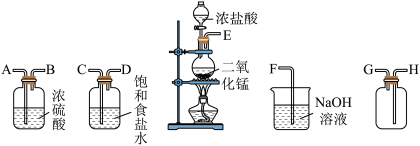
(1)连接上述装置的正确顺序(填各接口处的字母):____接___;___接___;___接___;___接___。__
(2)装置中,饱和食盐水的作用是__ ;NaOH溶液的作用是__ 。
(3)化学实验中常用湿润的淀粉—KI试纸检验是否有Cl2产生。如果有Cl2产生,可观察到__ ,反应化学方程式为___ 。
(4)写出下列化学反应的化学方程式:
①气体发生装置中进行的反应:___ 。
②NaOH溶液中发生的反应:____ 。

(1)连接上述装置的正确顺序(填各接口处的字母):____接___;___接___;___接___;___接___。
(2)装置中,饱和食盐水的作用是
(3)化学实验中常用湿润的淀粉—KI试纸检验是否有Cl2产生。如果有Cl2产生,可观察到
(4)写出下列化学反应的化学方程式:
①气体发生装置中进行的反应:
②NaOH溶液中发生的反应:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】高纯硅被誉为“信息革命的催化剂”。某小组同学模拟工业上用 与
与 在
在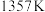 的条件下制备高纯硅,实验装置如图所示(加热及夹持装置已略去)。
的条件下制备高纯硅,实验装置如图所示(加热及夹持装置已略去)。
已知:① 的沸点为
的沸点为 ,密度为
,密度为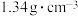 ,易溶于有机溶剂,能与
,易溶于有机溶剂,能与 剧烈反应,在空气中易被氧化;
剧烈反应,在空气中易被氧化;
② ;
;
③银氨溶液中存在: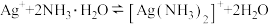 。
。
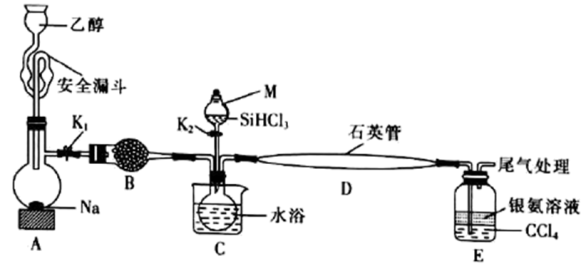
实验步骤:
①打开 ,向安全漏斗中加入足量乙醇,使装置
,向安全漏斗中加入足量乙醇,使装置 中的反应进行一段时间;
中的反应进行一段时间;
②加热装置 ,打开
,打开 ,滴加
,滴加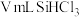 ;
;
③加热装置 至
至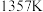 ;
;
④关闭 ;
;
⑤关闭 。
。
回答下列问题:
(1)仪器 的名称为
的名称为___________ 。
(2)相比长颈漏斗,安全漏斗使用时的优点是___________ 。
(3)干燥管 中盛装的试剂是
中盛装的试剂是___________ 。
(4)加热装置 之前,先进行装置
之前,先进行装置 中的反应,这样操作的目的是
中的反应,这样操作的目的是___________ 。
(5)装置 中发生反应的化学方程式为
中发生反应的化学方程式为___________ 。
(6) 中
中 的作用是
的作用是___________ ,实验过程中, 的上层溶液中观察到的现象是
的上层溶液中观察到的现象是___________ ,尾气的主要成分是___________ (填化学式)。
(7)根据下列数据可以计算出 的利用率的是
的利用率的是___________ (填标号)。
a.钠的质量b.乙醇的体积和密度c.硅的质量
 与
与 在
在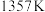 的条件下制备高纯硅,实验装置如图所示(加热及夹持装置已略去)。
的条件下制备高纯硅,实验装置如图所示(加热及夹持装置已略去)。已知:①
 的沸点为
的沸点为 ,密度为
,密度为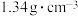 ,易溶于有机溶剂,能与
,易溶于有机溶剂,能与 剧烈反应,在空气中易被氧化;
剧烈反应,在空气中易被氧化;②
 ;
;③银氨溶液中存在:
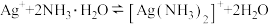 。
。
实验步骤:
①打开
 ,向安全漏斗中加入足量乙醇,使装置
,向安全漏斗中加入足量乙醇,使装置 中的反应进行一段时间;
中的反应进行一段时间;②加热装置
 ,打开
,打开 ,滴加
,滴加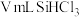 ;
;③加热装置
 至
至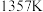 ;
;④关闭
 ;
;⑤关闭
 。
。回答下列问题:
(1)仪器
 的名称为
的名称为(2)相比长颈漏斗,安全漏斗使用时的优点是
(3)干燥管
 中盛装的试剂是
中盛装的试剂是(4)加热装置
 之前,先进行装置
之前,先进行装置 中的反应,这样操作的目的是
中的反应,这样操作的目的是(5)装置
 中发生反应的化学方程式为
中发生反应的化学方程式为(6)
 中
中 的作用是
的作用是 的上层溶液中观察到的现象是
的上层溶液中观察到的现象是(7)根据下列数据可以计算出
 的利用率的是
的利用率的是a.钠的质量b.乙醇的体积和密度c.硅的质量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】四氯化钛(TiCl4)是生产金属钛及其化合物的重要中间体。室温下,四氯化钛为无色液体。某化学兴趣小组同学以TiO2和CCl4为原料在实验室制取液态TiCl4,装置如图所示。

有关信息如下:
①反应原理:TiO2(s)+CCl4(g) TiCl4(g)+CO2(g)。
TiCl4(g)+CO2(g)。
②反应条件:无水无氧且加热。
③有关物质性质如表:
请回答下列问题:
(1)装置F中有氮气生成,该反应的化学方程式为______ 。
(2)实验装置依次连接的顺序为F→B→______ →______ →______ →______ 。
(3)欲分离C中的液态混合物,所采用操作的名称是______ 。
(4)实验开始前首先点燃______ 处酒精灯(填“D 或 F”),目的是______ 。
(5)E装置_______ 填“能或不能”)换成B装置,理由是______ 。

有关信息如下:
①反应原理:TiO2(s)+CCl4(g)
 TiCl4(g)+CO2(g)。
TiCl4(g)+CO2(g)。②反应条件:无水无氧且加热。
③有关物质性质如表:
| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
请回答下列问题:
(1)装置F中有氮气生成,该反应的化学方程式为
(2)实验装置依次连接的顺序为F→B→
(3)欲分离C中的液态混合物,所采用操作的名称是
(4)实验开始前首先点燃
(5)E装置
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】重铬酸钾( )是实验室常用的氧化剂。某实验小组以铬铁矿(主要成分为
)是实验室常用的氧化剂。某实验小组以铬铁矿(主要成分为 ,含
,含 、
、 等杂质)为原料制备重铬酸钾,并进行性质验证实验。
等杂质)为原料制备重铬酸钾,并进行性质验证实验。
已知:相关物质在不同温度时的溶解度/g如下表:
实验一:重铬酸钾的制备
步骤Ⅰ:将一定量NaOH和 的固体置于铁坩埚内,加热至熔融,再加铬铁矿粉与
的固体置于铁坩埚内,加热至熔融,再加铬铁矿粉与 继续加热50分钟,发生反应:
继续加热50分钟,发生反应: ,自然冷却。
,自然冷却。
步骤Ⅱ:取出坩埚中的熔块,置于烧杯中,加水并加热煮沸15分钟,冷却后抽滤,弃去含铁固体物质。
步骤Ⅲ:用冰醋酸调节上述滤液pH为7到8,产生浑浊,加热后过滤除去 和
和 ,将滤液转移至蒸发皿中,加冰醋酸调节pH为5。
,将滤液转移至蒸发皿中,加冰醋酸调节pH为5。
步骤Ⅳ:向上述溶液中加KCl,出现少量晶体再次调pH并进行结晶操作,有大量橙色晶体析出,抽滤,用少量冷水洗涤晶体,干燥得 晶体。
晶体。
回答下列问题:
(1)步骤Ⅰ中下列仪器不需要的是_____ (填仪器名称)。

(2)步骤Ⅲ中调节滤液pH用冰醋酸,不用强酸的原因是_______ ,过滤前先加热的目的是________ 。
(3)步骤Ⅳ中的结晶方法是_______ (填“蒸发结晶”或“冷却结晶”),有同学制得的重铬酸钾晶体颜色偏黄,可能的原因是_______ 。
实验二:用重铬酸钾测定 固体试样中铁的含量
固体试样中铁的含量
已知:二苯胺磺酸钠还原态为无色,氧化态为紫红色。
(4)取重铬酸钾晶体配制成0.02mol/L的标准液。称取2.00g 固体试样于锥形瓶中,加15.00mL混合酸,再加水配成100mL溶液,取10.00mL
固体试样于锥形瓶中,加15.00mL混合酸,再加水配成100mL溶液,取10.00mL 溶液于锥形瓶,加入几滴二苯胺磺酸钠作指示剂,用重铬酸钾标准液滴定至由绿色变为紫红色,消耗标准液8.00mL。
溶液于锥形瓶,加入几滴二苯胺磺酸钠作指示剂,用重铬酸钾标准液滴定至由绿色变为紫红色,消耗标准液8.00mL。
①写出滴定时重铬酸钾和硫酸亚铁反应的离子方程式________ 。
②测定 固体试样中铁的质量分数为
固体试样中铁的质量分数为_____ (保留两位小数)。
③测定结果偏大的可能原因是_______ 。
 )是实验室常用的氧化剂。某实验小组以铬铁矿(主要成分为
)是实验室常用的氧化剂。某实验小组以铬铁矿(主要成分为 ,含
,含 、
、 等杂质)为原料制备重铬酸钾,并进行性质验证实验。
等杂质)为原料制备重铬酸钾,并进行性质验证实验。已知:相关物质在不同温度时的溶解度/g如下表:
| 物质 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ |
| 重铬酸钾 | 4.7 | 12.3 | 26.3 | 45.6 | 73 |
| 重铬酸钠 | 163 | 183 | 215 | 269 | 76 |
步骤Ⅰ:将一定量NaOH和
 的固体置于铁坩埚内,加热至熔融,再加铬铁矿粉与
的固体置于铁坩埚内,加热至熔融,再加铬铁矿粉与 继续加热50分钟,发生反应:
继续加热50分钟,发生反应: ,自然冷却。
,自然冷却。步骤Ⅱ:取出坩埚中的熔块,置于烧杯中,加水并加热煮沸15分钟,冷却后抽滤,弃去含铁固体物质。
步骤Ⅲ:用冰醋酸调节上述滤液pH为7到8,产生浑浊,加热后过滤除去
 和
和 ,将滤液转移至蒸发皿中,加冰醋酸调节pH为5。
,将滤液转移至蒸发皿中,加冰醋酸调节pH为5。步骤Ⅳ:向上述溶液中加KCl,出现少量晶体再次调pH并进行结晶操作,有大量橙色晶体析出,抽滤,用少量冷水洗涤晶体,干燥得
 晶体。
晶体。回答下列问题:
(1)步骤Ⅰ中下列仪器不需要的是

(2)步骤Ⅲ中调节滤液pH用冰醋酸,不用强酸的原因是
(3)步骤Ⅳ中的结晶方法是
实验二:用重铬酸钾测定
 固体试样中铁的含量
固体试样中铁的含量已知:二苯胺磺酸钠还原态为无色,氧化态为紫红色。
(4)取重铬酸钾晶体配制成0.02mol/L的标准液。称取2.00g
 固体试样于锥形瓶中,加15.00mL混合酸,再加水配成100mL溶液,取10.00mL
固体试样于锥形瓶中,加15.00mL混合酸,再加水配成100mL溶液,取10.00mL 溶液于锥形瓶,加入几滴二苯胺磺酸钠作指示剂,用重铬酸钾标准液滴定至由绿色变为紫红色,消耗标准液8.00mL。
溶液于锥形瓶,加入几滴二苯胺磺酸钠作指示剂,用重铬酸钾标准液滴定至由绿色变为紫红色,消耗标准液8.00mL。①写出滴定时重铬酸钾和硫酸亚铁反应的离子方程式
②测定
 固体试样中铁的质量分数为
固体试样中铁的质量分数为③测定结果偏大的可能原因是
您最近一年使用:0次



