用氢气还原某二价金属氧化物,使金属元素成为单质,每4.0 g金属氧化物被还原时,需耗用0.10 g氢气,则该金属的相对原子质量是_________ ?写出该金属元素的名称为_______ 。
11-12高一上·浙江杭州·阶段练习 查看更多[1]
(已下线)2011-2012年浙江省杭州市西湖高级中学高一10月考化学试卷
更新时间:2011-10-19 12:51:16
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】回答下列问题
(1)49 g H2SO4的物质的量是_______ ;1.5 mol H2SO4的质量是_______ ,其中含有_______ molH
(2)已知NH3的相对分子质量为17,则NH3的摩尔质量为_______ 。
(3)标准状况下,16gO2的体积_______ L。
(4)6.02×1023个水分子的物质的量_______ mol。
(1)49 g H2SO4的物质的量是
(2)已知NH3的相对分子质量为17,则NH3的摩尔质量为
(3)标准状况下,16gO2的体积
(4)6.02×1023个水分子的物质的量
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】现有14.4gCO和CO2的混合气体,在标准状况下其体积为8.96L。
(1)将混合气体依次通过下列如图所示装置,最后收集在气球中(实验在标准状况下测定)。
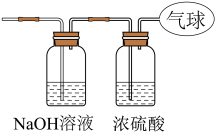
①气球中收集到的气体的摩尔质量为___ 。
②收集到气球中的气体的电子总数为____ (用NA表示阿伏加 德罗常数的值)。
(2)求该混合气体的平均摩尔质量(要有计算过程)___
(3)求混合气体中碳原子的个数(用NA表示阿伏加 德罗常数的值,且要有计算过程)。___
(1)将混合气体依次通过下列如图所示装置,最后收集在气球中(实验在标准状况下测定)。

①气球中收集到的气体的摩尔质量为
②收集到气球中的气体的电子总数为
(2)求该混合气体的平均摩尔质量(要有计算过程)
(3)求混合气体中碳原子的个数(用NA表示阿伏加 德罗常数的值,且要有计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】若将25mL盐酸与4.2gNaHCO3充分反应,计算:
(1)在标准状况下可得多少升CO2____ ?
(2)所使用盐酸的物质的量浓度是多少____ ?
(1)在标准状况下可得多少升CO2
(2)所使用盐酸的物质的量浓度是多少
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
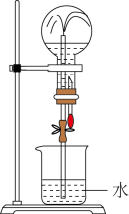
【推荐2】中学实验中,通常利用如图所示的装置进行喷泉实验,来验证HCl的极易溶于水。喷泉结束后,溶液占烧瓶体积的4/5,(已知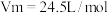 ,空气中
,空气中 占4/5)。不考虑扩散等其他因素,所得溶液的物质的量浓度约为
占4/5)。不考虑扩散等其他因素,所得溶液的物质的量浓度约为_______ ,(保留三位有效数字,下同)该瓶气体是用排空气法收集而得,则相同条件下混合气体对氢气的相对密度为_______ 。
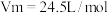 ,空气中
,空气中 占4/5)。不考虑扩散等其他因素,所得溶液的物质的量浓度约为
占4/5)。不考虑扩散等其他因素,所得溶液的物质的量浓度约为
您最近一年使用:0次
【推荐1】HIO4主要以H5IO6形式存在,H5IO6是白色晶体,易溶于水,具有很强的氧化性,在强酸溶液中能氧化Mn2+。
(1)请完成并配平下列离子反应。
__________ Mn2++________ H5IO6
__________  +
+________ 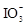 +
+________ H++________
(2)根据以上离子方程式判断H5IO6是________ 电离物质(填“易”或“难”)。
(3)上述反应,被氧化的元素是________ (填元素符号),当1 mol Mn2+参加反应时,转移电子的物质的量为________ 。
(1)请完成并配平下列离子反应。

 +
+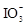 +
+(2)根据以上离子方程式判断H5IO6是
(3)上述反应,被氧化的元素是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】环境问题越来越受到人们的重视,“绿水青山就是金山银山”的理念已被人们认同。运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染具有重要意义。回答下列问题:
(1)亚硝酰氯(Cl—N=O)气体是有机合成中的重要试剂,它可由Cl2和NO在通常条件下反应制得,该反应的热化学方程式为______________________ 。相关化学键的键能如下表所示:
(2)有人设想采用下列方法减少SO2、NO2对环境的污染:用CH4还原SO2,从产物中分离出一种含硫质量分数约为94%的化合物,并用这种化合物来还原NO2。这种含硫化合物和NO2反应的化学方程式为______________________ 。
(3)用NaOH溶液吸收SO2也是减少大气污染的一种有效方法。25℃时,将一定量的SO2通入到NaOH溶液中,两者完全反应,若溶液中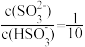 ,则该混合溶液的pH=
,则该混合溶液的pH=___________ (25℃时,H2SO3的电离平衡常数Ka1=1.0×10-2,K a2=1.0×10-7)。
(1)亚硝酰氯(Cl—N=O)气体是有机合成中的重要试剂,它可由Cl2和NO在通常条件下反应制得,该反应的热化学方程式为
| 化学键 | Cl—Cl | N≡O(NO气体) | Cl—N | N=O |
| 键能/(kJ·mol-1) | 243 | 630 | 200 | 607 |
(2)有人设想采用下列方法减少SO2、NO2对环境的污染:用CH4还原SO2,从产物中分离出一种含硫质量分数约为94%的化合物,并用这种化合物来还原NO2。这种含硫化合物和NO2反应的化学方程式为
(3)用NaOH溶液吸收SO2也是减少大气污染的一种有效方法。25℃时,将一定量的SO2通入到NaOH溶液中,两者完全反应,若溶液中
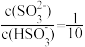 ,则该混合溶液的pH=
,则该混合溶液的pH=
您最近一年使用:0次
【推荐3】已知铜和浓硫酸可以在加热条件下发生反应,化学方程式如下(已配平),Cu+2H2SO4(浓)  CuSO4+A↑+2H2O,试通过计算和推理完成下面的问题:
CuSO4+A↑+2H2O,试通过计算和推理完成下面的问题:
(1)在参加反应的硫酸中,被还原的硫酸与未被还原的硫酸的物质的量之比为_________ 。A物质可以与强碱反应生成盐和水。则A应该属于_________ (用字母代号填写)。
a.酸 b.碱 c.盐 d.酸性氧化物 e.碱性氧化物
(2)一定量的铜片与含1.8mol H2SO4的浓H2SO4充分反应(浓H2SO4过量),如果该反应过程中转移了0.2 mol电子,生成的A气体在标准状况下体积为_________ L(假设气体全部逸出)。
(3)将(2)中反应后所得到的溶液稀释后与足量Ba(OH)2溶液反应,所得沉淀的质量为________________ g。写出此过程中发生反应的化学方程式:_______________
 CuSO4+A↑+2H2O,试通过计算和推理完成下面的问题:
CuSO4+A↑+2H2O,试通过计算和推理完成下面的问题:(1)在参加反应的硫酸中,被还原的硫酸与未被还原的硫酸的物质的量之比为
a.酸 b.碱 c.盐 d.酸性氧化物 e.碱性氧化物
(2)一定量的铜片与含1.8mol H2SO4的浓H2SO4充分反应(浓H2SO4过量),如果该反应过程中转移了0.2 mol电子,生成的A气体在标准状况下体积为
(3)将(2)中反应后所得到的溶液稀释后与足量Ba(OH)2溶液反应,所得沉淀的质量为
您最近一年使用:0次
【推荐1】实验室可以用KClO3和50mL浓盐酸反应制取Cl2,反应原理如下:
KClO3+HCl→KCl+Cl2↑+H2O
(1)配平上述化学方程式并用双线桥标出电子转移方向与数目__________________ ;
(2)浓盐酸在上述反应中表现出来的性质是__ (填选项编号)
A.只有氧化性 B.只有还原性 C.还原性和酸性 D.氧化性和酸性
(3)若产生0.1mol Cl2,则转移电子的物质的量为_______ (保留两位小数)
(4)若反应中HCl的利用率只有50%,当氧化产物比还原产物比还原产物多7.1g时,浓盐酸的物质的量浓度为__________ .
KClO3+HCl→KCl+Cl2↑+H2O
(1)配平上述化学方程式并用双线桥标出电子转移方向与数目
(2)浓盐酸在上述反应中表现出来的性质是
A.只有氧化性 B.只有还原性 C.还原性和酸性 D.氧化性和酸性
(3)若产生0.1mol Cl2,则转移电子的物质的量为
(4)若反应中HCl的利用率只有50%,当氧化产物比还原产物比还原产物多7.1g时,浓盐酸的物质的量浓度为
您最近一年使用:0次
【推荐2】将一定量的SO2和含0.7mol氧气的空气(忽略CO2)放入一定体积的密闭容器中,550℃时,在催化剂作用下发生反应:2SO2+O2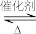 2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)
2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)
(1)求该反应达到平衡时SO2的转化率(用百分数表示)。_____________
(2)若将平衡混合气体的5%通入过量的BaCl2溶液,生成沉淀多少克?(要有解题过程)____
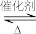 2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)
2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)(1)求该反应达到平衡时SO2的转化率(用百分数表示)。
(2)若将平衡混合气体的5%通入过量的BaCl2溶液,生成沉淀多少克?(要有解题过程)
您最近一年使用:0次



