按要求答题
I.NaNO2 因外观和食盐相似,又有咸味,容易使人误食中毒。已知 NaNO2能发生反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是________ 。
(2)根据上述反应,鉴别 NaNO2 和 NaCl。可选用的物质有①水、②碘化钾淀粉试纸③淀粉、④白酒、⑤食醋,你认为必须选用的物质有________ (填序号)。
(3)请配平以下化学方程式:____Al+____NaNO3+____ NaOH= ____NaAlO2+____ N2↑+___H2O,________________ ,若反应过程中转移 5 mol 电子,则生成标准状况下 N2 的体积为_________ L。
II.向100mL1.5mol/L 的氢氧化钠溶液中缓慢通入一定量的CO2,反应后,向所得溶液中逐滴缓慢滴加一定浓度的盐酸,所得气体的体积与所加盐酸的体积(不考虑气体溶解于水)关系如图所示。

则:①氢氧化钠溶液与一定量的CO2 充分反应后的溶液中溶质为____ (写化学式)。
②盐酸的浓度为_______ 。
③B点时,产生的气体在标准状况下的体积为_______ L。
I.NaNO2 因外观和食盐相似,又有咸味,容易使人误食中毒。已知 NaNO2能发生反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是
(2)根据上述反应,鉴别 NaNO2 和 NaCl。可选用的物质有①水、②碘化钾淀粉试纸③淀粉、④白酒、⑤食醋,你认为必须选用的物质有
(3)请配平以下化学方程式:____Al+____NaNO3+____ NaOH= ____NaAlO2+____ N2↑+___H2O,
II.向100mL1.5mol/L 的氢氧化钠溶液中缓慢通入一定量的CO2,反应后,向所得溶液中逐滴缓慢滴加一定浓度的盐酸,所得气体的体积与所加盐酸的体积(不考虑气体溶解于水)关系如图所示。

则:①氢氧化钠溶液与一定量的CO2 充分反应后的溶液中溶质为
②盐酸的浓度为
③B点时,产生的气体在标准状况下的体积为
更新时间:2019-02-05 20:46:53
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】过氧化氢(H2O2)俗称双氧水,外观为无色透明液体,共水溶液适用于医用伤口消毒、环境消毒和食品消毒。请回答下列问题:
(1)用过氧化钡(BaO2)和硫酸溶液反应可以制备H2O2,该反应的化学方程式为_______ 。
(2)保存H2O2时,不能接触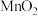 ,请用化学方程式说明其原因:
,请用化学方程式说明其原因:_______ ,该反应属于四大基本反应类型中的_______ 。
(3)H2O2是一种绿色氧化剂,可以用它除去酸性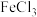 溶液中混有的少量
溶液中混有的少量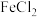 ,发生反应的离子方程式为
,发生反应的离子方程式为_______ ,氧化剂与还原剂的物质的量之比为_______ 。
(4)H2O2能使酸性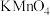 溶液(稀硫酸酸化)褪色,发生反应的化学方程式:
溶液(稀硫酸酸化)褪色,发生反应的化学方程式:
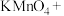
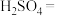
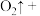
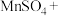
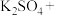 _____
_____
①请配平上述化学方程式,并用双线桥法表示电子的转移方向和数目_______ 。
②该反应中,H2O2作_______ (填“氧化剂”或“还原剂”)。
(1)用过氧化钡(BaO2)和硫酸溶液反应可以制备H2O2,该反应的化学方程式为
(2)保存H2O2时,不能接触
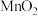 ,请用化学方程式说明其原因:
,请用化学方程式说明其原因:(3)H2O2是一种绿色氧化剂,可以用它除去酸性
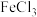 溶液中混有的少量
溶液中混有的少量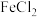 ,发生反应的离子方程式为
,发生反应的离子方程式为(4)H2O2能使酸性
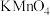 溶液(稀硫酸酸化)褪色,发生反应的化学方程式:
溶液(稀硫酸酸化)褪色,发生反应的化学方程式:
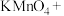
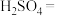
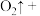
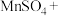
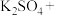 _____
_____①请配平上述化学方程式,并用双线桥法表示电子的转移方向和数目
②该反应中,H2O2作
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】物质的类别和核心元素的化合价是研究物质性质的两个重要角度。如图所示是的其部分化合物的“价类二维图”,根据图示回答下列问题:

(1)常用作保护气(如填充灯泡、贮存粮食等)的是_____ ,可用作制冷剂的是_____ 。
(2)从氮元素的化合价能否发生变化的角度判断,图中既有氧化性又有还原性的含氮化合物有_____ 。
(3)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学方程式:____ 。将64 g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.9 mol,这些气体恰好能被650 mL2 mol/LNaOH溶液完全吸收,生成NaNO3和NaNO2的混合溶液,其中生成的NaNO3的物质的量为___ mol(已知2NO2+2NaOH=NaNO3+NaNO2+H2O)。

(1)常用作保护气(如填充灯泡、贮存粮食等)的是
(2)从氮元素的化合价能否发生变化的角度判断,图中既有氧化性又有还原性的含氮化合物有
(3)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】交警部门严厉打击酒后驾驶行为。80mg/100mL>血液中酒精含量≥20mg/100mL为饮酒驾驶;血液中酒精含量≥80mg/100mL为醉酒驾驶。K2Cr2O7是一种橙红色的物质,当其中的铬元素被还原成正三价铬时,颜色有明显变化。据此,当交警让司机对填充了吸附有K2Cr2O7的硅胶颗粒的装置(即酒精含量探测器)吹气,发生反应。
(1)该反应中K2Cr2O7跟_______ (写化学式)发生了反应,反应中氧化剂是_______ ;
(2)若交警测得某司机血液中酒精含量为0.01mol∙L-1,即证明司机是_______ 。(填“饮酒驾驶”或“醉酒驾驶”)
(1)该反应中K2Cr2O7跟
(2)若交警测得某司机血液中酒精含量为0.01mol∙L-1,即证明司机是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】Cr(Ⅵ)对A体具有致癌、致突变作用。铁氧体法(铁氧体是组成类似于Fe3O4的复合氧化物,其中部分Fe(Ⅲ)可被Cr(Ⅲ)等所代换)是目前处理Cr(Ⅵ)废水的常见方法之一,其工艺流程如下:

铁氧体法处理含Cr2O 废水的工艺流程中:
废水的工艺流程中:
“反应槽”中发生反应的离子方程式为___________ 。

铁氧体法处理含Cr2O
 废水的工艺流程中:
废水的工艺流程中:“反应槽”中发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)在一定条件下,可以用H2O2氧化H2S。随着参加反应的 变化,氧化产物不同,当
变化,氧化产物不同,当 =4时,氧化产物的分子式为
=4时,氧化产物的分子式为________ 。
(2)利用废铁屑制备聚合硫酸铁的过程中,需要向反应釜中加入氧化剂氧化Fe2+,最合适的是________ 。
(3)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO ,常用作脱氯剂,该反应的离子方程式为
,常用作脱氯剂,该反应的离子方程式为______________ 。
(4)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为_____________ 。
(5)SiHCl3在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO)2O等,写出该反应的化学方程式___________ 。
(6)NH3在催化剂条件下还原NO2生成N2和H2O的化学方程式:_________________ 。
 变化,氧化产物不同,当
变化,氧化产物不同,当 =4时,氧化产物的分子式为
=4时,氧化产物的分子式为(2)利用废铁屑制备聚合硫酸铁的过程中,需要向反应釜中加入氧化剂氧化Fe2+,最合适的是
(3)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO
 ,常用作脱氯剂,该反应的离子方程式为
,常用作脱氯剂,该反应的离子方程式为(4)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为
(5)SiHCl3在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO)2O等,写出该反应的化学方程式
(6)NH3在催化剂条件下还原NO2生成N2和H2O的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】废水废气对自然环境有严重的破坏作用,大气和水污染治理刻不容缓。
(1)某化工厂产生的废水中含有Fe2+、Mn2+等金属离子,可用过硫酸铵[(NH4)2S2O8]氧化除去。
①过硫酸铵与Mn2+反应生成MnO2的离子方程式为_____ 。
②温度与Fe2+、Mn2+氧化程度之间的关系如图所示:

实验过程中应将温度控制在_____ 。Fe2+与Mn2+被氧化后形成胶体絮状粒子,常加入活性炭处理,加入活性炭的目的为_____ 。
③H2O2也有较强氧化性,在实际生产中不用H2O2氧化Mn2+的原因是_____ 。
(2)利用某分子筛作催化剂,NH3可脱除废气中NO、NO2,其反应机理如图所示。A包含物质的化学式为N2和_____ 。

(3)工业上废气中SO2可用Na2CO3溶液吸收,反应过程中溶液组成变化如图所示。
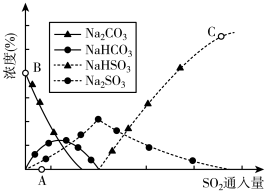
①吸收初期(图中A点以前)反应的化学方程式为_____ 。
②C点高于B点的原因是_______
(1)某化工厂产生的废水中含有Fe2+、Mn2+等金属离子,可用过硫酸铵[(NH4)2S2O8]氧化除去。
①过硫酸铵与Mn2+反应生成MnO2的离子方程式为
②温度与Fe2+、Mn2+氧化程度之间的关系如图所示:

实验过程中应将温度控制在
③H2O2也有较强氧化性,在实际生产中不用H2O2氧化Mn2+的原因是
(2)利用某分子筛作催化剂,NH3可脱除废气中NO、NO2,其反应机理如图所示。A包含物质的化学式为N2和

(3)工业上废气中SO2可用Na2CO3溶液吸收,反应过程中溶液组成变化如图所示。

①吸收初期(图中A点以前)反应的化学方程式为
②C点高于B点的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】向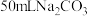 和
和 混合溶液中缓慢滴加一定浓度的盐酸,测得溶液中
混合溶液中缓慢滴加一定浓度的盐酸,测得溶液中 物质的量与所加盐酸体积之间的关系如图所示。
物质的量与所加盐酸体积之间的关系如图所示。
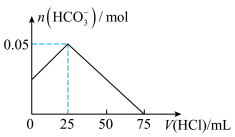
请回答下列问题:
(1)加盐酸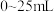 过程中发生反应的离子方程式为:
过程中发生反应的离子方程式为:___________ 。
(2)盐酸物质的量浓度为___________  ,原混合溶液中
,原混合溶液中 的物质的量浓度为
的物质的量浓度为___________  。
。
(3)当滴入的盐酸体积为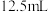 时,溶液中
时,溶液中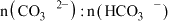 为
为___________ 。
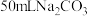 和
和 混合溶液中缓慢滴加一定浓度的盐酸,测得溶液中
混合溶液中缓慢滴加一定浓度的盐酸,测得溶液中 物质的量与所加盐酸体积之间的关系如图所示。
物质的量与所加盐酸体积之间的关系如图所示。
请回答下列问题:
(1)加盐酸
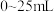 过程中发生反应的离子方程式为:
过程中发生反应的离子方程式为:(2)盐酸物质的量浓度为
 ,原混合溶液中
,原混合溶液中 的物质的量浓度为
的物质的量浓度为 。
。(3)当滴入的盐酸体积为
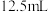 时,溶液中
时,溶液中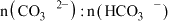 为
为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有一份 溶液,向其中通入一定量
溶液,向其中通入一定量 ,得到一份混合溶液,为测定溶液的成分,某小组同学做了以下实验:
,得到一份混合溶液,为测定溶液的成分,某小组同学做了以下实验:
Ⅰ.配制 的标准盐酸
的标准盐酸
实验室现有密度为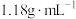 ,质量分数为36.5%的浓盐酸,若要配制
,质量分数为36.5%的浓盐酸,若要配制 标准盐酸,据此回答下列问题:
标准盐酸,据此回答下列问题:
(1)该浓盐酸的物质的量浓度为_____  ;应选用的容量瓶的规格为
;应选用的容量瓶的规格为_____ 。
(2)在配制稀盐酸溶液时,有如下操作,正确的操作顺序是_____ 。
A.用量筒量取浓盐酸注入烧杯中,再向烧杯中加入少量蒸馏水,慢慢搅动,使其混合均匀
B.用蒸馏水洗涤烧杯内壁及玻璃棒仪器各2~3次,将洗涤液全部注入容量瓶中,轻轻摇动容量瓶
C.盖好瓶塞,反复上下颠倒摇匀
D.将已恢复至室温的盐酸转移注入所选用的容量瓶中
E.用胶头滴管滴加蒸馏水,使溶液的凹液面恰好与容量瓶上的刻度线相切
F.继续往容量瓶中加蒸馏水,直到液面接近瓶颈上的刻度线1~2cm处
(3)若是定容时俯视容量瓶瓶颈上的刻度线会使所配制的溶液浓度_____ (填“偏低”“偏高”“无影响”,下同);容量瓶用蒸馏水洗净后,没烘干直接使用对实验的结果_____ 。
Ⅱ、测定混合溶液成分
向混合溶液中滴入上述配制的稀盐酸,滴入盐酸体积与产生气体体积(标准状况)如图所示:
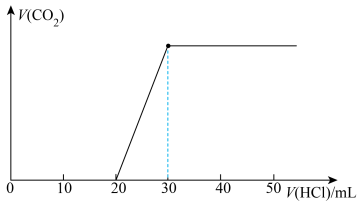
(4)混合溶液的溶质为_____ (填化学式)。
(5)原 溶液的物质的量浓度为
溶液的物质的量浓度为_____ 。
 溶液,向其中通入一定量
溶液,向其中通入一定量 ,得到一份混合溶液,为测定溶液的成分,某小组同学做了以下实验:
,得到一份混合溶液,为测定溶液的成分,某小组同学做了以下实验:Ⅰ.配制
 的标准盐酸
的标准盐酸实验室现有密度为
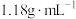 ,质量分数为36.5%的浓盐酸,若要配制
,质量分数为36.5%的浓盐酸,若要配制 标准盐酸,据此回答下列问题:
标准盐酸,据此回答下列问题:(1)该浓盐酸的物质的量浓度为
 ;应选用的容量瓶的规格为
;应选用的容量瓶的规格为(2)在配制稀盐酸溶液时,有如下操作,正确的操作顺序是
A.用量筒量取浓盐酸注入烧杯中,再向烧杯中加入少量蒸馏水,慢慢搅动,使其混合均匀
B.用蒸馏水洗涤烧杯内壁及玻璃棒仪器各2~3次,将洗涤液全部注入容量瓶中,轻轻摇动容量瓶
C.盖好瓶塞,反复上下颠倒摇匀
D.将已恢复至室温的盐酸转移注入所选用的容量瓶中
E.用胶头滴管滴加蒸馏水,使溶液的凹液面恰好与容量瓶上的刻度线相切
F.继续往容量瓶中加蒸馏水,直到液面接近瓶颈上的刻度线1~2cm处
(3)若是定容时俯视容量瓶瓶颈上的刻度线会使所配制的溶液浓度
Ⅱ、测定混合溶液成分
向混合溶液中滴入上述配制的稀盐酸,滴入盐酸体积与产生气体体积(标准状况)如图所示:

(4)混合溶液的溶质为
(5)原
 溶液的物质的量浓度为
溶液的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求完成下列填空:
(1)某金属氯化物 的摩尔质量为
的摩尔质量为 ,取该金属氯化物
,取该金属氯化物 配成水溶液,与足量
配成水溶液,与足量 溶液完全反应,生成
溶液完全反应,生成 白色沉淀。则金属M的摩尔质量为
白色沉淀。则金属M的摩尔质量为___________ g/mol
(2)一定量的液态化合物 ,在一定量
,在一定量 中恰好完全反应:
中恰好完全反应: (注:l表示液态,g表示气态),冷却后在标准状况下,测得生成物的体积为
(注:l表示液态,g表示气态),冷却后在标准状况下,测得生成物的体积为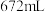 ,则反应前
,则反应前 的体积是
的体积是___________ mL,反应结束后,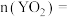
___________ mol
(3) 某物质的量浓度的
某物质的量浓度的 溶液中缓慢通入一定量的
溶液中缓慢通入一定量的 充分反应,再向上述所得溶液中逐滴滴加
充分反应,再向上述所得溶液中逐滴滴加 的盐酸,(忽略液体混合带来的体积变化)所得气体的体积与所加盐酸的体积关系如图所示:
的盐酸,(忽略液体混合带来的体积变化)所得气体的体积与所加盐酸的体积关系如图所示:
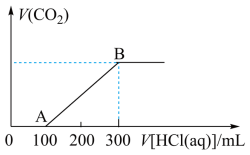
①OA段、AB段发生反应的化学方程式___________ 、___________ 。
②B点时,反应所得溶液中溶质的物质的量浓度是___________ mol/L
(1)某金属氯化物
 的摩尔质量为
的摩尔质量为 ,取该金属氯化物
,取该金属氯化物 配成水溶液,与足量
配成水溶液,与足量 溶液完全反应,生成
溶液完全反应,生成 白色沉淀。则金属M的摩尔质量为
白色沉淀。则金属M的摩尔质量为(2)一定量的液态化合物
 ,在一定量
,在一定量 中恰好完全反应:
中恰好完全反应: (注:l表示液态,g表示气态),冷却后在标准状况下,测得生成物的体积为
(注:l表示液态,g表示气态),冷却后在标准状况下,测得生成物的体积为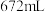 ,则反应前
,则反应前 的体积是
的体积是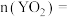
(3)
 某物质的量浓度的
某物质的量浓度的 溶液中缓慢通入一定量的
溶液中缓慢通入一定量的 充分反应,再向上述所得溶液中逐滴滴加
充分反应,再向上述所得溶液中逐滴滴加 的盐酸,(忽略液体混合带来的体积变化)所得气体的体积与所加盐酸的体积关系如图所示:
的盐酸,(忽略液体混合带来的体积变化)所得气体的体积与所加盐酸的体积关系如图所示:
①OA段、AB段发生反应的化学方程式
②B点时,反应所得溶液中溶质的物质的量浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】向盛有一定量烧碱溶液的烧杯中通入一定量的CO2 气体后,再向所得溶液中逐滴加入盐酸至过量,产生的 CO2 气体与加入 HCl 的物质的量的关系如下图所示(忽略 CO2 的溶解和 HCl的挥发):

请问图中O点对应溶液的溶质为_____ (填化学式),其物质的量之比为_____ 。开始产生 CO2 气体时对应的离子方程式为_____ 。

请问图中O点对应溶液的溶质为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】将一定量的NaOH和Na2CO3混合并配成溶液,向溶液中滴加0.1mol•L−1稀盐酸。加入盐酸的体积和生成CO2的物质的量的关系如图所示,请回答下列问题:
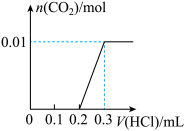
(1)该实验需要配制450mL、0.1mol•L−1的稀盐酸。除了需要用到量筒、烧杯、胶头滴管之外,还需要用到的玻璃仪器是___ 。
(2)若用浓度为10mol•L-1的盐酸来配制0.1mol•L-1稀盐酸,需要量取该盐酸___ mL。
(3)据图所示,当加入盐酸体积0.2~0.3L时的离子方程式为___ 。
(4)根据已知数据可知混合溶液中NaOH的物质的量为___ mol。

(1)该实验需要配制450mL、0.1mol•L−1的稀盐酸。除了需要用到量筒、烧杯、胶头滴管之外,还需要用到的玻璃仪器是
(2)若用浓度为10mol•L-1的盐酸来配制0.1mol•L-1稀盐酸,需要量取该盐酸
(3)据图所示,当加入盐酸体积0.2~0.3L时的离子方程式为
(4)根据已知数据可知混合溶液中NaOH的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】把由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量的水中,有1.16g白色沉淀析出,向所得的浊液里,逐渐加入0.5mol/L的盐酸,加入盐酸的体积和生成沉淀的质量如图所示:

(1)写出mn段反应的离子方程式_______________________
(2)混合物中NaOH的物质的量是_______________ ,AlCl3的物质的量是________________ ,MgCl2的物质的量是______________ 。
(3)P点所表示的加入盐酸的体积是_______________ mL。

(1)写出mn段反应的离子方程式
(2)混合物中NaOH的物质的量是
(3)P点所表示的加入盐酸的体积是
您最近一年使用:0次



