W、X、Y、Z是原子序数依次递增的短周期主族元素,X和Y组成的某二元化合物是生产普通玻璃所需主要原料之一,Z的K层电子数与最外层电子数之和等于次外层电子数,WX2和W2X4中的化合价相同,且二者可以互相转换。下列有关说法中正确的是
| A.YX2是酸性氧化物,与酸不反应 |
| B.原子半径Y>Z>X |
| C.简单氢化物的稳定性W>X |
| D.氢元素与W、X形成的化合物一定是共价化合物 |
更新时间:2019-02-20 17:17:23
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列关于元素周期表和元素周期律的说法不正确 的是
| A.电子层数相同的原子一定为同一周期 |
| B.最外层电子数相同的原子一定为同一族 |
| C.第ⅦA族从氟到碘,单质的熔沸点依次增大 |
| D.同周期元素从左到右金属性逐渐减弱,非金属性逐渐增强(稀有气体元素除外) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据元素周期律和周期表,下列各项叙述正确的组合是
①同一主族元素,原子半径越大,非金属单质的熔点一定越高;②同一周期元素的原子(除稀有气体),半径越大越容易失去电子;③若R2—和M+的电子层结构相同,则微粒半径:M+>R2—;④原子半径X小于Y的同一主族的两种元素,若X(OH)n是强碱,则Y(OH)n也是强碱;⑤除第一周期外,第n周期的最后一种金属元素位于第n主族
①同一主族元素,原子半径越大,非金属单质的熔点一定越高;②同一周期元素的原子(除稀有气体),半径越大越容易失去电子;③若R2—和M+的电子层结构相同,则微粒半径:M+>R2—;④原子半径X小于Y的同一主族的两种元素,若X(OH)n是强碱,则Y(OH)n也是强碱;⑤除第一周期外,第n周期的最后一种金属元素位于第n主族
| A.①②④ | B.①③⑤ | C.②③④ | D.②④⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列 10 句话,其中表述正确的个数是
①C4H9Cl有4种同分异构体 ②甲烷和氯气光照条件下可制得纯净的一氯甲烷 ③糖、蛋白质、油脂在一定条件下都能水解 ④乙醇、乙酸、乙酸乙酯都能发生取代反应 ⑤ 除去甲烷中含有的乙烯气体,可将混合气体通入装有酸性高锰酸钾溶液的洗气瓶中,再干燥 ⑥用铁片和稀硫酸反应制取氢气时,改用 98%的浓硫酸可加快产生氢气的速率 ⑦100mL2mol/L 的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 ⑧在氧气中完全燃烧后生成物只有CO2和H2O的有机物一定是烃 ⑨CH2Cl2没有同分异构体的事实证明了甲烷分子是以碳原子为中心的正四面体结构 ⑩ⅦA 族元素的阴离子还原性越强,其氢化物的熔沸点越高
①C4H9Cl有4种同分异构体 ②甲烷和氯气光照条件下可制得纯净的一氯甲烷 ③糖、蛋白质、油脂在一定条件下都能水解 ④乙醇、乙酸、乙酸乙酯都能发生取代反应 ⑤ 除去甲烷中含有的乙烯气体,可将混合气体通入装有酸性高锰酸钾溶液的洗气瓶中,再干燥 ⑥用铁片和稀硫酸反应制取氢气时,改用 98%的浓硫酸可加快产生氢气的速率 ⑦100mL2mol/L 的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 ⑧在氧气中完全燃烧后生成物只有CO2和H2O的有机物一定是烃 ⑨CH2Cl2没有同分异构体的事实证明了甲烷分子是以碳原子为中心的正四面体结构 ⑩ⅦA 族元素的阴离子还原性越强,其氢化物的熔沸点越高
| A.5 个 | B.4个 | C.3 个 | D.2 个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中T所处的周期序数与主族序数相等,下列说法正确的是
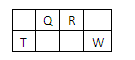

| A.W在周期表中的位置是第三周期,ⅤA族 |
| B.原子半径Q>R>T |
| C.W原子得电子能力强于Q原子,且可形成共价化合物QW2 |
| D.原子序数比R多1的元素只有一种氢化物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】根据元素周期表和元素周期律,判断下列叙述不正确的是
| A.气态氢化物的稳定性:H2O>NH3>SiH4 |
| B.氢元素与其他元素可形成共价化合物或离子化合物 |
C.如图所示实验可证明元素的非金属性:Cl>C>Si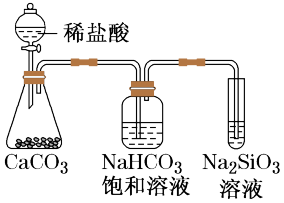 |
D.用中文“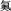 ”(ào)命名的第118号元素在周期表中位于第七周期0族 ”(ào)命名的第118号元素在周期表中位于第七周期0族 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列各项中,理由、结论及因果关系均正确的是

| 选项 | 理由 | 结论 |
| A | 共价键强弱: | 沸点: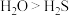 |
| B | 元素的非金属性: | 酸性: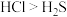 |
| C | 相同外界条件下反应速率:a反应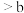 反应 反应 | 活化能:b反应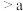 反应 反应 |
| D | 还原性: | 氧化性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】利用如图所示的装置和下列试剂能同时探究同周期和同主族元素性质递变规律的是
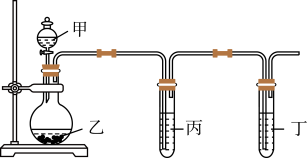

| 选项 | 甲 | 乙 | 丙 | 丁 |
| A | 盐酸 | 碳酸钙 | 饱和NaHCO3溶液 | Na2SiO3溶液 |
| B | 浓盐酸 | 高锰酸钾 | 饱和食盐水 | Na2S溶液 |
| C | 硝酸 | 碳酸钙 | 饱和NaHCO3溶液 | 澄清石灰水 |
| D | 硝酸 | 碳酸钙 | 饱和NaHCO3溶液 | Na2SiO3溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】如图为元素周期表中短周期元素的一部分,下列说法中正确的是
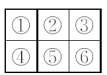

A.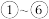 不可能出现金属元素 不可能出现金属元素 |
B.气态氢化物的热稳定性: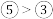 |
| C.六种元素中,③的最高价氧化物对应的水化物的酸性一定最强 |
| D.六种元素,相互结合形成的二元化合物一定都是共价化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 检验 溶液是否变质 溶液是否变质 | 取少量溶液于试管中,加入盐酸酸化的硝酸钡溶液 | 若产生白色沉淀,则说明已经变质 |
| B | 检验有机物 中的官能团 中的官能团 | 取少量该有机物于试管1中,加入新制氢氧化铜,加热;另取少量溴水于试管2中,滴加该有机物 | 若试管1产生砖红色沉淀,则证明有醛基;若试管2中溴水褪色,则证明存在碳碳双键 |
| C | 探究浓度对反应速率的影响 | 两支试管中均装有2ml0.01mol/L酸性高锰酸钾溶液,向第一支试管中加入2ml0.01mol/L的草酸溶液和3ml蒸馏水,第二支试管中加入5ml0.01mol/L的草酸溶液 | 第一支试管褪色时间比第二支试管长。说明其他条件相同时,反应物浓度越大反应速率越快 |
| D | 判断化合物组成中的化学键类型 | 将熔融状态下的HCl和NaCl进行导电性实验 | 不能导电的HCl由共价键形成;能导电的NaCl则由离子键形成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 与
与 溶液能发生置换反应
溶液能发生置换反应
 的原子序数依次增大。W是碱金属元素中原子半径最小的元素,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的元素,Z原子的最外层电子数是其电子层数的2倍。下列说法错误的是
的原子序数依次增大。W是碱金属元素中原子半径最小的元素,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的元素,Z原子的最外层电子数是其电子层数的2倍。下列说法错误的是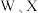 的氯化物中,各原子最外层均满足8电子的稳定结构
的氯化物中,各原子最外层均满足8电子的稳定结构


