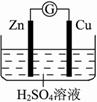
天然气是一种清洁能源,用途广泛。
(1)工业上可用焦炉煤气(主要成分为CO、CO2和H2)制备天然气。已知:CO(g)+3H2(g)=CH4(g) +H2O(g) △H1=-206kJ/mol,CO(g)+H2O(g)=H2(g)+CO2(g) △H2= -41kJ/mol。
①CO2转化为CH4的热化学方程式是:_______ 。
②有利于提高混合气中CH4含量的措施是:_______ 。
a. 使用催化剂 b. 升高温度 c. 及时导出水蒸气
(2)甲烷可制成燃料电池,其装置如下图所示。
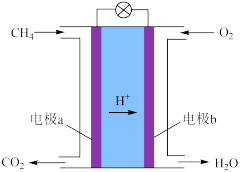
①电极b是_______ 极(填“正”或“负”)。
②a极的电极反应式是_______________ 。
(1)工业上可用焦炉煤气(主要成分为CO、CO2和H2)制备天然气。已知:CO(g)+3H2(g)=CH4(g) +H2O(g) △H1=-206kJ/mol,CO(g)+H2O(g)=H2(g)+CO2(g) △H2= -41kJ/mol。
①CO2转化为CH4的热化学方程式是:
②有利于提高混合气中CH4含量的措施是:
a. 使用催化剂 b. 升高温度 c. 及时导出水蒸气
(2)甲烷可制成燃料电池,其装置如下图所示。

①电极b是
②a极的电极反应式是
更新时间:2019-03-03 22:49:48
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】根据已知信息,按要求写出指定反应的热化学方程式
(1)LiH可作飞船的燃料,已知下列反应:
①2Li(s)+H2(g)=2LiH(s) ΔH=-182kJ·mol-1
②2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ·mol-1
③4Li(s)+O2(g)=2Li2O(s) ΔH=-1196kJ·mol-1
试写出LiH在O2中燃烧的热化学方程式:____________ 。
(2)工业上制取硝酸铵的流程图如下所示:
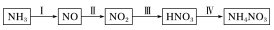
已知:4NO(g)+4NH3(g)+O2(g)⇌4N2(g)+6H2O(g) ΔH=-1745.2kJ·mol-1;
6NO(g)+4NH3(g)⇌5N2(g)+6H2O(g) ΔH=-1925.2kJ·mol-1。
则反应I的热化学方程式可表示为_______ 。
(3)饮用水中的 主要来自于
主要来自于 。已知在微生物的作用下,
。已知在微生物的作用下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
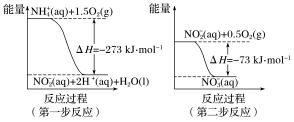
1mol 全部被氧化成
全部被氧化成 的热化学方程式为
的热化学方程式为_______ 。
(1)LiH可作飞船的燃料,已知下列反应:
①2Li(s)+H2(g)=2LiH(s) ΔH=-182kJ·mol-1
②2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ·mol-1
③4Li(s)+O2(g)=2Li2O(s) ΔH=-1196kJ·mol-1
试写出LiH在O2中燃烧的热化学方程式:
(2)工业上制取硝酸铵的流程图如下所示:

已知:4NO(g)+4NH3(g)+O2(g)⇌4N2(g)+6H2O(g) ΔH=-1745.2kJ·mol-1;
6NO(g)+4NH3(g)⇌5N2(g)+6H2O(g) ΔH=-1925.2kJ·mol-1。
则反应I的热化学方程式可表示为
(3)饮用水中的
 主要来自于
主要来自于 。已知在微生物的作用下,
。已知在微生物的作用下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
1mol
 全部被氧化成
全部被氧化成 的热化学方程式为
的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:
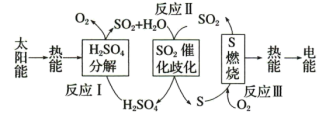
反应Ⅰ: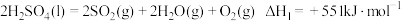
反应Ⅲ:
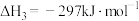
反应Ⅱ的热化学方程式:_______ 。

反应Ⅰ:
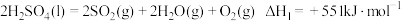
反应Ⅲ:

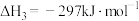
反应Ⅱ的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g) CH3OH(g) ΔH1
CH3OH(g) ΔH1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH2
CH3OH(g)+H2O(g) ΔH2
③CO2(g)+H2(g) CO(g)+H2O(g) ΔH3
CO(g)+H2O(g) ΔH3
(1)回答下列问题:已知反应①中相关的化学键键能数据如下:
由此计算ΔH1=______ kJ·mol-1;已知ΔH2=-58 kJ·mol-1,则ΔH3=_______ kJ·mol-1。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1 275.6 kJ·mol-1
②H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
写出表示甲醇燃烧热的热化学方程式_________________ 。
(3)已知常温时红磷比白磷稳定,已知:
①P4(白磷,s)+5O2(g)=2P2O5(s)ΔH1
②4P(红磷,s)+5O2(g)=2P2O5(s)ΔH2
比较反应中ΔH的大小:ΔH1_______ ΔH2(填“>”、“<”或“=”)。
(4)已知:稀溶液中,H+(aq)+OH﹣(aq)===H2O(l)ΔH=﹣57.3 kJ•mol-1,则浓硫酸与稀氢氧化钠溶液反应生成1 mol水,放出的热量_____ 57.3 kJ(填“>”、“<”或“=”)。
①CO(g)+2H2(g)
 CH3OH(g) ΔH1
CH3OH(g) ΔH1②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH2
CH3OH(g)+H2O(g) ΔH2③CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH3
CO(g)+H2O(g) ΔH3(1)回答下列问题:已知反应①中相关的化学键键能数据如下:
| 化学键 | H—H | C—O | C≡O | H—O | C—H |
| E/(kJ·mol-1) | 436 | 343 | 1 076 | 465 | 413 |
由此计算ΔH1=
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1 275.6 kJ·mol-1
②H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
写出表示甲醇燃烧热的热化学方程式
(3)已知常温时红磷比白磷稳定,已知:
①P4(白磷,s)+5O2(g)=2P2O5(s)ΔH1
②4P(红磷,s)+5O2(g)=2P2O5(s)ΔH2
比较反应中ΔH的大小:ΔH1
(4)已知:稀溶液中,H+(aq)+OH﹣(aq)===H2O(l)ΔH=﹣57.3 kJ•mol-1,则浓硫酸与稀氢氧化钠溶液反应生成1 mol水,放出的热量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】分别按下图A、B、C所示装置进行实验,图中三个烧杯里的溶液为同浓度的稀硫酸。请回答下列问题:
(1)以下叙述中,正确的是__________
A.B中铁片是负极,C中铁片是正极
B.三个烧杯中铁片表面均有气泡产生
C.A、B两烧杯中溶液的pH均增大
D.产生气泡的速率A中比B中慢
E.B溶液中SO42-向Sn电极移动
(2)装置B变化过程中能量转化的形式主要是:____________ 。
(3)有同学想把Ba(OH)2·8H2O晶体与NH4Cl晶体的反应设计成原电池,你认为是否可行?__________ (填“是”或“否”),理由是__________ .
(4)A、B、C三个烧杯中铁的腐蚀速率________ >_______ >______
(5)对于反应2A2+B2=2A2B,已知A2、B2、A2B的键能如下表:
右图能正确表示该反应过程中能量变化的选项是_______ 。
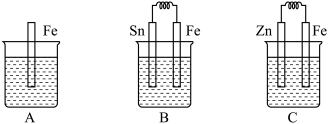
(1)以下叙述中,正确的是
A.B中铁片是负极,C中铁片是正极
B.三个烧杯中铁片表面均有气泡产生
C.A、B两烧杯中溶液的pH均增大
D.产生气泡的速率A中比B中慢
E.B溶液中SO42-向Sn电极移动
(2)装置B变化过程中能量转化的形式主要是:
(3)有同学想把Ba(OH)2·8H2O晶体与NH4Cl晶体的反应设计成原电池,你认为是否可行?
(4)A、B、C三个烧杯中铁的腐蚀速率
(5)对于反应2A2+B2=2A2B,已知A2、B2、A2B的键能如下表:
| 化学键 | A-A | B=B | A-B |
| 键能KJ/mol | 236 | 406 | 163 |
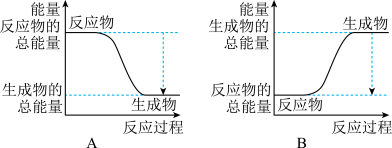
右图能正确表示该反应过程中能量变化的选项是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】将铁片、铜片通过导线相连,置于稀硫酸中,构成原电池。
(1)该原电池的负极是______ (填“铁片”或“铜片”),其电极反应式______ ;
(2)正极产生的现象是______ ,其发生的反应的类型是______ 反应;(填“氧化”或“还原”)
(3)若导线中通过了0.4mol电子,负极材料的质量理论上减少______ 克。
(1)该原电池的负极是
(2)正极产生的现象是
(3)若导线中通过了0.4mol电子,负极材料的质量理论上减少
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
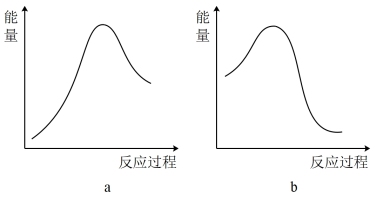
(1)从化学键的角度分析化学反应中能量变化的实质如图所示。回答下列问题:
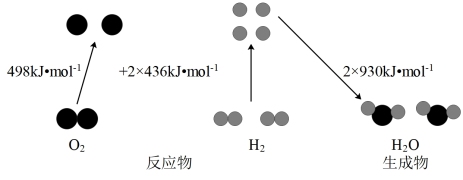
①氢气燃烧生成2molH2O(g)时,应____ (填“释放”或“吸收”)____ kJ能量。
②上述反应的能量变化可用图____ (填“a”或“b”)表示。
(2)燃料电池是将燃料具有的化学能直接变为电能的发电装置。甲烷(CH4)燃料电池的工作原理如图所示,回答下列问题:
①a电极为____ (填“正”或“负”)极,电极反应式为____ 。
②电池工作时H+移向____ (填“a”或“b”)极,当消耗标准状况下11.2LO2时,通过电流表电子的物质的量为____ 。
(1)从化学键的角度分析化学反应中能量变化的实质如图所示。回答下列问题:

①氢气燃烧生成2molH2O(g)时,应
②上述反应的能量变化可用图

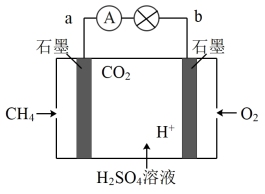
(2)燃料电池是将燃料具有的化学能直接变为电能的发电装置。甲烷(CH4)燃料电池的工作原理如图所示,回答下列问题:

①a电极为
②电池工作时H+移向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
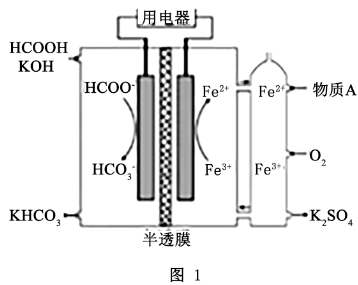
【推荐2】(1) ①如图1所示的HCOOH燃料电池放电的本质是通过HCOOH与 的反应,将化学能转化为电能,其反应的离子方程式为
的反应,将化学能转化为电能,其反应的离子方程式为___________ 。
②两电极区间用允许 、
、 通过的半透膜隔开。电池负极电极反应式为
通过的半透膜隔开。电池负极电极反应式为___________ ;
(2)电解熔融 Al2O3,电解过程中作阳极的石墨易消耗,原因是___________ 。
(3)电解Na2CO3溶液,原理如图所示。
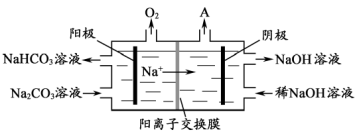
阳极的电极反应式为___________ ,
(4) 与盐酸、氧气构成燃料电池,则燃料电池的负极反应式为
与盐酸、氧气构成燃料电池,则燃料电池的负极反应式为 ___________ 。
 的反应,将化学能转化为电能,其反应的离子方程式为
的反应,将化学能转化为电能,其反应的离子方程式为②两电极区间用允许
 、
、 通过的半透膜隔开。电池负极电极反应式为
通过的半透膜隔开。电池负极电极反应式为
(2)电解熔融 Al2O3,电解过程中作阳极的石墨易消耗,原因是
(3)电解Na2CO3溶液,原理如图所示。

阳极的电极反应式为
(4)
 与盐酸、氧气构成燃料电池,则燃料电池的负极反应式为
与盐酸、氧气构成燃料电池,则燃料电池的负极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图所示组成闭合回路,其中,甲装置中CH4为负极,O2和CO2的混合气体为正极,稀土金属材料为电极,以熔融碳酸盐为电解质;乙装置中a、b为石墨,b极上有红色物质析出,CuSO4溶液的体积为200mL。
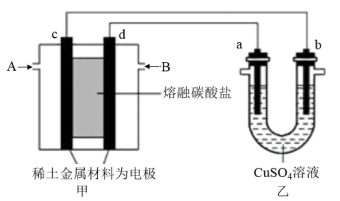
①装置中气体A为_______ (填“CH4”或“O2和CO2”),d极上的电极反应式为 _______ 。
②乙装置中a极上的电极反应式为_______ 。若在a极产生112mL(标准状况)气体,则甲装置中消耗CH4_______ mL(标准状况),乙装置中所得溶液的pH如何变化 _______ (变大、变小、不变)。

①装置中气体A为
②乙装置中a极上的电极反应式为
您最近一年使用:0次