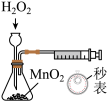
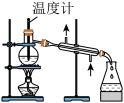
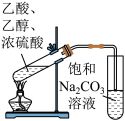
探究2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+10CO2↑+8H2O反应速率的影响因素,有关实验数据如下表所示:下列说法不正确的是( )
| 实验编号 | 温度 | 催化剂用量(g) | 酸性KMnO4溶液 | H2C2O4溶液 | KMnO4溶液褪色平均时间 min | ||
| 体积(mL) | 浓度mol·L-1 | 体积(mL) | 浓度 mol·L-1 | ||||
| 1 | 25 | 0.5 | 4 | 0.1 | 8 | 0.2 | 12.7 |
| 2 | 80 | 0.5 | 4 | 0.1 | 8 | 0.2 | a |
| 3 | 25 | 0.5 | 4 | 0.01 | 8 | 0.2 | 6.7 |
| 4 | 25 | 0 | 4 | 0.01 | 8 | 0.2 | b |
| A.a<12.7,b>6.7 |
| B.用KMnO4表示该反应速率,v(实验3)<v(实验1) |
| C.用H2C2O4表示该反应速率,v(实验1)约为7.87×10-5 mol·L-1·min-1 |
| D.可通过比较收集相同体积CO2所消耗的时间来判断反应速率快慢 |
18-19高三下·河南许昌·阶段练习 查看更多[2]
更新时间:2019-03-05 17:32:28
|
相似题推荐
单选题
|
适中
(0.65)
名校
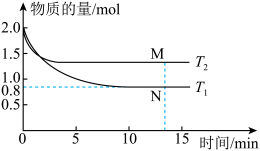
【推荐1】碳单质可应用于脱硝。向容积为1L的密闭容器中加入炭(足量)和NO,模拟发生脱硝反应:C(s)+2NO(g)  N2(g)+CO2(g),测得不同温度下,NO的物质的量随时间的变化如下图所示,下列有关说法不正确的是
N2(g)+CO2(g),测得不同温度下,NO的物质的量随时间的变化如下图所示,下列有关说法不正确的是
 N2(g)+CO2(g),测得不同温度下,NO的物质的量随时间的变化如下图所示,下列有关说法不正确的是
N2(g)+CO2(g),测得不同温度下,NO的物质的量随时间的变化如下图所示,下列有关说法不正确的是
| A.该反应ΔH<0 |
| B.正反应速率:M>N |
| C.T1时,若起始向容器中充入N2(g)和CO2(g)各2mol,平衡时,NO的体积分数为40% |
| D.T1时,0~15min时的反应速率v(CO2)=0.08mol·L-1·min-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某合成氨速率方程为: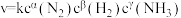 (k为速率常数),部分数据如下表。下列说法正确的是
(k为速率常数),部分数据如下表。下列说法正确的是
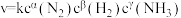 (k为速率常数),部分数据如下表。下列说法正确的是
(k为速率常数),部分数据如下表。下列说法正确的是| 实验 | 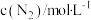 | 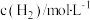 |  |  |
| 1 | m | n | p | q |
| 2 | 2m | n | p | 2q |
| 3 | m | n | 0.1p | 10q |
| 4 | m | 2n | p | 2.828q |
| A.k与物质性质有关,与反应温度、压强、反应物浓度无关 |
| B.α=1,γ= -1 |
| C.恒容容器中反应时,充He气,压强增大反应速率加快 |
| D.采用适当催化剂,反应活化能、焓变均减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】体积均为1L的两个恒容密闭容器I、Ⅱ中,均充入2mol 和2mol
和2mol ,发生反应:
,发生反应:
 ,相对容器Ⅱ,容器I只改变一个外界条件,测得N2的物质的量与时间关系如图所示。下列叙述正确的是
,相对容器Ⅱ,容器I只改变一个外界条件,测得N2的物质的量与时间关系如图所示。下列叙述正确的是
 和2mol
和2mol ,发生反应:
,发生反应:
 ,相对容器Ⅱ,容器I只改变一个外界条件,测得N2的物质的量与时间关系如图所示。下列叙述正确的是
,相对容器Ⅱ,容器I只改变一个外界条件,测得N2的物质的量与时间关系如图所示。下列叙述正确的是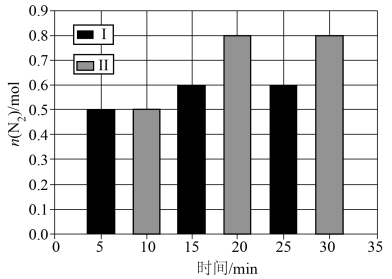
| A.容器I改变的条件可能是使用了催化剂 |
| B.相对容器Ⅱ,容器I改变的条件可能是加压或者升温 |
| C.容器Ⅱ中NO的平衡转化率为80% |
D.容器Ⅱ中0~10min内, |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】某温度时,浓度都是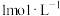 的两种气体
的两种气体 和
和 ,在密闭容器中发生可逆反应生成气体Z,充分反应后
,在密闭容器中发生可逆反应生成气体Z,充分反应后 的浓度为
的浓度为 ,
, 的浓度为
的浓度为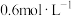 ,生成的Z的浓度为
,生成的Z的浓度为 ,则该反应的化学方程式(Z用X、Y表示)是
,则该反应的化学方程式(Z用X、Y表示)是
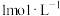 的两种气体
的两种气体 和
和 ,在密闭容器中发生可逆反应生成气体Z,充分反应后
,在密闭容器中发生可逆反应生成气体Z,充分反应后 的浓度为
的浓度为 ,
, 的浓度为
的浓度为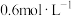 ,生成的Z的浓度为
,生成的Z的浓度为 ,则该反应的化学方程式(Z用X、Y表示)是
,则该反应的化学方程式(Z用X、Y表示)是A.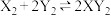 | B.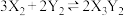 |
C. | D.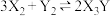 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用纯净的CaCO3与100mL稀盐酸反应制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况下的体积)。下列分析正确的是
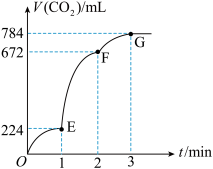

| A.EF段,用盐酸表示该反应的平均反应速率为0.4mol·(L·min)−1 |
| B.OE段表示的平均速率最快 |
| C.F点收集到的CO2的量最多 |
| D.OE、EF、FG三段中,该反应用二氧化碳表示的平均反应速率之比为2∶6∶7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。下列说法不正确的是


| A.图甲可通过观察气泡产生快慢来比较反应速率的大小 |
| B.图甲所示实验中,若左边试管里的反应速率大于右边的,则证明Fe3+对H2O2分解的催化效果比Cu2+的好 |
| C.用图乙装置测定反应速率,可测定反应产生的气体体积及反应时间 |
| D.为检查乙装置的气密性,可关闭a处旋塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验不能达到相应实验目的的是
| 操作及现象 | 实验目的 | |
| A | 向5 mL 0.005 mol/L FeCl3溶液中加入5 mL 0.1mol/L KSCN溶液,充分反应后,再滴加4滴饱和FeCl3溶液,充分振荡,溶液红色加深 | 探究浓度对平衡移动的影响 |
| B | 分别向装有2 mL 0.1 mol/L H2C2O4溶液和2 mL 0.2 mol/L H2C2O4溶液的两支试管中加入4 mL 0.01mol/L酸性KMnO4溶液,振荡,后者溶液先褪色 | 探究浓度对反应速率的影响 |
| C | 将研细后的20 g Ba(OH)2·8H2O晶体与10 g NH4Cl晶体一起放入烧杯中,用玻璃棒快速搅拌,闻到刺激性气味的气体,烧杯壁温度下降 | 证明Ba(OH)2·8H2O晶体与NH4Cl晶体的反应是吸热反应 |
| D | 将50 mL 0.55 mol/L 的烧碱溶液分多次加入到盛有50 mL 0.5 mol/L 盐酸的量热计中,温度计示数由T1升高至T2 | 测定并计算中和热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关化学反应速率的说法中,正确的是
| A.100 mL 1 mol/L的稀硫酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变 |
| B.合成氨的反应是一个放热反应,所以升高温度,反应速率减慢 |
| C.用铁片和 |
| D.汽车尾气中的CO和NO可以缓慢反应生成N2和CO2,减小压强,反应速率减慢 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】把下列四种 溶液分别加入四只均盛有20mL3mol/L稀硫酸的烧杯中(稀硫酸的初始温度相同),然后均加入蒸馏水稀释到60mL,溶液中最先出现浑浊的是
溶液分别加入四只均盛有20mL3mol/L稀硫酸的烧杯中(稀硫酸的初始温度相同),然后均加入蒸馏水稀释到60mL,溶液中最先出现浑浊的是
 溶液分别加入四只均盛有20mL3mol/L稀硫酸的烧杯中(稀硫酸的初始温度相同),然后均加入蒸馏水稀释到60mL,溶液中最先出现浑浊的是
溶液分别加入四只均盛有20mL3mol/L稀硫酸的烧杯中(稀硫酸的初始温度相同),然后均加入蒸馏水稀释到60mL,溶液中最先出现浑浊的是A.20℃,10mL,5mol/L的 溶液 溶液 |
B.20℃,20mL,3mol/L的 溶液 溶液 |
C.30℃,10mL,4mol/L的 溶液 溶液 |
D.30℃,30mL,2mol/L的 溶液 溶液 |
您最近一年使用:0次

 pC(g)+qD(g),经过5 min达到平衡,此时各物质的变化为A物质的量浓度减少amol·L-1,B的平均反应速率v(B)=a/15 mol·L-1·min-1,C物质的量浓度增加2a/3 mol·L-1,这时若增大系统压强,发现A与C的百分含量不变,则m∶n∶p∶q为( )
pC(g)+qD(g),经过5 min达到平衡,此时各物质的变化为A物质的量浓度减少amol·L-1,B的平均反应速率v(B)=a/15 mol·L-1·min-1,C物质的量浓度增加2a/3 mol·L-1,这时若增大系统压强,发现A与C的百分含量不变,则m∶n∶p∶q为( )