下列依据热化学方程式得出的结论正确的是
A.已知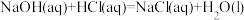 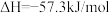 ,则 ,则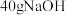 固体与稀盐酸完全反应,放出的热量即为 固体与稀盐酸完全反应,放出的热量即为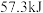 |
B.已知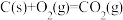 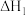 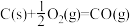 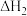 则 则 |
C.已知 ,则反应物总能量小于生成物总能量 ,则反应物总能量小于生成物总能量 |
D.已知 (白磷,s)= (白磷,s)= (红磷,s) (红磷,s) ,则白磷比红磷稳定 ,则白磷比红磷稳定 |
更新时间:2019-03-04 18:47:30
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】断裂1mol丙烷分子中所有共价键需要4006 kJ的能量,而断裂1mol新戊烷分子中所有共价键需要6356 kJ的能量。则C—C键的平均键能为
| A.386 kJ/mol | B.347kJ/mol | C.368 kJ/mol | D.414 kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】已知在1×105Pa,298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是
A.H2O(g)=H2(g)+ O2(g) △H=+484kJ/mol O2(g) △H=+484kJ/mol |
| B.2H2(g)+O2(g)=2H2O(l) △H=-484kJ/mol |
C.H2(g)+ O2(g)=H2O(l) △H=+242kJ/mol O2(g)=H2O(l) △H=+242kJ/mol |
D.H2O(g)=H2(g)+ O2(g) △H=+242kJ/mol O2(g) △H=+242kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】NA代表阿伏加 德罗常数,下列说法正确的是
| A.标准状况下,22.4LSO3中含有氧原子数目为3NA |
| B.在25℃、101kPa下,1 mol 硫和2 mol硫燃烧热相等 |
| C.18 g D2O中含有的质子数目为10NA |
| D.含0.5 mol H2SO4的稀溶液与含0.5mol Ba(OH)2 的晶体完全中和所放出的热量为中和热 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】在测定盐酸与NaOH溶液反应的反应热的实验中,下列说法正确的是
| A.使用环形玻璃搅拌棒是为了使溶液混合均匀,反应充分,减小实验误差 |
| B.为了准确测定反应混合溶液的温度,实验中温度计水银球应与内筒底部接触 |
| C.将量筒中的NaOH溶液分三次倒入量热计的内筒,并盖好杯盖 |
| D.在测定该反应热实验中需要使用的仪器有天平、烧杯、环形玻璃搅拌棒、温度计 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列说法不正确的是
| A.离子键实质是阴、阳离子间的静电作用 |
| B.石墨转化为金刚石的反应是吸热反应,说明金刚石比石墨稳定 |
| C.原电池反应的实质是自发进行的氧化还原反应 |
| D.理论上可燃物与氧气的反应均能设置成原电池装置 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列依据热化学方程式得出的结论正确的是
A.已知2SO2(g)+O2(g) 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 |
| B.已知C(石墨,s)=C(金刚石,s) △H﹥0,则金刚石比石墨稳定 |
| C.已知H+(aq)+OH–(aq)=H2O(1) △H = -57.3kJ·mol-1,则任何酸碱中和的反应热均为57.3kJ |
D.一定条件下2SO2(g)+O2(g)  2SO3(g) △H1 ,2SO2(g)+O2(g) 2SO3(g) △H1 ,2SO2(g)+O2(g)  2SO3(l) △H2 则△H1>△H2 2SO3(l) △H2 则△H1>△H2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列有关热化学方程式的叙述正确的是
| A.在稀溶液中,H+(aq)+OH-(aq)=H2O(1) ∆H=-57.3kJ/mol,若将1mol NaOH固体的加入1L 1mo/L的稀盐酸溶液中,放出的热量大于57.3kJ |
| B.已知:2H2(g)+O2(g)=2H2O(g) ∆H=-483.6kJ/mol,则氢气的燃烧热为241.8kJ/mol |
| C.已知:S(g)+O2(g)=SO2(g) ∆H1;S(s)+O2(g)=SO2(g) ∆H2,则∆H1>∆H2 |
| D.已知:N2(g)+3H2(g)⇌2NH3(g) ∆H=-92kJ/mol,增加氮气和氢气的用量,则∆H变大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
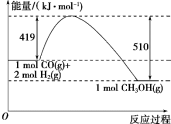
【推荐2】利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g) CH3OH(g)反应过程中的能量变化情况如图所示。下列判断正确的是
CH3OH(g)反应过程中的能量变化情况如图所示。下列判断正确的是
 CH3OH(g)反应过程中的能量变化情况如图所示。下列判断正确的是
CH3OH(g)反应过程中的能量变化情况如图所示。下列判断正确的是
| A.该反应反应物的键能之和小于生成物的键能之和 |
| B.该反应逆反应的活化能为419kJ·mol-1 |
| C.该反应的ΔH=+91 kJ·mol-1 |
| D.如果该反应生成液态CH3OH,则ΔH增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】下列说法正确的是( )
| A.燃烧热和中和热的数值都会随反应物的用量不同而改变,故1molS(s)和2molS(s)的燃烧热不相等 |
| B.已知:2C(s)+2O2(g)=2CO2(g) ΔH=akJ/mol,2C(s)+O2(g)=2CO(g)ΔH=bkJ/mol,则a>b |
| C.H2(g)的燃烧热为285.8kJ/mol,则表示H2燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l)ΔH=-571.6kJ/mol |
| D.反应NH4HCO3(s)=NH3(g)+H2O(g)+CO2(g) ΔH=+185.57kJ/mol,在低温条件下不能自发进行,但在高温条件下能自发进行 |
您最近一年使用:0次

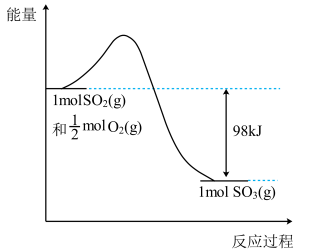
 O2(g)=SO3(g) ΔH=+98kJ·mol-1
O2(g)=SO3(g) ΔH=+98kJ·mol-1

