有一包白色粉末状混合物,可能含有Na2CO3、NaCl、CaCO3、CuSO4、Na2SO4、MgCl2中的某几种,现进行如下实验。请根据实验现象回答各问题。
实验操作 | 实验结论 |
| (1)将混合物溶于水,得到无色透明溶液 | 原混合物肯定无 |
| (2)取少量上述溶液两份,其中一份加入BaCl2溶液,立即产生白色沉淀,再加入稀硝酸,沉淀不溶解 | 原混合物肯定有 无 |
| (3)在另一份溶液中加入NaOH溶液,也产生白色沉淀 | 原混合物肯定有 不能确定的物质是 |
更新时间:2019/04/09 19:25:29
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】某无色溶液X,由 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种离子组成,取该溶液进行如下实验:
中的若干种离子组成,取该溶液进行如下实验:
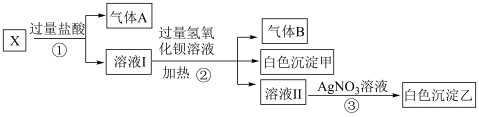
(1)白色沉淀甲是___________ 。
(2)试写出实验过程中生成气体A、B的离子方程式___________ 。
(3)通过上述实验,可确定X溶液中一定存在的离子是___________ ,一定不存在的离子是___________ ,可能存在的是___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种离子组成,取该溶液进行如下实验:
中的若干种离子组成,取该溶液进行如下实验:
(1)白色沉淀甲是
(2)试写出实验过程中生成气体A、B的离子方程式
(3)通过上述实验,可确定X溶液中一定存在的离子是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】实验室有NaHSO4、Ba(OH)2、NH3·H2O、NaHCO3、KAl(SO4)2五种无色溶液,现欲通过它们之间的相互反应的现象对其进行鉴别。部分物质间的反应现象如表。
表中“↑”表示生成气体物质,“↓”表示生成沉淀。根据以上信息,回答以下问题。
(1)B,E的化学式分别为________ 、________ 。
(2)写出A的电离方程式:_____________ 。
(3)向含有0.1mol溶质的D溶液中滴加E溶液,所生成沉淀的物质的量之和最多为________ mol。
| A | B | C | D | E | |
| A | ↓ | ||||
| B | ↑ | ↓ | |||
| C | ↑ | ↑↓ | ↓ | ||
| D | ↓ | ↑↓ | ↓ | ||
| E | ↓ | ↓ | ↓ |
(1)B,E的化学式分别为
(2)写出A的电离方程式:
(3)向含有0.1mol溶质的D溶液中滴加E溶液,所生成沉淀的物质的量之和最多为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】A、B、C、D为四种可溶性的盐,它们的阳离子分别可能是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别可能是NO3-、SO42-、Cl−、CO32-中的一种。(离子在物质中不重复出现)
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
根据①②实验事实可推断:
(1)A的化学式为____________ ,B的化学式为____________ 。
(2)写出少量盐酸与D反应的离子方程式:___________________________ 。
(3)写出C与Ba(OH)2溶液反应的离子方程式:________________________ 。
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
根据①②实验事实可推断:
(1)A的化学式为
(2)写出少量盐酸与D反应的离子方程式:
(3)写出C与Ba(OH)2溶液反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】为消除煤烟气中的 ,研究者提出了多种方法。
,研究者提出了多种方法。
(1)向燃煤中加入适量石灰石( ),高温时将
),高温时将 转化为
转化为 的化学方程式是
的化学方程式是_______ 。
(2)以 溶液作为吸收剂,一定条件下将
溶液作为吸收剂,一定条件下将 转化为
转化为 的反应为放热反应。在图中画出该反应过程的能量变化
的反应为放热反应。在图中画出该反应过程的能量变化______ 。

(3)用 溶液吸收烟气中的
溶液吸收烟气中的 ,得到亚硫酸钠(
,得到亚硫酸钠( )粗品,其流程如下。
)粗品,其流程如下。

① 与
与 溶液反应的离子方程式是
溶液反应的离子方程式是_______ 。
②设计实验证明亚硫酸钠粗品中含有
_______ 。
 ,研究者提出了多种方法。
,研究者提出了多种方法。(1)向燃煤中加入适量石灰石(
 ),高温时将
),高温时将 转化为
转化为 的化学方程式是
的化学方程式是(2)以
 溶液作为吸收剂,一定条件下将
溶液作为吸收剂,一定条件下将 转化为
转化为 的反应为放热反应。在图中画出该反应过程的能量变化
的反应为放热反应。在图中画出该反应过程的能量变化
(3)用
 溶液吸收烟气中的
溶液吸收烟气中的 ,得到亚硫酸钠(
,得到亚硫酸钠( )粗品,其流程如下。
)粗品,其流程如下。
①
 与
与 溶液反应的离子方程式是
溶液反应的离子方程式是②设计实验证明亚硫酸钠粗品中含有

您最近一年使用:0次
【推荐2】锂/磷酸氧铜电池是一种以磷酸氧铜作为正极材料的锂离子电池,其正极的活性物质是Cu4O(PO4)2,制备流程如下:
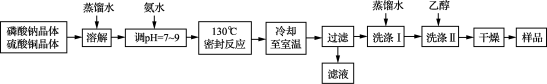
主要反应原理:2Na3PO4+4CuSO4+2NH3·H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)实验室进行“过滤”操作使用的玻璃仪器除烧杯外主要有____________ 。
(2)流程中“洗涤Ⅰ”后,检验沉淀已洗涤干净的方法是__________ 。

主要反应原理:2Na3PO4+4CuSO4+2NH3·H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)实验室进行“过滤”操作使用的玻璃仪器除烧杯外主要有
(2)流程中“洗涤Ⅰ”后,检验沉淀已洗涤干净的方法是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】海洋中蕴含着丰富的资源,我们通过“浓缩、氧化、提取”等步骤提取其中的溴单质等资源。为研究海水提溴工艺,甲、乙两同学分别设计了如下实验流程:
甲:苦卤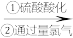 含溴海水
含溴海水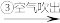 含溴空气
含溴空气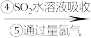 溴水混合物
溴水混合物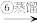 溴蒸气
溴蒸气 液溴
液溴
乙:苦卤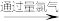 含溴海水
含溴海水 溴蒸气
溴蒸气 液溴
液溴
(1)甲同学方案中步骤①硫酸酸化的目的是_______ 。
(2)步骤③通入热空气或水蒸气吹出 ,利用了溴的
,利用了溴的_______ 性。甲同学步骤④所发生反应的化学反应方程式为_______ 。
(3)步骤④用 水溶液吸收
水溶液吸收 ,吸收率可达95%,由此反应可知,除环境保护外,该工业生产还应解决的主要问题是
,吸收率可达95%,由此反应可知,除环境保护外,该工业生产还应解决的主要问题是_______ 。
(4)步骤④中 被氧化生成
被氧化生成 ,写出检验
,写出检验 的方法
的方法_______ 。
(5)对比甲、乙两流程,最大的区别在于对含溴海水的处理方法不同,其中符合工业生产要求的是_______ (填“甲”或“乙”),理由是_______ 。
甲:苦卤
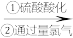 含溴海水
含溴海水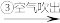 含溴空气
含溴空气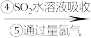 溴水混合物
溴水混合物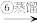 溴蒸气
溴蒸气 液溴
液溴乙:苦卤
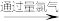 含溴海水
含溴海水 溴蒸气
溴蒸气 液溴
液溴(1)甲同学方案中步骤①硫酸酸化的目的是
(2)步骤③通入热空气或水蒸气吹出
 ,利用了溴的
,利用了溴的(3)步骤④用
 水溶液吸收
水溶液吸收 ,吸收率可达95%,由此反应可知,除环境保护外,该工业生产还应解决的主要问题是
,吸收率可达95%,由此反应可知,除环境保护外,该工业生产还应解决的主要问题是(4)步骤④中
 被氧化生成
被氧化生成 ,写出检验
,写出检验 的方法
的方法(5)对比甲、乙两流程,最大的区别在于对含溴海水的处理方法不同,其中符合工业生产要求的是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】氧化镁在医药、建筑等行业应用广泛。某兴趣小组用菱镁矿(主要成分为 ,还含少量
,还含少量 及不溶于酸的杂质)制备氧化镁,设计实验流程如下:
及不溶于酸的杂质)制备氧化镁,设计实验流程如下:

(1)菱镁矿与稀硫酸反应前,将菱镁矿石粉碎成粉末的目的是___ 。
(2)步骤(Ⅰ)中生成气体的分子式为______ 。分离溶液A和沉淀的操作的名称是_____ 。
(3)步骤(Ⅱ)中发生的反应 ,其中还原剂是
,其中还原剂是_______ 。
(4)溶液B中含有的主要阴离子是______ 。
(5)为检验步骤(Ⅲ)中所得 溶液是否还含有
溶液是否还含有 ,使用的试剂是
,使用的试剂是_____ 。
(6)步骤(Ⅳ)中发生反应的离子方程式为______ 。
(7)步骤(Ⅴ)中 受热分解的化学方程式为
受热分解的化学方程式为________ 。
 ,还含少量
,还含少量 及不溶于酸的杂质)制备氧化镁,设计实验流程如下:
及不溶于酸的杂质)制备氧化镁,设计实验流程如下:
(1)菱镁矿与稀硫酸反应前,将菱镁矿石粉碎成粉末的目的是
(2)步骤(Ⅰ)中生成气体的分子式为
(3)步骤(Ⅱ)中发生的反应
 ,其中还原剂是
,其中还原剂是(4)溶液B中含有的主要阴离子是
(5)为检验步骤(Ⅲ)中所得
 溶液是否还含有
溶液是否还含有 ,使用的试剂是
,使用的试剂是(6)步骤(Ⅳ)中发生反应的离子方程式为
(7)步骤(Ⅴ)中
 受热分解的化学方程式为
受热分解的化学方程式为
您最近一年使用:0次
【推荐2】Ⅰ.氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为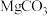 ,另含少量杂质
,另含少量杂质 和
和 等)为原料制备高纯氧化镁的实验流程如下:
等)为原料制备高纯氧化镁的实验流程如下:
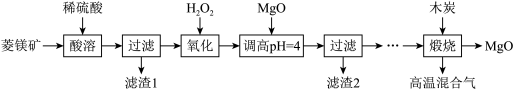
已知:① 不溶于稀硫酸和稀盐酸,②滤渣2中除了过量的MgO外,还含有
不溶于稀硫酸和稀盐酸,②滤渣2中除了过量的MgO外,还含有 。
。
(1)酸溶时,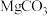 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为_______ 。
(2)滤渣1的化学式为_______ 。
(3)“氧化”流程的目的把 氧化成
氧化成 ,再调节pH把
,再调节pH把 除去,写出“氧化”流程的离子方程式为
除去,写出“氧化”流程的离子方程式为_______ 。
Ⅱ.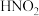 是一种弱酸,且不稳定,易分解生成NO和
是一种弱酸,且不稳定,易分解生成NO和 ;它能被常见的强氧化剂氧化:在酸性溶液中它也是一种氧化剂,如能把
;它能被常见的强氧化剂氧化:在酸性溶液中它也是一种氧化剂,如能把 氧化成
氧化成 。
。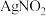 是一种难溶于水、易溶于酸的化合物,试回答下列问题:
是一种难溶于水、易溶于酸的化合物,试回答下列问题:
(4)人体正常的血红蛋白含有 ,若误食亚硝酸盐(如
,若误食亚硝酸盐(如 ),则导致血红蛋白中的
),则导致血红蛋白中的 转化为
转化为 而中毒,服用维生素C可解毒。下列叙述不正确的是_______(填字母)。
而中毒,服用维生素C可解毒。下列叙述不正确的是_______(填字母)。
(5)某同学把新制的氯水(主要成分 )加到
)加到 溶液中,观察到氯水褪色,同时生成
溶液中,观察到氯水褪色,同时生成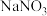 和HCl,请写出反应的离子方程式:
和HCl,请写出反应的离子方程式:_______ 。
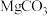 ,另含少量杂质
,另含少量杂质 和
和 等)为原料制备高纯氧化镁的实验流程如下:
等)为原料制备高纯氧化镁的实验流程如下:
已知:①
 不溶于稀硫酸和稀盐酸,②滤渣2中除了过量的MgO外,还含有
不溶于稀硫酸和稀盐酸,②滤渣2中除了过量的MgO外,还含有 。
。(1)酸溶时,
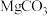 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为(2)滤渣1的化学式为
(3)“氧化”流程的目的把
 氧化成
氧化成 ,再调节pH把
,再调节pH把 除去,写出“氧化”流程的离子方程式为
除去,写出“氧化”流程的离子方程式为Ⅱ.
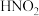 是一种弱酸,且不稳定,易分解生成NO和
是一种弱酸,且不稳定,易分解生成NO和 ;它能被常见的强氧化剂氧化:在酸性溶液中它也是一种氧化剂,如能把
;它能被常见的强氧化剂氧化:在酸性溶液中它也是一种氧化剂,如能把 氧化成
氧化成 。
。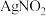 是一种难溶于水、易溶于酸的化合物,试回答下列问题:
是一种难溶于水、易溶于酸的化合物,试回答下列问题:(4)人体正常的血红蛋白含有
 ,若误食亚硝酸盐(如
,若误食亚硝酸盐(如 ),则导致血红蛋白中的
),则导致血红蛋白中的 转化为
转化为 而中毒,服用维生素C可解毒。下列叙述不正确的是_______(填字母)。
而中毒,服用维生素C可解毒。下列叙述不正确的是_______(填字母)。| A.亚硝酸盐被还原 | B.维生素C是还原剂 |
C.维生素C将 还原为 还原为 | D.亚硝酸盐是还原剂 |
 )加到
)加到 溶液中,观察到氯水褪色,同时生成
溶液中,观察到氯水褪色,同时生成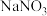 和HCl,请写出反应的离子方程式:
和HCl,请写出反应的离子方程式:
您最近一年使用:0次


 中燃烧的化学方程式为
中燃烧的化学方程式为

