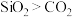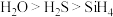下列结论正确的是
①粒子半径:K+>Al3+>S2->Cl- ②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I- ④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO ⑥非金属性:O>N>P>Si
①粒子半径:K+>Al3+>S2->Cl- ②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I- ④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO ⑥非金属性:O>N>P>Si
| A.②③⑤ | B.②④⑤⑥ | C.①②⑥ | D.②③⑥ |
更新时间:2019-04-09 08:50:06
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列对一些实验事实的理论解释不正确的是
选项 | 实验事实 | 理论解释 |
A |  比 比 原子稳定 原子稳定 | 最外层电子数: 有8个, 有8个, 有1个 有1个 |
B | 酸性: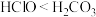 | 非金属性: |
C | 原子半径: |  原子、 原子、 原子的电子层数相同,但 原子的电子层数相同,但 原子的核电荷数比 原子的核电荷数比 原子多,对核外电子的吸引能力比 原子多,对核外电子的吸引能力比 原子强 原子强 |
D |  分子比 分子比 分子稳定 分子稳定 |  键比 键比 键强 键强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W是原子序数依次增大的四种短周期元素,其中只有一种是金属元素,X、W同主族且能形成一种离子化合物WX;Y的气态氢化物、最高价氧化物的水化物可反应生成一种盐;Z原子的最外层电子数与其电子总数之比为3∶4。下列说法中正确的是
| A.原子半径:W>Z>Y>X | B.氢化物稳定性:Y>Z |
| C.WY3中只有离子键没有共价键 | D.X与Z可形成10电子和18电子分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于F、Cl、Br、I的比较,不正确 的是
| A.它们的原子核外电子层数随核电荷数的增加而增多 |
| B.单质的氧化性随核电荷数的增加而减弱 |
| C.它们的氢化物的稳定性随核电荷数的增加而增强 |
| D.单质的颜色随核电荷数的增加而加深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一、如图是元素周期表的一部分,下列说法正确的是
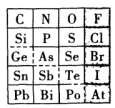

A.氢化物的还原性: |
B.最高价氧化物对应水化物的酸性: |
C.Bi的最高价氧化物为 |
| D.阴影部分元素中,简单氢化物稳定性最强的是At |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】Na、Al、Fe都是重要的金属元素。下列说法正确的是
| A.氧化物都是碱性氧化物 |
| B.氢氧化物都是白色固体 |
| C.单质都可以与水反应 |
| D.单质在空气中都形成致密氧化膜 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列各组物质性质的比较中,正确的是
| A.还原性:HCl>HBr>HI | B.热稳定性:H2O<H2S<H2Se |
| C.酸性:HClO4>HBrO4>HIO4 | D.碱性:NaOH>KOH>RbOH |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关比较正确的是
A.熔点: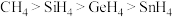 | B.熔、沸点:NaBr>NaCl>MgO |
C.酸性: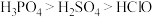 | D.热稳定性: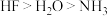 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】我国嫦娥五号探测器带回1.731kg的月球土壤,经分析发现其构成与地球土壤类似。月球土壤中含有的短周期元素W、X、Y、Z原子序数依次增大,最外层电子数之和为15。X、Y、Z为同周期相邻元素,且均不与W同族,下列说法正确的是
A.离子半径: | B.金属性: |
C.氢化物的稳定性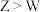 | D.XW属于共价化合物 |
您最近一年使用:0次