下列离子方程式书写正确的是
| A.漂白粉溶液中通入过量的CO2: Ca2++2ClO-+ CO2+ H2O = CaCO3↓+2HClO |
| B.氢氧化铁与HI溶液反应的离子方程式为Fe(OH)3+3H+═Fe3++3H2O |
| C.NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-=BaCO3↓+H2O |
| D.钠和冷水反应 : Na+2H2O=Na++2OH-+H2↑ |
更新时间:2019-04-23 10:55:23
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列化学反应的离子方程式正确的是 ( )
| A.将少量金属钠放入冷水中:Na+2H2O=Na++2OH-+H2↑ |
| B.过氧化钠固体与水反应:2O22-+2H2O=4OH-+O2↑ |
| C.向澄清石灰水中通入过量的碳酸氢钠:Ca2++2OH-+2HCO3-=CaCO₃↓+2H2O+CO32- |
| D.将除去氧化膜的铝片加入烧碱溶液中:Al++2H2O=2AlO2-+2H2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列指定反应的离子方程式正确的是
A.用铝粉和NaOH溶液反应制取少量H2: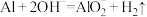 |
B.室温下用浓HNO3溶解Cu: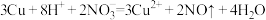 |
C.含等物质的量的Fe2+、I-、Br-的溶液中通入适量氯气: 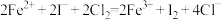 |
D.亚硫酸钠溶液吸收少量氯气:  |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下面是用饱和NaCl溶液来制备一种重要的含氯消毒剂 的工艺流程图:
的工艺流程图:
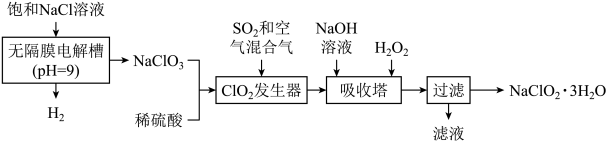
下列说法正确的是
 的工艺流程图:
的工艺流程图:
下列说法正确的是
A.发生器中通入空气的目的是氧化 |
B.吸收塔内发生反应的离子方程式: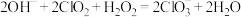 |
C.过滤后的滤液中大量存在: 、 、 、 、 、 、 、 、 |
D.电解槽中总的离子方程式: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知下列三个离子反应方程式如下:①X2++Y=X+Y2+ ②Y2++W=W2++Y ③W2++Z=Z2++W。则氧化性最弱的粒子是
| A.X2+ | B.Y2+ | C.W2+ | D.Z2+ |
您最近一年使用:0次
【推荐2】根据下表信息,下列叙述中正确的是
| 序号 | 氧化剂 | 还原剂 | 氧化产物 | 还原产物 |
| ① |  (足量) (足量) |  |  | |
| ② |  |  |  |  |
| ③ |  | 浓盐酸 |  | |
| ④ |  | 浓盐酸 |  |  |
A.表中①反应的氧化产物只能有 |
B.表中②生成1个 将有4个电子转移 将有4个电子转移 |
C.表中④的离子方程式配平后, 的化学计量数为16 的化学计量数为16 |
| D.表中③还原产物是KCl |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列离子方程式与所述事实相符且正确的是
A.漂白粉溶液在空气中失效:ClO﹣+CO2+H2O=HClO+ |
B.用浓盐酸与二氧化锰反应制取少量氯气:MnO2+4HCl Mn2++2Cl﹣+Cl2↑+2H2O Mn2++2Cl﹣+Cl2↑+2H2O |
C.向NaAlO2溶液中通入过量的CO2制Al(OH)3: +CO2+2H2O=Al(OH)3↓+ +CO2+2H2O=Al(OH)3↓+ |
D.氯气在强碱溶液中反应生成氯化钠、次氯酸钠与氯酸钠:6Cl2+12OH﹣=6Cl﹣+5ClO﹣+ +6H2O +6H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列试剂贮存方法错误的是
| A.钠应保存在石蜡油或煤油中 | B.漂白粉密封存放在干燥阴暗的地方 |
| C.新制氯水保存在棕色试剂瓶中 | D.过氧化钠可以暂时存放在敞口瓶中 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列“类比”“推理”中正确的是
| A.铁与氯气加热生成FeCl3,则铁与碘单质加热生成FeI3 |
| B.Na与H2O反应生成NaOH,则Fe与水蒸气在高温下反应生成Fe(OH)3 |
| C.Na与O2加热生成Na2O2,则Li与O2加热生成Li2O2 |
| D.FeCl3和足量氨水反应生成Fe(OH)3,则AlCl3与足量氨水反应生成Al(OH)3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验方案能够达到目的的是
| 实验目的 | 实验方案 | |
| A | 除去氯气中的水蒸气 | 将混合气体通过盛有碱石灰的干燥管 |
| B | 检验钠与H2O的反应产物NaOH | 将绿豆粒大小的钠投入盛有适量水的培养皿中,加入稀盐酸 |
| C | 鉴别碳酸钠和碳酸氢钠溶液 | 向溶液中分别滴加稀盐酸 |
| D | 检验新制氯水中含有HClO | 向新制氯水中加入少量CaCO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 和
和 反应可能有
反应可能有 可能化合生成
可能化合生成
 可能被NaOH溶液完全吸收生成
可能被NaOH溶液完全吸收生成 和
和


