关于常温下浓度均为0.1 mol·Lˉ1的盐酸和醋酸溶液,下列说法正确的是
| A.c(CH3COOˉ)=c(Clˉ) |
| B.醋酸溶液的pH小于盐酸 |
| C.醋酸的电离方程式:CH3COOH=CH3COOˉ+H+ |
| D.等物质的量浓度、等体积的盐酸与氢氧化钠溶液混合后溶液呈中性 |
更新时间:2019-05-08 11:15:37
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】常温下,下列说法正确的是(忽略混合或溶解时溶液体积变化)
| A.pH=3的醋酸和pH=3的盐酸中分别加入足量锌粒,产生的氢气总量醋酸多 |
| B.体积和物质的量浓度均相同的醋酸和盐酸,分别与NaOH固体反应后呈中性的溶液中:c(CH3COO-)=c(Cl-) |
| C.pH=3的醋酸溶液和pH=13的氢氧化钠溶液等体积混合后,恰好完全反应,则所用醋酸溶液的浓度等于所用氢氧化钠溶液的浓度 |
| D.pH=11的氨水和pH=11的NaOH溶液等体积混合,溶液pH>11 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列实验装置(加持装置忽略)及操作错误的是
 |  | 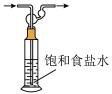 | 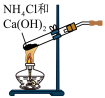 |
| A.验证铁的吸氧腐蚀 | B.用pH计测量溶液的pH | C.除去Cl2中的HCl | D.实验室制备氨气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列说法不正确 的是
| A.测得0.1 mol·L-1的一元酸HA溶液pH=3.0,则HA一定为弱电解质 |
| B.25℃时,将0.1 mol·L-1的NaOH溶液加水稀释100倍,所得溶液的pH=11.0 |
| C.25℃时,将0.1 mol·L-1的HA溶液加水稀释至pH=4.0,所得溶液c(OH-)=1×10-10 mol·L-1 |
| D.0.1 mol·L-1的HA溶液与0.1 mol·L-1的NaOH溶液等体积混合,所得溶液pH一定等于7.0 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】在醋酸的下列性质中,可以证明它一定是弱电解质的是
| A.1mol/L的醋酸溶液中c(H+)约为10-3mol/L |
| B.醋酸能与水以任意比互溶 |
| C.10mL 1mol/L的醋酸恰好与10mL 1mol/L NaOH溶液完全反应 |
| D.醋酸的导电性比强酸溶液弱 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】常温下,0.1mol/L的下列溶液,pH大于7的是
| A.Na2SO4 | B.NaHSO4 | C.Na2CO3 | D.CH3COOH |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列电离方程式错误的是
A.Al2(SO4)3=2Al3++3 | B.NaHCO3=Na++ |
C.H2SO4=2H++ | D.H2SO3=2H++ |
您最近一年使用:0次



