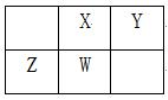
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知,下列说法正确的是( )
| W | X | |
| Y | Z |
| A.W、Z的气态氢化物相遇反应并有白烟生成,该物质为共价化合物 |
| B.Z元素氧化物对应水化物的酸性一定强于Y |
| C.X、Y两元素的最高正价相等 |
| D.最简单的气态氢化物的稳定性:Z>Y |
更新时间:2019-05-08 09:20:59
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】某无色混合气体可能由H2、O2、NH3、N2、CO2、HCl和He中的两种或多种组成。常温下取此气体200mL进行实验,实验的过程和结果如下(上述气体的体积都是折算成相同条件下的体积)。下列说法错误是
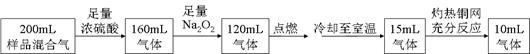

| A.原混合气体中有5ml O2 |
| B.原混合气体中肯定存在NH3,肯定不存在HCl |
| C.原混合气体中CO2的体积分数为40% |
| D.可能存在N2或He,它们在原混合气体中的体积分数不可能超过5% |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验现象描述正确的是
| A.细铁丝在氧气中剧烈燃烧,火星四射,产生黑色固体 |
| B.向澄清石灰水中通入一氧化碳,产生白色沉淀 |
| C.将氢氧化铁固体溶于稀盐酸,得到无色溶液 |
| D.将分别蘸有浓氨水与浓盐酸的玻璃棒相互靠近,无明显现象 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】根据元素周期表和元素周期律分析下面的推断,其中错误的是( )
| A.铍(Be)原子的失电子能力比镁弱 | B.硒(Se)化氢比硫化氢稳定 |
| C.氢氧化铷(Rb)是强碱 | D.Si 半径大于 C |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】X、Y、Z、W是四种短周期主族元素,X原子最外层电子数是次外层的 2 倍,Y 是地壳中含量最多的元素,Z元素在短周期中金属性最强,W与Y 位于同一主族。下列叙述正确的是
| A.原子半径:r(W)>r(Z)>r(Y)>r(X) |
| B.Y与Z形成的两种常见化合物化学键类型完全相同 |
| C.X的最高价氧化物对应水化物的酸性比W的强 |
| D.Y的简单气态氢化物的热稳定性比W的强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】短周期主族元素R、X、Y、Z、W的原子序数依次增大,它们能组成一种锂离子电池的电解质溶液添加剂(结构如图1所示),它们的原子半径与原子序数的关系如图2所示。这五种元素的原子序数之和等于28。下列叙述错误的是
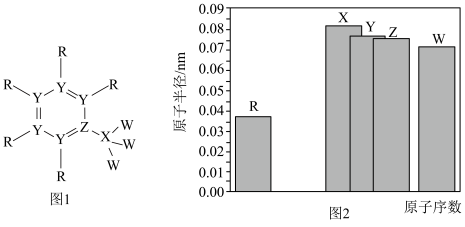

| A.元素的电负性:W>Z>Y>X |
| B.Y、Z的最简单氢化物均是由极性键形成的非极性分子 |
| C.常温下,W的单质能与R的单质发生剧烈反应 |
| D.最高价氧化物对应水化物的酸性:Z>Y |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】短周期元素 X、Y、Z、W、Q 在周期表中相对位置如图所示,已知 X 元素是地壳中含量最高的元素,下列说法正确的是


| A.Y 的非金属性比Q强,所以HnY的酸性比HnQ强 |
| B.ZX2、WX2的熔沸点、硬度相差很大,这是由于它们的化学键类型不同造成的 |
| C.W、Q、Y 元素的原子半径及其简单离子半径依次减小 |
| D.将足量的 X 单质通入 W 的氢化物的水溶液,能得到 W 的低价氧化物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】根据实验操作和现象,能达到实验目的的是
| 选项 | 实验操作和现象 | 实验目的 |
| A | 将乙烯和甲烷混合气体通入盛有酸性高锰酸钾溶液的洗气瓶中,溶液紫色变浅 | 除去甲烷中的乙烯 |
| B | 分别向MgCl2溶液和AlCl3溶液中滴加NaOH溶液至过量。MgCl2溶液产生白色沉淀,沉淀不溶解;AlCl3溶液产生的白色沉淀溶解。 | 证明金属性Mg>Al |
| C | 向亚硫酸钠溶液中滴加足量盐酸,将反应产生的气体通入品红溶液,品红溶液褪色 | 证明氯的得电子能力比硫强 |
| D | 向KI溶液中先滴加少量溴水,然后加入四氯化碳,充分振荡静置,溶液分层,上层呈紫红色,下层近乎无色。 | 证明氧化性:Br2>I2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次