某固体混合物,仅含有以下阴、阳离子中的某几种(不考虑水的电离):
为了判断该混合物的组成,现依次进行如下实验,根据实验现象,回答下列问题:
(1)取该固体混合物,加水后固体完全溶解得到无色溶液,用pH试纸测得溶液的pH为12.则混合物组成中肯定不存在的离子是_______ 。
(2)向(1)所得溶液中滴加盐酸,开始有沉淀生成,继续滴加,沉淀消失,同时有无色无味气体逸出。则肯定存在的离子是_______ ,可以排除的离子是_______ 。
(3)取以上实验的上层澄清液,滴加AgNO3溶液,有白色沉淀生成。你认为还有哪些离子尚待检验:_______ (填离子符号),请你对尚待检验的离子提出合理的检验方法(要求写出具体的步骤、现象与结论):_______
| 阳离子 | K+、Ba2+、Ag+、Mg2+ |
| 阴离子 | Cl-、 、 、 、 、 、 、 |
(1)取该固体混合物,加水后固体完全溶解得到无色溶液,用pH试纸测得溶液的pH为12.则混合物组成中肯定不存在的离子是
(2)向(1)所得溶液中滴加盐酸,开始有沉淀生成,继续滴加,沉淀消失,同时有无色无味气体逸出。则肯定存在的离子是
(3)取以上实验的上层澄清液,滴加AgNO3溶液,有白色沉淀生成。你认为还有哪些离子尚待检验:
更新时间:2019-05-16 19:29:44
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某无色透明溶液中可能存在大量Ag+、Mg2+、Fe3+、Cu2+中的一种或几种,请填写下列空白。
(1)不用做任何实验就可以肯定溶液中不存在的离子是____________________ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是__________________ ,有关反应的离子方程式为____________________ 。
(3)取(2)的滤液加过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有________________ ,有关反应的离子方程式为____________________ 。
(1)不用做任何实验就可以肯定溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是
(3)取(2)的滤液加过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】Ⅰ.为除去粗盐中的Ca2+、Mg2+、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量):
称取粗盐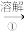
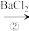
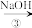
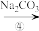
 滤液
滤液
 精盐
精盐
(1)检验 是否去除干净的方法是
是否去除干净的方法是___________ 。
(2)第③步中,发生的主要化学反应的离子方程式是_______ 。
(3)第⑥步中,发生的两个主要化学反应的化学方程式是______ 和______ 。
Ⅱ.将上述提纯的精盐配制1 mol·L-1 的NaCl溶液480mL。回答下列问题:
(4)如图所示的仪器中,配制溶液肯定不需要的是_______ (填序号)。

(5)若出现如下情况,其中将引起所配溶液浓度偏低的是_______ ;(填下列编号)
①容量瓶实验前用水洗干净,但未烘干 ②定容观察液面时俯视
③配制过程中没有洗涤烧杯和玻璃棒 ④加蒸馏水时不慎超过刻度线
 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量):称取粗盐
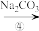
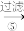 滤液
滤液
 精盐
精盐(1)检验
 是否去除干净的方法是
是否去除干净的方法是(2)第③步中,发生的主要化学反应的离子方程式是
(3)第⑥步中,发生的两个主要化学反应的化学方程式是
Ⅱ.将上述提纯的精盐配制1 mol·L-1 的NaCl溶液480mL。回答下列问题:
(4)如图所示的仪器中,配制溶液肯定不需要的是

(5)若出现如下情况,其中将引起所配溶液浓度偏低的是
①容量瓶实验前用水洗干净,但未烘干 ②定容观察液面时俯视
③配制过程中没有洗涤烧杯和玻璃棒 ④加蒸馏水时不慎超过刻度线
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】有A、B、C、D四种强电解质,它们在水中电离产生下列离子(每种物质只含一种阴离子且互不重复)。
已知:①A、C溶液的pH均大于7,A、B的溶液中水的电离程度相同;②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无现象。
(1)A是__________ ,B是__________ (填化学式) 。
(2)用离子方程式表示A溶液pH大于7的原因:____________________
(3)写出C和D反应的离子方程式_________________ 。
(4)25 ℃时,0.1 mol·L-1 B溶液的pH=a,则B溶液中c(H+)-c(NH3·H2O)=_____________ (用含有a的关系式表示)。
(5)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序是______________ 。
| 阳离子 | Na+、Ba2+、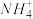 |
| 阴离子 | CH3COO-、OH-、Cl-、 |
(1)A是
(2)用离子方程式表示A溶液pH大于7的原因:
(3)写出C和D反应的离子方程式
(4)25 ℃时,0.1 mol·L-1 B溶液的pH=a,则B溶液中c(H+)-c(NH3·H2O)=
(5)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.已知某无色溶液中可能含有Na+、NH4+、Ba2+、Cu2+、SO42﹣、SO32﹣、Cl﹣、Br﹣、CO32﹣中的若干种,为检验其中含有的离子,进行如下实验:
①取10mL溶液,加入足量氯水,无气体产生,再加入CCl4溶液分层,下层为橙红色;
②分液后,往①的上层溶液中加入足量BaCl2和HCl溶液,产生白色沉淀2.33g;
③另取10mL原溶液,加入过量的浓氢氧化钠溶液并加热,收集到标准状况下448mL气体。
回答下列问题:
(1)一定不存在的离子为:____________ ;
(2)需要通过焰色反应来确定是否存在Na+吗?_________ (填“是”或“否”),请简要说明原因_________ 。
Ⅱ.电子工业常用30%的FeCl3溶液腐蚀绝缘板上的铜箔,制造印刷电路板。
(1)FeCl3溶液与金属铜发生反应的化学反应方程式是__________________ ;
(2)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得氯化铁溶液,准备采用下列步骤:

上述实验中加入或生成的有关物质的化学式为②_________ ; ④____________ ;
若向溶液②中加入氢氧化钠溶液,其实验现象为______________________ 。
①取10mL溶液,加入足量氯水,无气体产生,再加入CCl4溶液分层,下层为橙红色;
②分液后,往①的上层溶液中加入足量BaCl2和HCl溶液,产生白色沉淀2.33g;
③另取10mL原溶液,加入过量的浓氢氧化钠溶液并加热,收集到标准状况下448mL气体。
回答下列问题:
(1)一定不存在的离子为:
(2)需要通过焰色反应来确定是否存在Na+吗?
Ⅱ.电子工业常用30%的FeCl3溶液腐蚀绝缘板上的铜箔,制造印刷电路板。
(1)FeCl3溶液与金属铜发生反应的化学反应方程式是
(2)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得氯化铁溶液,准备采用下列步骤:

上述实验中加入或生成的有关物质的化学式为②
若向溶液②中加入氢氧化钠溶液,其实验现象为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D四种可溶性盐,阳离子分别可能是Ba2+、Na+、Ag+、Cu2+中的某一种,阴离子分别可能是NO3-、SO42-、Cl-、CO32-中的某一种。根据你所学习的知识回答下列问题:①把四种盐分别溶于盛有蒸馏水的试管中,只有C盐的溶液呈蓝色。②向①的四支试管中分别加入盐酸,B盐有沉淀生成,D盐有无色无味气体溢出。
(1)四种盐的化学式分别为:A、_______ ;B、___________ ;C、__________ ;D、________ 。
(2)写出向①的四支试管中分别加盐酸时的离子反应方程式____________________________ 。
(1)四种盐的化学式分别为:A、
(2)写出向①的四支试管中分别加盐酸时的离子反应方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】某pH =1的溶液X,其中可能含有Al3+、Fe2+、Fe3+、Ba2+、NH4+、CO32-、SO42-、SiO32-、NO3-中的一种或几种,取500 mL该溶液进行实验,其现象及转化如图所示。

已知:反应过程中有一种气体是红棕色。请回答下列问题:
(1)仅由强酸性条件便可判断溶液X中一定不存在的离子有______ 。
(2)溶液X中,关于NO3-的判断一定正确的是______  填字母
填字母 。
。
a.一定有
b.一定没有
c.可能有
(3)反应①中产生气体A的离子方程式为______ 。
(4)反应⑦中生成沉淀K的离子方程式为______ 。
(5)溶液X中不能确定的离子是______ 。
(6)若实验测定A、F、K均为0.01 mol,试确定沉淀C是______ ,其物质的量范围是______ 。

已知:反应过程中有一种气体是红棕色。请回答下列问题:
(1)仅由强酸性条件便可判断溶液X中一定不存在的离子有
(2)溶液X中,关于NO3-的判断一定正确的是
 填字母
填字母 。
。a.一定有
b.一定没有
c.可能有
(3)反应①中产生气体A的离子方程式为
(4)反应⑦中生成沉淀K的离子方程式为
(5)溶液X中不能确定的离子是
(6)若实验测定A、F、K均为0.01 mol,试确定沉淀C是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】烧碱在保存过程会部分变质(杂质主要为Na2CO3)。
Ⅰ、定性检验
取少量烧碱样品于试管,加蒸馏水使其完全溶解。向所得溶液滴加几滴BaCl2溶液,若出现白色沉淀,则说明已变质,反之则未变质
Ⅱ、定量测定
准确称取5.0g样品配制成250mL溶液,各取配制好的烧碱溶液20.00mL于三个锥形瓶中,分别加入过量的BaCl2溶液(使Na2CO3完全转变成BaCO3沉淀),并向锥形瓶中各加入1∼2滴指示剂(已知几种酸碱指示剂变色的pH范围:①甲基橙3.1∼4.4②甲基红4.4∼6.2③酚酞8.2∼10),用浓度为0.2000mol·L−1的盐酸标准液进行滴定。相关数据记录如下:
试回答:
(1)如何确定BaCl2溶液是否滴加过量?__________________
(2)向混有BaCO3沉淀的NaOH溶液中滴入盐酸,应选用_______________ 做指示剂,理由是____________ ;判断到达滴定终点的实验现象是___________________ .
(3)滴定时的正确操作是____________________________________ .依据表中数据,计算出烧碱样品中含NaOH(M=40g/mol)的质量分数为________________ %.(小数点后保留两位数字)
(4)下列操作会导致烧碱样品中NaOH含量测定值偏高的是_________________
A. 锥形瓶用蒸馏水洗后未用待测液润洗 B. 酸式滴定管用蒸馏水洗后未用标准液润洗
C. 在滴定前有气泡,滴定后气泡消失 D. 滴定前平视读数,滴定结束俯视读数。
Ⅰ、定性检验
取少量烧碱样品于试管,加蒸馏水使其完全溶解。向所得溶液滴加几滴BaCl2溶液,若出现白色沉淀,则说明已变质,反之则未变质
Ⅱ、定量测定
准确称取5.0g样品配制成250mL溶液,各取配制好的烧碱溶液20.00mL于三个锥形瓶中,分别加入过量的BaCl2溶液(使Na2CO3完全转变成BaCO3沉淀),并向锥形瓶中各加入1∼2滴指示剂(已知几种酸碱指示剂变色的pH范围:①甲基橙3.1∼4.4②甲基红4.4∼6.2③酚酞8.2∼10),用浓度为0.2000mol·L−1的盐酸标准液进行滴定。相关数据记录如下:
| 实验编号 | V(烧碱溶液)/mL | V(HCl)/mL | |
| 初读数 | 末读数 | ||
| 1 | 20.00 | 0.50 | 31.50 |
| 2 | 20.00 | 1.00 | 32.04 |
| 3 | 20.00 | 1.10 | 32.18 |
试回答:
(1)如何确定BaCl2溶液是否滴加过量?
(2)向混有BaCO3沉淀的NaOH溶液中滴入盐酸,应选用
(3)滴定时的正确操作是
(4)下列操作会导致烧碱样品中NaOH含量测定值偏高的是
A. 锥形瓶用蒸馏水洗后未用待测液润洗 B. 酸式滴定管用蒸馏水洗后未用标准液润洗
C. 在滴定前有气泡,滴定后气泡消失 D. 滴定前平视读数,滴定结束俯视读数。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某工厂的工业废水中含有大量的FeSO4和较多的Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图,回答下列问题:

(1)⑥的操作方法是_______ ,试剂⑦是_______
(2)若取2mL溶液④加入试管中,然后滴加氢气化钠溶液,产生的现象是_______ ;此过程中属于氧化还原反应的化学方程式是_______
(3)溶液②在空气中易被氧化,写出检验溶液②被氧化的具体操作方法_______ ,相应的离子方程式是_______

(1)⑥的操作方法是
(2)若取2mL溶液④加入试管中,然后滴加氢气化钠溶液,产生的现象是
(3)溶液②在空气中易被氧化,写出检验溶液②被氧化的具体操作方法
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有一包白色固体,它可能是NaCl、K2CO3、CuSO4、NaNO3中的一种或几种,进行下列实验:
①溶于水,得无色溶液;
②在所得溶液中滴入AgNO3溶液,生成白色沉淀;
③再滴加稀硝酸,沉淀量减少但不完全消失,同时有气泡生成。
根据上述现象判断:
(1)白色固体一定含有的成分是____ ,一定不含有的成分是____ ,可能含有的成分是____ 。(以上各种物质均写化学式)
(2)请写出上述实验②中有关反应的离子方程式:____ 。
①溶于水,得无色溶液;
②在所得溶液中滴入AgNO3溶液,生成白色沉淀;
③再滴加稀硝酸,沉淀量减少但不完全消失,同时有气泡生成。
根据上述现象判断:
(1)白色固体一定含有的成分是
(2)请写出上述实验②中有关反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
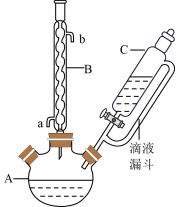
【推荐1】对氯苯甲酸是合成非甾族消炎镇痛药的中间体,还能用于燃料和农药的合成,实验室中制备对氯苯甲酸的反应原理和装置图如图:

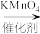
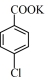 +MnO2
+MnO2
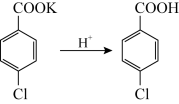
常温条件下的有关数据如表所示:
实验步骤:在装置A中加入一定量的催化剂、适量KMnO4、100mL水;安装好装置,在滴液漏斗中加入6.00mL对氯甲苯,在温度为93℃左右时,逐滴滴入对氯甲苯;控制温度在93℃左右,反应2h,过滤,将滤渣用热水洗涤,使洗涤液与滤液合并,加入稀硫酸酸化,加热浓缩;然后过滤,将滤渣用冷水进行洗涤,干燥后称量其质量为7.19g。
回答下列问题:
(1)装置A的名称是____ ,根据上述实验药品的用量,该装置的最适宜规格为____ (填标号)。
A.100mL B.250mL C.500mL D.1000mL
(2)在装置中仪器B的作用是____ 。
(3)控制温度为93℃左右的方法是____ 。
(4)滤液中加入稀硫酸酸化,可观察到的实验现象是____ 。
(5)第二次过滤所得滤渣要用冷水进行洗涤,其原因是____ ,判断滤渣洗干净的操作和现象是____ 。
(6)本实验的产率是____ (保留3位有效数字)。


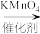
 +MnO2
+MnO2
常温条件下的有关数据如表所示:
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 颜色 | 水溶性 | |
| 对氯甲苯 | 126.5 | 7.5 | 162 | 1.07 | 无色 | 难溶 |
| 对氯苯甲酸 | 156.5 | 243 | 275 | 1.54 | 白色 | 微溶 |
| 对氯苯甲酸钾 | 194.5 | 具有盐的通性,属于可溶性盐 | ||||
回答下列问题:
(1)装置A的名称是
A.100mL B.250mL C.500mL D.1000mL
(2)在装置中仪器B的作用是
(3)控制温度为93℃左右的方法是
(4)滤液中加入稀硫酸酸化,可观察到的实验现象是
(5)第二次过滤所得滤渣要用冷水进行洗涤,其原因是
(6)本实验的产率是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某钠盐溶液可能含有阴离子NO3-、CO32-、SO32-、SO42-、Cl-、Br-、I-。为鉴别这些离子,分别取少量溶液进行以下实验:
①测得混合液呈碱性;
②加HCl后,生成无色无味气体,该气体能使饱和石灰水溶液变浑浊;
③加CCl4后,滴加少量氯水,振荡后,CCl4层未变色;
④加BaCl2溶液产生白色沉淀,分离,在沉淀中加入足量盐酸,沉淀不能完全溶解;
⑤加HNO3酸化后,再加过量AgNO3,溶液中析出白色沉淀。
根据上述实验判断,原溶液中一定存在的阴离子为__________ ,一定不存在的阴离子为__________ ,可能存在的阴离子为_________ 。
①测得混合液呈碱性;
②加HCl后,生成无色无味气体,该气体能使饱和石灰水溶液变浑浊;
③加CCl4后,滴加少量氯水,振荡后,CCl4层未变色;
④加BaCl2溶液产生白色沉淀,分离,在沉淀中加入足量盐酸,沉淀不能完全溶解;
⑤加HNO3酸化后,再加过量AgNO3,溶液中析出白色沉淀。
根据上述实验判断,原溶液中一定存在的阴离子为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
真题
【推荐3】已知化合物X由3种元素组成,某学习小组进行了如下实验:
①取适量X,加水完全溶解,无气体产生,溶液呈碱性;进行焰色反应,透过蓝色钴玻璃观察到火焰呈紫色;
②取1.685gX溶于水,加入含HCl 0.02000mol的盐酸恰好中和;中和后的溶液与硝酸酸化的过量AgNO3溶液反应,得到4.305g白色沉淀。
请回答:
(1)X中3种元素是___________ (用元素符号表示);
(2)X与水反应的化学方程式是___________ ;
(3)X中一种元素对应的单质,可与足量的Na2CO3溶液反应得到Cl2O,写出该反应的化学方程式:___________ 。
①取适量X,加水完全溶解,无气体产生,溶液呈碱性;进行焰色反应,透过蓝色钴玻璃观察到火焰呈紫色;
②取1.685gX溶于水,加入含HCl 0.02000mol的盐酸恰好中和;中和后的溶液与硝酸酸化的过量AgNO3溶液反应,得到4.305g白色沉淀。
请回答:
(1)X中3种元素是
(2)X与水反应的化学方程式是
(3)X中一种元素对应的单质,可与足量的Na2CO3溶液反应得到Cl2O,写出该反应的化学方程式:
您最近一年使用:0次



