有一包白色固体,它可能是NaCl、K2CO3、CuSO4、NaNO3中的一种或几种,进行下列实验:
①溶于水,得无色溶液;
②在所得溶液中滴入AgNO3溶液,生成白色沉淀;
③再滴加稀硝酸,沉淀量减少但不完全消失,同时有气泡生成。
根据上述现象判断:
(1)白色固体一定含有的成分是____ ,一定不含有的成分是____ ,可能含有的成分是____ 。(以上各种物质均写化学式)
(2)请写出上述实验②中有关反应的离子方程式:____ 。
①溶于水,得无色溶液;
②在所得溶液中滴入AgNO3溶液,生成白色沉淀;
③再滴加稀硝酸,沉淀量减少但不完全消失,同时有气泡生成。
根据上述现象判断:
(1)白色固体一定含有的成分是
(2)请写出上述实验②中有关反应的离子方程式:
更新时间:2022-09-15 22:46:43
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有一包白色固体,可能含有CaCO3、Na2SO4、KNO3、CuSO4、BaCl2五种电解质中的一种或几种。现进行如下实验:
①取少量固体粉末,加入盛有足量水的烧杯中,充分搅拌静置后,底部白色沉淀,上层为无色 溶液;
②继续往烧杯中加入足量稀硝酸,白色沉淀完全消失;并有气泡产生。
③取少量②中溶液滴加Ba(NO3)2溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解。
(1)请写出上述第②步中,白色沉淀与稀硝酸反应的方程式_____________ ;
(2)根据以上实验现象可知,该白色固体中一定含有_____ ,(填化学式,下同)一定不含有______ ,可能含有_______ 。
(3)如果要进一步确定可能存在的物质,进行的实验方法是___ 。
①取少量固体粉末,加入盛有足量水的烧杯中,充分搅拌静置后,底部白色沉淀,上层为
②继续往烧杯中加入足量稀硝酸,白色沉淀完全消失;并有气泡产生。
③取少量②中溶液滴加Ba(NO3)2溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解。
(1)请写出上述第②步中,白色沉淀与稀硝酸反应的方程式
(2)根据以上实验现象可知,该白色固体中一定含有
(3)如果要进一步确定可能存在的物质,进行的实验方法是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】2019年3月21日是第二十七届“世界水日”,保护水资源,合理利用废水节省水资源,加强废水的回收利用已被越来越多的人所关注。已知:某无色废水中可能含有H+、NH4+、Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品100 ,进行了三组实验,其操作和有关图象如下图所示,请回答下列问题:
,进行了三组实验,其操作和有关图象如下图所示,请回答下列问题:
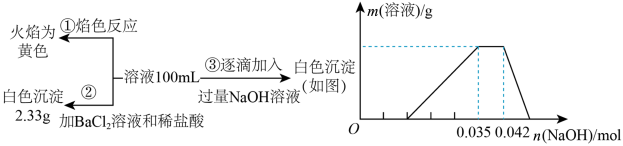
(1)根据上述3组实验可以分析废水中一定不存在的阴离子是_______ ,一定存在的阳离子是____________________ 。
(2)写出实验③图象中沉淀达到最大量且质量不再发生变化阶段发生反应的离子反应方程式:_________________________ 。
(3)分析图象,在原溶液中c(NH4+)与c(Al3+)的比值为__________ ,所得沉淀的最大质量是__________ g。
(4)若通过实验确定原废水中c(Na+)=0.14mol/L,试判断原废水中NO3-是否存在?__________ (填“存在”“不存在”或“不确定”)。若存在,c(NO3-)=__________ mol/L。(若不存在或不确定则此空不填)。
 ,进行了三组实验,其操作和有关图象如下图所示,请回答下列问题:
,进行了三组实验,其操作和有关图象如下图所示,请回答下列问题:
(1)根据上述3组实验可以分析废水中一定不存在的阴离子是
(2)写出实验③图象中沉淀达到最大量且质量不再发生变化阶段发生反应的离子反应方程式:
(3)分析图象,在原溶液中c(NH4+)与c(Al3+)的比值为
(4)若通过实验确定原废水中c(Na+)=0.14mol/L,试判断原废水中NO3-是否存在?
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某无色溶液可能含有以下离子中的某几种:Na+、Mg2+、Cu2+、Ba2+、H+、Cl-、SO 、CO
、CO 。现分别进行如下实验:
。现分别进行如下实验:
a.取10mL溶液,加入Na2CO3溶液至过量,产生112mL气体(已换算为标准状况,假定产生的气
体全部逸出),并有白色沉淀产生。
b.取10mL溶液,加入AgNO3溶液,有白色沉淀产生。
c.取10mL溶液,加入过量氯化钡溶液,过滤、洗涤、干燥,称得沉淀质量为4.66g。
d.取10mL溶液,向其中加入2mol•L-1的NaOH溶液,一段时间后,产生白色沉淀,恰好完全沉淀时,共消耗NaOH溶液15mL。
请回答下列问题:
(1)该无色溶液中一定含有___ ,一定不含___ ,可能含有__ 。
(2)溶液中c(Mg2+)=___ mol•L-1。
(3)检验可能含有的离子的实验方法是___ 。
 、CO
、CO 。现分别进行如下实验:
。现分别进行如下实验:a.取10mL溶液,加入Na2CO3溶液至过量,产生112mL气体(已换算为标准状况,假定产生的气
体全部逸出),并有白色沉淀产生。
b.取10mL溶液,加入AgNO3溶液,有白色沉淀产生。
c.取10mL溶液,加入过量氯化钡溶液,过滤、洗涤、干燥,称得沉淀质量为4.66g。
d.取10mL溶液,向其中加入2mol•L-1的NaOH溶液,一段时间后,产生白色沉淀,恰好完全沉淀时,共消耗NaOH溶液15mL。
请回答下列问题:
(1)该无色溶液中一定含有
(2)溶液中c(Mg2+)=
(3)检验可能含有的离子的实验方法是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子有_______ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是_______ ,有关的离子方程式为_______ 。
(3)取(2)中的滤液,加入过量的NaOH溶液,出现白色沉淀,说明液中肯定有_______ , 有关的离子方程式为_______ 。
(4)原溶液可能大量存在的阴离子是下列的_______ 。
A.Cl- B. C.
C.
(1)不做任何实验就可以肯定原溶液中不存在的离子有
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取(2)中的滤液,加入过量的NaOH溶液,出现白色沉淀,说明液中肯定有
(4)原溶液可能大量存在的阴离子是下列的
A.Cl- B.
 C.
C.
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】按要求完成下列各题。
(1)某无色透明溶液中可能大量存在Ag+,Mg2+,Cu2+,Fe3+中的一种或几种离子。
①不做任何实验就可以肯定原溶液中不存在的离子有_______ 。
②取少量原溶液加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,有关的离子反应方程式为_______ 。
③取②的滤液加入过量NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子有_______ 。
④原溶液中可能大量存在的阴离子是_______
A.Cl- B. C.
C. D.OH-
D.OH-
(2)根据要求完成下列方程式
①用单线桥法表示以下反应电子转移的方向和数目_______ 。
2Al+3CuSO4=3Cu+Al2(SO4)3
②用双线桥法表示以下反应电子转移的方向和数目_______ 。
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
该反应的离子方程式为:_______ 。
(1)某无色透明溶液中可能大量存在Ag+,Mg2+,Cu2+,Fe3+中的一种或几种离子。
①不做任何实验就可以肯定原溶液中不存在的离子有
②取少量原溶液加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,有关的离子反应方程式为
③取②的滤液加入过量NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子有
④原溶液中可能大量存在的阴离子是
A.Cl- B.
 C.
C. D.OH-
D.OH-(2)根据要求完成下列方程式
①用单线桥法表示以下反应电子转移的方向和数目
2Al+3CuSO4=3Cu+Al2(SO4)3
②用双线桥法表示以下反应电子转移的方向和数目
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
该反应的离子方程式为:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】现有A、B、C、D、E六种元素原子序数依次增大;只有E不是短周期元素;对其分别描述如下表:
(1)元素D的最高价氧化物为无色液体, 0.25mol该物质与一定量水混合得到一种稀溶液,并放出Q kJ的热量。写出该反应的热化学方程式______________________ ;
(2)用一个化学方程式表示C与E的金属性强弱_____________________________ 。
(3)A与B两种元素组成一种阳离子,检验某溶液中含有该离子的方法是__________ 。
(4)含C的某化合物可用作净水剂,该物质的水溶液呈酸性,其原因是________________ 。(用离子方程式表示)
(5)E单质在海水中易被腐蚀,写出正极反应式:______________________ 。
| 元素编号 | 元素描述 |
| A | 单质是最理想的气体燃料;而氧化物是最常用的液态灭火剂 |
| B | 氧化物之一不但能造成酸雨,还能造成光化学烟雾 |
| C | 所处周期数、族序数都与电子层数相等 |
| D | 最高化合价为+7 |
| E | 目前用量最大,应用最广泛的金属 |
(2)用一个化学方程式表示C与E的金属性强弱
(3)A与B两种元素组成一种阳离子,检验某溶液中含有该离子的方法是
(4)含C的某化合物可用作净水剂,该物质的水溶液呈酸性,其原因是
(5)E单质在海水中易被腐蚀,写出正极反应式:
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】味精的鲜味物质是谷氨酸钠,杂质主要是氯化钠。某学生欲测定味精中食盐的含量。
(1)下面是该学生所做的有关实验,请补写缺失的实验步骤②和④。
①称取某品牌的袋装味精样品5.0g,并溶于蒸馏水;
②___________________________________________________________________
③过滤;
④____________________________________________________________________
⑤将沉淀烘干、称量,测得固体质量为2.9g。
(2)根据上述实验步骤回答下列有关问题:
①过滤操作所需要的玻璃仪器有____________________________________________
②验沉淀是否洗净的方法是_____________________________________________
③若味精包装上标注“谷氨酸钠含量≥80%,NaCl含量≤20%”,问此样品是否符合产品标注的质量分数?________________ (填“符合”或“不符合”)。
(3)若有甲、乙两学生分别做了这个实验,甲学生认真地做了一次实验,就取得了实验数据,而乙学生认真地做了两次实验,取两次数据的平均值作为实验的测定数据,你认为_____ 学生的方法更合理(填“甲”或“乙”)。
(1)下面是该学生所做的有关实验,请补写缺失的实验步骤②和④。
①称取某品牌的袋装味精样品5.0g,并溶于蒸馏水;
②
③过滤;
④
⑤将沉淀烘干、称量,测得固体质量为2.9g。
(2)根据上述实验步骤回答下列有关问题:
①过滤操作所需要的玻璃仪器有
②验沉淀是否洗净的方法是
③若味精包装上标注“谷氨酸钠含量≥80%,NaCl含量≤20%”,问此样品是否符合产品标注的质量分数?
(3)若有甲、乙两学生分别做了这个实验,甲学生认真地做了一次实验,就取得了实验数据,而乙学生认真地做了两次实验,取两次数据的平均值作为实验的测定数据,你认为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D 4种可溶性盐,它们的阳离子可能分别是Ca2+、Ag+、Na+、Cu2+中的某一种,阴离子可能分别是NO3-、SO42-、Cl-、CO32-中的某一种。
①若把4种盐分别溶解于盛有蒸馏水的4支试管中,均得澄清溶液,只有B盐的溶液呈蓝色。
②若向①的4支试管中分别加盐酸,C溶液中有沉淀产生,A溶液中有无色无味气体逸出。
(1)根据①②的事实推断B、C的化学式分别为_________ 、___________
(2)写出A与D反应的化学方程式:______________________________________ ;
(3)若想从A与D反应后的混合物中分别提取两种固体产物,需要进行的实验操作是_________ 和________ .
①若把4种盐分别溶解于盛有蒸馏水的4支试管中,均得澄清溶液,只有B盐的溶液呈蓝色。
②若向①的4支试管中分别加盐酸,C溶液中有沉淀产生,A溶液中有无色无味气体逸出。
(1)根据①②的事实推断B、C的化学式分别为
(2)写出A与D反应的化学方程式:
(3)若想从A与D反应后的混合物中分别提取两种固体产物,需要进行的实验操作是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】磺酰氯(SO2Cl2)是一种重要的有机合成试剂,实验室可利用SO2与Cl2在活性炭作用下反应制取少量的SO2Cl2,装置如下图所示(有些夹持装置省略)。已知SO2Cl2的熔点为-54.1 ℃,沸点为69.1 ℃,遇水能发生剧烈的水解反应,并产生白雾。
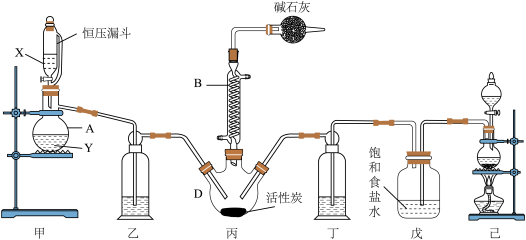
(1)单独检验己装置气密性的方法是:_______ 。
(2)由仪器B的使用可知SO2与Cl2反应的ΔH_______ 0(填“>”或“<”),仪器C的作用是_______ 。
(3)试剂X、Y的组合最好是________ 。
a.18.4 mol/L H2SO4+Cu b.4 mol/L HNO3+Na2SO3 c.60% H2SO4+K2SO3
(4)反应结束后,将丙中产物分离的实验操作是_______ 。
(5)分离产物后,向获得的SO2Cl2中加入足量NaOH溶液,振荡、静止得到无色溶液w。
①写出该反应的离子方程式:________ ;
②检验溶液w中存在Cl-的方法是________ 。
(6)SO2Cl2可以作为锂离子电池的正极活性材质,已知电池反应为:2Li+SO2Cl2=2LiCl +SO2↑。则电池工作时,正极的电极反应式为_________ 。

(1)单独检验己装置气密性的方法是:
(2)由仪器B的使用可知SO2与Cl2反应的ΔH
(3)试剂X、Y的组合最好是
a.18.4 mol/L H2SO4+Cu b.4 mol/L HNO3+Na2SO3 c.60% H2SO4+K2SO3
(4)反应结束后,将丙中产物分离的实验操作是
(5)分离产物后,向获得的SO2Cl2中加入足量NaOH溶液,振荡、静止得到无色溶液w。
①写出该反应的离子方程式:
②检验溶液w中存在Cl-的方法是
(6)SO2Cl2可以作为锂离子电池的正极活性材质,已知电池反应为:2Li+SO2Cl2=2LiCl +SO2↑。则电池工作时,正极的电极反应式为
您最近半年使用:0次



