现有A、B、C、D、E六种元素原子序数依次增大;只有E不是短周期元素;对其分别描述如下表:
(1)元素D的最高价氧化物为无色液体, 0.25mol该物质与一定量水混合得到一种稀溶液,并放出Q kJ的热量。写出该反应的热化学方程式______________________ ;
(2)用一个化学方程式表示C与E的金属性强弱_____________________________ 。
(3)A与B两种元素组成一种阳离子,检验某溶液中含有该离子的方法是__________ 。
(4)含C的某化合物可用作净水剂,该物质的水溶液呈酸性,其原因是________________ 。(用离子方程式表示)
(5)E单质在海水中易被腐蚀,写出正极反应式:______________________ 。
| 元素编号 | 元素描述 |
| A | 单质是最理想的气体燃料;而氧化物是最常用的液态灭火剂 |
| B | 氧化物之一不但能造成酸雨,还能造成光化学烟雾 |
| C | 所处周期数、族序数都与电子层数相等 |
| D | 最高化合价为+7 |
| E | 目前用量最大,应用最广泛的金属 |
(2)用一个化学方程式表示C与E的金属性强弱
(3)A与B两种元素组成一种阳离子,检验某溶液中含有该离子的方法是
(4)含C的某化合物可用作净水剂,该物质的水溶液呈酸性,其原因是
(5)E单质在海水中易被腐蚀,写出正极反应式:
10-11高三上·福建厦门·期中 查看更多[1]
(已下线)2011届福建省厦门市双十中学高三上学期期中考试化学试卷
更新时间:2016-12-09 01:12:25
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有氧化性。下述为相关实验步骤和实验现象。请回答:
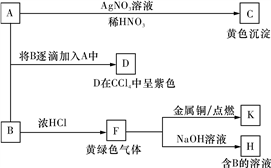
(1)写出C、D的化学式或分子式:__________ 、____________ 。
(2)指出D中所含元素在周期表中的位置________________ ,指出K的水溶液由稀到浓的颜色变化________________ 。
(3)将SO2气体通入D溶液,D溶液变为无色,生成两种强酸。写出该反应的化学方程式:________________________________________________________________________ 。
(4)F与粗硅加热生成__________ (填分子式),该物质经蒸馏提纯后在1 100 ℃下与氢气反应生成高纯硅,写出后一步骤反应的化学方程式:_____________________________ 。
(5)0.25 mol F缓慢通入含有0.1 mol FeBr2、0.1 mol FeI2的混合溶液中,充分反应,试用一个离子方程式表示总反应:__________________________________________ 。
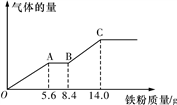
(6)某稀硫酸和稀硝酸的混合溶液100 mL,将其平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g铜粉;向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化关系如图所示(假设硝酸的还原产物为NO气体)。则原混合溶液中NO3-的物质的量为__________ ,硫酸的物质的量浓度为______________ 。

(1)写出C、D的化学式或分子式:
(2)指出D中所含元素在周期表中的位置
(3)将SO2气体通入D溶液,D溶液变为无色,生成两种强酸。写出该反应的化学方程式:
(4)F与粗硅加热生成
(5)0.25 mol F缓慢通入含有0.1 mol FeBr2、0.1 mol FeI2的混合溶液中,充分反应,试用一个离子方程式表示总反应:
(6)某稀硫酸和稀硝酸的混合溶液100 mL,将其平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g铜粉;向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化关系如图所示(假设硝酸的还原产物为NO气体)。则原混合溶液中NO3-的物质的量为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A-J分别表示中学化学中常见的一种物质,它们之间相互关系如图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。请填写下列空白:

(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中位置_________
(2)写出检验D溶液中阳离子的方法____ 。
(3)写出反应④的离子方程式________ 。
(4)若向气体K的水溶液中加入盐酸,使其恰好完全反应,所得溶液的pH_____ 7(填“>”、“<”或“=”),用离子方程式表示其原因:______ ;
(5)若向气体K的0.1mol/L水溶液中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,则所得溶液中各离子物质的量浓度由大到小 的关系是______ 。

(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中位置
(2)写出检验D溶液中阳离子的方法
(3)写出反应④的离子方程式
(4)若向气体K的水溶液中加入盐酸,使其恰好完全反应,所得溶液的pH
(5)若向气体K的0.1mol/L水溶液中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,则所得溶液中各离子物质的量浓度
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:
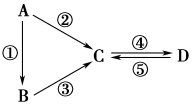
(1)若A是淡黄色固体,C、D是氧化物,C是造成酸雨的主要物质,但C也有其广泛的用途,写出其中的2个用途:__________________________ 。
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气的主要成分,写出该反应的化学方程式:________________ 。
(3)若D物质具有两性,②、③反应均要用强碱溶液。如④反应时通入过量的一种引起温室效应的主要气体,写出该气体的电子式:_________ ,A的元素在周期表中的位置:__________________ 。
(4)若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性。写出②反应的化学方程式:_____________________ 。D的化学式是______ 。

(1)若A是淡黄色固体,C、D是氧化物,C是造成酸雨的主要物质,但C也有其广泛的用途,写出其中的2个用途:
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气的主要成分,写出该反应的化学方程式:
(3)若D物质具有两性,②、③反应均要用强碱溶液。如④反应时通入过量的一种引起温室效应的主要气体,写出该气体的电子式:
(4)若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性。写出②反应的化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】氮的氧化物是造成大气污染的主要物质。研究氮氧化物的反应机理对消除环境污染有重要意义。
(1)NO在空气中存在如下反应:2NO(g)+O2(g)=2NO2(g)△H,上述反应分两步完成,其反应历程如下图所示:
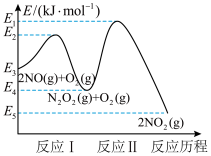
回答下列问题:
①写出反应I的热化学方程式_________ 。
②反应I和反应II中,一个是快反应,会快速建立平衡状态,而另一个是慢反应。决定2NO(g)+O2(g)=2NO2(g)反应速率的是_______ (填“反应I”或“反应II”);对该反应体系升高温度,发现总反应速率反而变慢,其原因可能是________ (反应未使用催化剂)。
(2)用活性炭还原法处理氮氧化物的有关反应为:C(s)+2NO(g) N2(g)+CO2(g)。向恒容密闭容器中加入一定量的活性炭和NO,T℃时,各物质起始浓度及l0 min和20 min各物质平衡浓度如表所示:
N2(g)+CO2(g)。向恒容密闭容器中加入一定量的活性炭和NO,T℃时,各物质起始浓度及l0 min和20 min各物质平衡浓度如表所示:
①T℃时,该反应的平衡常数为 ________ (保留两位有效数字)。
②在l0 min时,若只改变某一条件使平衡发生移动,20 min时重新达到平衡,则改变的条件是________
③在20 min时,保持温度和容器体积不变再充入NO和N2,使二者的浓度均增加至原来的两倍,此时反应v正____ v逆(填“>”、“<”或“=”)。
(3)NO2存在如下平衡:2NO2(g)⇌N2O4(g) △H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系:v(NO2)=k1·p2(NO2),v(N2O4)=k2·p(N2O4),相应的速率与其分压关系如图所示。
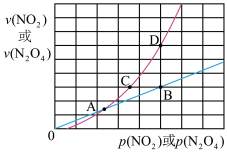
一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=____ ;在上图标出点中,指出能表示反应达到平衡状态的点是 ______ 。
(1)NO在空气中存在如下反应:2NO(g)+O2(g)=2NO2(g)△H,上述反应分两步完成,其反应历程如下图所示:

回答下列问题:
①写出反应I的热化学方程式
②反应I和反应II中,一个是快反应,会快速建立平衡状态,而另一个是慢反应。决定2NO(g)+O2(g)=2NO2(g)反应速率的是
(2)用活性炭还原法处理氮氧化物的有关反应为:C(s)+2NO(g)
 N2(g)+CO2(g)。向恒容密闭容器中加入一定量的活性炭和NO,T℃时,各物质起始浓度及l0 min和20 min各物质平衡浓度如表所示:
N2(g)+CO2(g)。向恒容密闭容器中加入一定量的活性炭和NO,T℃时,各物质起始浓度及l0 min和20 min各物质平衡浓度如表所示:| 浓度/mol/L 时间/min | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.040 | 0.030 | 0.030 |
| 20 | 0.032 | 0.034 | 0.017 |
②在l0 min时,若只改变某一条件使平衡发生移动,20 min时重新达到平衡,则改变的条件是
③在20 min时,保持温度和容器体积不变再充入NO和N2,使二者的浓度均增加至原来的两倍,此时反应v正
(3)NO2存在如下平衡:2NO2(g)⇌N2O4(g) △H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系:v(NO2)=k1·p2(NO2),v(N2O4)=k2·p(N2O4),相应的速率与其分压关系如图所示。

一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】氢气是一种理想的绿色能源。利用生物发酵得到的乙醇制取氢气,具有良好的应用前景。乙醇水蒸气重整制氢的部分反应过程如下图所示:

已知:反应I和反应II的平衡常数随温度变化曲线如图所示。

(1)反应I中,1 mol CH3CH2OH(g)参与反应后的热量变化是256 kJ。
① H2O的电子式是:_________________ 。
② 反应I的热化学方程式是:___________________________ 。
(2)反应II,在进气比[n(CO) : n(H2O)]不同时,测得相应的CO的平衡转化率见下图(各点对应的反应温度可能相同,也可能不同)。

① 图中D、E两点对应的反应温度分别为TD和TE。判断:TD_______ TE(填“<” “=”或“>”)。
② 经分析,A、E和G三点对应的反应温度相同,其原因是A、E和G三点对应的____ 相同。
③ 当不同的进气比达到相同的CO平衡转化率时,对应的反应温度和进气比的关系是______ 。
(3)反应III,在经CO2饱和处理的KHCO3电解液中,电解活化CO2制备乙醇的原理如下图所示。

① 阴极的电极反应式是__________________________ 。
② 从电解后溶液中分离出乙醇的操作方法是______________ 。

已知:反应I和反应II的平衡常数随温度变化曲线如图所示。

(1)反应I中,1 mol CH3CH2OH(g)参与反应后的热量变化是256 kJ。
① H2O的电子式是:
② 反应I的热化学方程式是:
(2)反应II,在进气比[n(CO) : n(H2O)]不同时,测得相应的CO的平衡转化率见下图(各点对应的反应温度可能相同,也可能不同)。

① 图中D、E两点对应的反应温度分别为TD和TE。判断:TD
② 经分析,A、E和G三点对应的反应温度相同,其原因是A、E和G三点对应的
③ 当不同的进气比达到相同的CO平衡转化率时,对应的反应温度和进气比的关系是
(3)反应III,在经CO2饱和处理的KHCO3电解液中,电解活化CO2制备乙醇的原理如下图所示。

① 阴极的电极反应式是
② 从电解后溶液中分离出乙醇的操作方法是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】 溶液与
溶液与 锌粉在量热计中充分反应。测得反应前温度为
锌粉在量热计中充分反应。测得反应前温度为 ,反应后最高温度为
,反应后最高温度为 。
。
已知:反应前后,溶液的比热容均近似为 、溶液的密度均近似为
、溶液的密度均近似为 ,忽略溶液体积、质量变化和金属吸收的热量。请计算:
,忽略溶液体积、质量变化和金属吸收的热量。请计算:
(1)反应放出的热量Q=_______ J。
(2)反应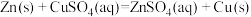 的
的
_______  。
。
(3)在金催化剂表面水煤气变换的反应历程如图所示,其中吸附在金催化剂表面的物种用*标注。
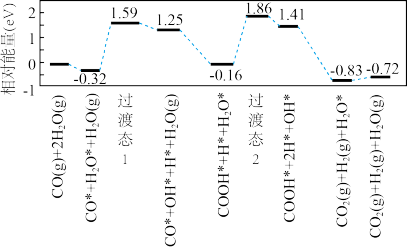
则水煤气变换反应的
_______ 0(填“大于”“等于”或“小于”)。该历程中最大能垒(活化能)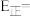
_______  ,写出该步骤的化学方程式:
,写出该步骤的化学方程式:_______ 。
(4)可以证明乙酸是弱酸的事实是_______(填序号)
(5)有下列物质的溶液:a.CH3COOH b.HCl c.H2SO4 d.NaHSO4。若四种溶液的物质的量浓度相同,其c(H+)由大到小顺序为_______ (用字母序号表示,下同)。若四种溶液的c(H+)相同,其物质的量浓度由大到小顺序为_______ 。
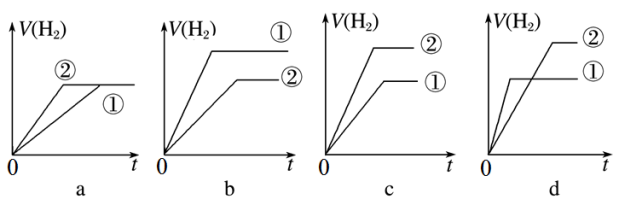
(6)常温下,有 相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是_______ (填字母)。(①表示盐酸,②表示醋酸)
 溶液与
溶液与 锌粉在量热计中充分反应。测得反应前温度为
锌粉在量热计中充分反应。测得反应前温度为 ,反应后最高温度为
,反应后最高温度为 。
。已知:反应前后,溶液的比热容均近似为
 、溶液的密度均近似为
、溶液的密度均近似为 ,忽略溶液体积、质量变化和金属吸收的热量。请计算:
,忽略溶液体积、质量变化和金属吸收的热量。请计算:(1)反应放出的热量Q=
(2)反应
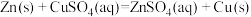 的
的
 。
。(3)在金催化剂表面水煤气变换的反应历程如图所示,其中吸附在金催化剂表面的物种用*标注。

则水煤气变换反应的

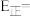
 ,写出该步骤的化学方程式:
,写出该步骤的化学方程式:(4)可以证明乙酸是弱酸的事实是_______(填序号)
| A.乙酸钠水溶液显碱性 |
| B.在乙酸水溶液中含有未电离的乙酸分子 |
| C.乙酸与Na2CO3溶液反应放出CO2气体 |
| D.常温下,0.1 mol·L-1的乙酸水溶液pH为3 |
(6)常温下,有
 相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】金属的腐蚀与防腐是科学研究的重点领域,现代防腐技术日益受到关注。回答下列问题:
(1)“经远舰”在海底多年,舰体腐蚀严重。舰体发生电化学腐蚀时,其正极的电极反应式为___________ (已知正常海水呈弱碱性);为保护舰体,科研人员提出将舰体与电源___________ (填“正极”或“负极”)相连,这种保护方法称为___________ 。
(2)金属铬具有优良的抗腐蚀性能。常在钢铁表面镀一层铬达到防腐的目的。一般电镀过程中,金属铬作为___________ (填“阳极”或“阴极”)材料。工业上常用沉淀法处理含 (橙色)和
(橙色)和 (黄色)的电镀废水,工艺流程如图所示:
(黄色)的电镀废水,工艺流程如图所示:
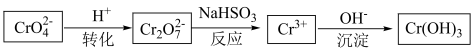
①“转化”过程存在平衡,下列能说明转化达到平衡状态的是___________ 。
A.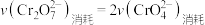 B.溶液颜色保持不变
B.溶液颜色保持不变
C. D.含铬微粒的总浓度保持不变
D.含铬微粒的总浓度保持不变
②“反应”过程中发生反应的离子方程式为___________ 。
③“沉淀”过程中,室温下当 恰好沉淀完全时,溶液的pH=
恰好沉淀完全时,溶液的pH=___________ 。(已知: ,c(Cr3+)≤10-5mol/L时沉淀完全)
,c(Cr3+)≤10-5mol/L时沉淀完全)
(3)钼酸钠和苯并三氮䂳(BTA)的混合液常作为碳钢的缓蚀剂。常温下,碳钢在不同浓度的硫酸和缓蚀剂介质中的腐蚀速率[单位: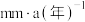 ]数据如图所示。
]数据如图所示。
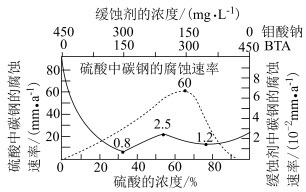
①要使碳钢的缓蚀效果最优,钼酸钠和BTA的浓度比应为___________ 。
②硫酸中碳钢的最高腐蚀速率和缓蚀剂中碳钢的最低腐蚀速率之比为___________ 。
(1)“经远舰”在海底多年,舰体腐蚀严重。舰体发生电化学腐蚀时,其正极的电极反应式为
(2)金属铬具有优良的抗腐蚀性能。常在钢铁表面镀一层铬达到防腐的目的。一般电镀过程中,金属铬作为
 (橙色)和
(橙色)和 (黄色)的电镀废水,工艺流程如图所示:
(黄色)的电镀废水,工艺流程如图所示:
①“转化”过程存在平衡,下列能说明转化达到平衡状态的是
A.
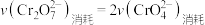 B.溶液颜色保持不变
B.溶液颜色保持不变C.
 D.含铬微粒的总浓度保持不变
D.含铬微粒的总浓度保持不变②“反应”过程中发生反应的离子方程式为
③“沉淀”过程中,室温下当
 恰好沉淀完全时,溶液的pH=
恰好沉淀完全时,溶液的pH= ,c(Cr3+)≤10-5mol/L时沉淀完全)
,c(Cr3+)≤10-5mol/L时沉淀完全)(3)钼酸钠和苯并三氮䂳(BTA)的混合液常作为碳钢的缓蚀剂。常温下,碳钢在不同浓度的硫酸和缓蚀剂介质中的腐蚀速率[单位:
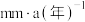 ]数据如图所示。
]数据如图所示。
①要使碳钢的缓蚀效果最优,钼酸钠和BTA的浓度比应为
②硫酸中碳钢的最高腐蚀速率和缓蚀剂中碳钢的最低腐蚀速率之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】用如下装置进行实验:
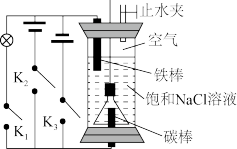
(1)关闭上端止水夹,接通K1,一段时间后用压强传感器测得装置上部压强减小,铁棒表面出现锈迹。则铁棒主要发生,_______ 腐蚀(填“析氢”或“吸氧”);此时碳棒上的电极反应式为:_______ 。
(2)Na2FeO4是一种新型净水剂,可以通过以下反应制备:Fe(OH)2+2Cl2+6NaOH=Na2FeO4+4NaCl+4H2O,为制得Na2FeO4,用一支倒扣的漏斗罩住碳极,如图,首先打开止水夹,断开K1、K2,接通K3。几分钟后,漏斗中产生的气体是_______ ;此时发生的总反应化学方程式为:_______ 。
(3)断开K1、K3,接通K2。阳极的电极反应式为_______ 。打开漏斗上口软塞,发生(2)中反应生成Na2FeO4。
(4)Na2FeO4有强氧化性可用于杀菌消毒,还可净水,其净水的原理是_______ 。

(1)关闭上端止水夹,接通K1,一段时间后用压强传感器测得装置上部压强减小,铁棒表面出现锈迹。则铁棒主要发生,
(2)Na2FeO4是一种新型净水剂,可以通过以下反应制备:Fe(OH)2+2Cl2+6NaOH=Na2FeO4+4NaCl+4H2O,为制得Na2FeO4,用一支倒扣的漏斗罩住碳极,如图,首先打开止水夹,断开K1、K2,接通K3。几分钟后,漏斗中产生的气体是
(3)断开K1、K3,接通K2。阳极的电极反应式为
(4)Na2FeO4有强氧化性可用于杀菌消毒,还可净水,其净水的原理是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】铁生锈是比较常见的现象,某实验小组,为研究铁生锈的条件,设计了以下快速易行的方法:首先检查制氧气装置的气密性,然后按图连接好装置,点燃酒精灯给药品加热,持续3分钟左右,观察到的实验现象为:①直形管中用蒸馏水浸过的光亮铁丝表面颜色变得灰暗,发生锈蚀;②直形管中干燥的铁丝表面依然光亮,没有发生锈蚀;③烧杯中潮湿的铁丝依然光亮。
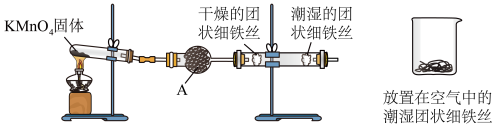
试回答以下问题:
(1)由于与接触的介质不同,金属腐蚀分成不同类型,本实验中铁生锈属于___ ,能表示其原理的正极反应式为_________ ,负极反应式为________ ;
(2)仪器A的名称为____ ,其中装的药品可以是____ ,其作用是_____________ ;
(3)由实验可知,该类铁生锈的条件为_____ 。决定铁生锈快慢的一个重要因素是_______ 。

试回答以下问题:
(1)由于与接触的介质不同,金属腐蚀分成不同类型,本实验中铁生锈属于
(2)仪器A的名称为
(3)由实验可知,该类铁生锈的条件为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】有一无色透明溶液200mL,欲确定是否含有下列离子: 、
、 、
、 、
、 、
、 、
、 、
、 ,
, 、
、 、
、 、
、 、
、 。分成四等份,取一份溶液进行如下实验:
。分成四等份,取一份溶液进行如下实验:
①加几滴甲基橙溶液变红色;
②加入足量 溶液,生成白色沉淀和溶液A;在溶液A中加
溶液,生成白色沉淀和溶液A;在溶液A中加 溶液有稳定的白色沉淀生成,且不溶于稀硝酸;
溶液有稳定的白色沉淀生成,且不溶于稀硝酸;
③加热浓缩,加入Cu片和稀盐酸,有无色气体产生,气体遇空气变成红棕色,溶液中阴离子种类不变;
④加入足量NaOH溶液,生成白色沉淀和溶液B,溶液B中通入过量 ,加热、过滤、洗涤、灼烧,得到白色沉淀(1.02g)。
,加热、过滤、洗涤、灼烧,得到白色沉淀(1.02g)。
回答下列问题:
(1)溶液中肯定存在的阴离子是_______ 。
(2)如何实验检验其中的 ,
,_______ ,说明 存在。
存在。
(3)为了进一步确定其它离子,应该补充的实验为(不必写详细操作步骤)_______ 。
(4)步骤④中“加入足量NaOH溶液”,共有_______ 种阳离子发生反应。
(5)原溶液中
_______  。
。
(6)步骤④中加热的目的是_______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 ,
, 、
、 、
、 、
、 、
、 。分成四等份,取一份溶液进行如下实验:
。分成四等份,取一份溶液进行如下实验:①加几滴甲基橙溶液变红色;
②加入足量
 溶液,生成白色沉淀和溶液A;在溶液A中加
溶液,生成白色沉淀和溶液A;在溶液A中加 溶液有稳定的白色沉淀生成,且不溶于稀硝酸;
溶液有稳定的白色沉淀生成,且不溶于稀硝酸;③加热浓缩,加入Cu片和稀盐酸,有无色气体产生,气体遇空气变成红棕色,溶液中阴离子种类不变;
④加入足量NaOH溶液,生成白色沉淀和溶液B,溶液B中通入过量
 ,加热、过滤、洗涤、灼烧,得到白色沉淀(1.02g)。
,加热、过滤、洗涤、灼烧,得到白色沉淀(1.02g)。回答下列问题:
(1)溶液中肯定存在的阴离子是
(2)如何实验检验其中的
 ,
, 存在。
存在。(3)为了进一步确定其它离子,应该补充的实验为(不必写详细操作步骤)
(4)步骤④中“加入足量NaOH溶液”,共有
(5)原溶液中

 。
。(6)步骤④中加热的目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】工业上冶炼冰铜(mCu2O·nFeS)可得到粗铜,再以粗铜为原料制备硫酸铜晶体。
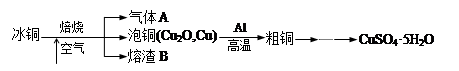
完成下列填空:
(1)气体A中的大气污染物可选用下列试剂中的_______ (填序号)吸收。
a. 浓H2SO4 b. 浓HNO3 c. NaOH溶液 d. 氨水
(2)用稀H2SO4 浸泡熔渣B,取少量所得溶液,滴加____ (填物质名称)溶液后呈红色,说明溶液中存在Fe3+,检验溶液中还存在Fe2+的方法是___ (注明试剂、现象)。
实验室可用图的装置完成泡铜冶炼粗铜的反应。
(3)泡铜冶炼粗铜的化学方程式是____________________________ 。
(4)装置中镁带的作用是____ 。泡铜和铝粉混合物表面覆盖少量白色固体a,
a是__ (填名称)。沙子能否换成水?__ (填“能”或“不能”)。
(5)用滴定法测定CuSO4·5H2O的含量。取a g试样配成100 mL溶液,取20.00mL用c mol /L 滴定剂(H2Y2–,滴定剂不与杂质反应)滴定至终点,消耗滴定剂bmL,滴定反应:Cu2++ H2Y2–=CuY2–+ 2H+。则CuSO4·5H2O质量分数的表达式是_______ 。
(6)下列操作会导致CuSO4·5H2O含量的测定结果偏高的是_____________ 。
a.滴定临近终点时,用洗瓶中的蒸馏水洗下滴定管尖嘴口的半滴标准液至锥形瓶中
b.滴定管用蒸馏水洗涤后,直接注入待测液,取20.00mL进行滴定
c.滴定前,滴定管尖端有气泡,滴定后气泡消失
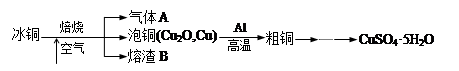
完成下列填空:
(1)气体A中的大气污染物可选用下列试剂中的
a. 浓H2SO4 b. 浓HNO3 c. NaOH溶液 d. 氨水
(2)用稀H2SO4 浸泡熔渣B,取少量所得溶液,滴加
实验室可用图的装置完成泡铜冶炼粗铜的反应。

(3)泡铜冶炼粗铜的化学方程式是
(4)装置中镁带的作用是
a是
(5)用滴定法测定CuSO4·5H2O的含量。取a g试样配成100 mL溶液,取20.00mL用c mol /L 滴定剂(H2Y2–,滴定剂不与杂质反应)滴定至终点,消耗滴定剂bmL,滴定反应:Cu2++ H2Y2–=CuY2–+ 2H+。则CuSO4·5H2O质量分数的表达式是
(6)下列操作会导致CuSO4·5H2O含量的测定结果偏高的是
a.滴定临近终点时,用洗瓶中的蒸馏水洗下滴定管尖嘴口的半滴标准液至锥形瓶中
b.滴定管用蒸馏水洗涤后,直接注入待测液,取20.00mL进行滴定
c.滴定前,滴定管尖端有气泡,滴定后气泡消失
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】Ⅰ.写出下列反应的离子方程式:
(1)将鸡蛋壳在醋酸中溶解有气泡产生:_____________________________________________ ;
(2)CuSO4溶液与Ba(OH)2溶液混合:________________________________________ 。
Ⅱ.对一份稀溶液作初步分析后发现,溶液无色、澄清,其可能含有 、Na+、
、Na+、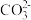 、H+、
、H+、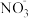 、
、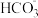 、Cl−等离子中的若干种。然后又作了如下分析,以确定这些离子是否存在。
、Cl−等离子中的若干种。然后又作了如下分析,以确定这些离子是否存在。
①用石蕊试液检测该溶液时,溶液显红色。
②取2 mL溶液用BaCl2溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。
请回答下列问题:
(1)原溶液中一定存在的离子是__________ ,一定不存在的离子是____________ 。
(2)在上述实验操作中,有错误的步骤是(填代号)______ 。对该错误改正的方法是(要作较详细的说明)_________________________________________________________ 。
(3)到目前为止,不能肯定在原溶液中是否存在的离子是____________ 。
(1)将鸡蛋壳在醋酸中溶解有气泡产生:
(2)CuSO4溶液与Ba(OH)2溶液混合:
Ⅱ.对一份稀溶液作初步分析后发现,溶液无色、澄清,其可能含有
 、Na+、
、Na+、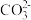 、H+、
、H+、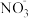 、
、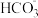 、Cl−等离子中的若干种。然后又作了如下分析,以确定这些离子是否存在。
、Cl−等离子中的若干种。然后又作了如下分析,以确定这些离子是否存在。①用石蕊试液检测该溶液时,溶液显红色。
②取2 mL溶液用BaCl2溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。
请回答下列问题:
(1)原溶液中一定存在的离子是
(2)在上述实验操作中,有错误的步骤是(填代号)
(3)到目前为止,不能肯定在原溶液中是否存在的离子是
您最近一年使用:0次



