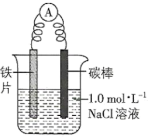
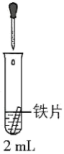
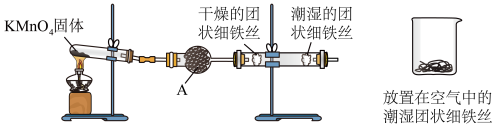
铁生锈是比较常见的现象,某实验小组,为研究铁生锈的条件,设计了以下快速易行的方法:首先检查制氧气装置的气密性,然后按图连接好装置,点燃酒精灯给药品加热,持续3分钟左右,观察到的实验现象为:①直形管中用蒸馏水浸过的光亮铁丝表面颜色变得灰暗,发生锈蚀;②直形管中干燥的铁丝表面依然光亮,没有发生锈蚀;③烧杯中潮湿的铁丝依然光亮。
试回答以下问题:
(1)由于与接触的介质不同,金属腐蚀分成不同类型,本实验中铁生锈属于___ ,能表示其原理的正极反应式为_________ ,负极反应式为________ ;
(2)仪器A的名称为____ ,其中装的药品可以是____ ,其作用是_____________ ;
(3)由实验可知,该类铁生锈的条件为_____ 。决定铁生锈快慢的一个重要因素是_______ 。

试回答以下问题:
(1)由于与接触的介质不同,金属腐蚀分成不同类型,本实验中铁生锈属于
(2)仪器A的名称为
(3)由实验可知,该类铁生锈的条件为
11-12高二下·江苏苏州·期中 查看更多[6]
云南省玉溪市第二中学2022-2023学年高二下学期期末考试化学试题云南省普洱市云南省思茅第一中学2022-2023学年高二下学期6月月考化学试题云南省景东彝族自治县第一中学2022-2023学年高二下学期期末考试化学试题海南省海南枫叶国际学校2019-2020学年高二上学期期末考试化学试题(已下线)2018年12月12日 《每日一题》人教选修4-影响钢铁腐蚀的因素(已下线)2011-2012学年江苏省苏州五中高二第二学期期中考试化学试卷
更新时间:2020-05-11 21:06:15
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】某兴趣小组用镀锌铁皮按下列流程制备七水合硫酸锌: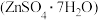 :
:
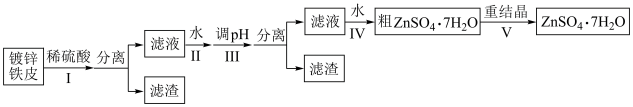
相关信息如下:金属离子形成氢氧化物沉淀的相关pH范围。
(1)镀锌铁皮的锌镀层被破坏后将在潮湿的空气中发生电化学腐蚀,相关描述正确的是______ 。
a.负极反应式为
b.负极反应式为
c.电子从铁流向锌
d.铁不但得不到保护,反而被腐蚀的更快
(2)在镀锌铁皮的锌镀层厚度的测定过程中,下列操作会导致测定结果偏高的是__ 。
a.过早判断反应终点 b.过迟判断反应终点
c.锌在酸中溶解后,铁皮未烘干就去称重
d.在测定铁皮的面积时测得面积比铁皮的实际面积大
(3)判断锌层已完全反应的依据是______________________ 。
(4)步骤Ⅱ,需加过量 ,理由是
,理由是______________________ 。
(5)步骤Ⅲ,合适的pH范围是______________________ 。
(6) 产品的纯度可用配位滴定法测定。
产品的纯度可用配位滴定法测定。
①下列关于滴定分析,正确的是____________________ 。
a.滴定前,锥形瓶和滴定管均须用标准溶液润洗
b.将标准溶液装入滴定管时,应借助烧杯或漏斗等玻璃仪器转移
c.滴定时,通常用左手控制旋塞滴加溶液,右手摇动锥形瓶,使溶液向同一方向旋转
d.滴定前滴定管尖嘴内无气泡,滴定后尖嘴内有气泡,则测得的体积比实际消耗的小
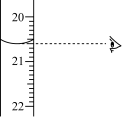
②如图中显示滴定终点时的读数是________ mL。
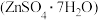 :
:
相关信息如下:金属离子形成氢氧化物沉淀的相关pH范围。
| 金属离子 | pH | |
| 开始沉淀 | 完全沉淀 | |
 | 1.5 | 2.8 |
 | 5.5 | 8.3 |
 | 6.4 | 8.2 |
(1)镀锌铁皮的锌镀层被破坏后将在潮湿的空气中发生电化学腐蚀,相关描述正确的是
a.负极反应式为

b.负极反应式为

c.电子从铁流向锌
d.铁不但得不到保护,反而被腐蚀的更快
(2)在镀锌铁皮的锌镀层厚度的测定过程中,下列操作会导致测定结果偏高的是
a.过早判断反应终点 b.过迟判断反应终点
c.锌在酸中溶解后,铁皮未烘干就去称重
d.在测定铁皮的面积时测得面积比铁皮的实际面积大
(3)判断锌层已完全反应的依据是
(4)步骤Ⅱ,需加过量
 ,理由是
,理由是(5)步骤Ⅲ,合适的pH范围是
(6)
 产品的纯度可用配位滴定法测定。
产品的纯度可用配位滴定法测定。①下列关于滴定分析,正确的是
a.滴定前,锥形瓶和滴定管均须用标准溶液润洗
b.将标准溶液装入滴定管时,应借助烧杯或漏斗等玻璃仪器转移
c.滴定时,通常用左手控制旋塞滴加溶液,右手摇动锥形瓶,使溶液向同一方向旋转
d.滴定前滴定管尖嘴内无气泡,滴定后尖嘴内有气泡,则测得的体积比实际消耗的小
②如图中显示滴定终点时的读数是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某小组同学利用如图所示装置进行铁的电化学腐蚀原理的探究实验:
(1)小组同学认为以上两种检验方法,均能证明铁发生了吸氧腐蚀。
①实验i中的现象是________ 。
②用电极反应式解释实验i中的现象:________ 。
(2)查阅资料: 具有氧化性。
具有氧化性。
①据此有同学认为仅通过ii中现象不能证明铁发生了电化学腐蚀,理由是________ 。
②进行下列实验,几分钟后的记录如下:
a.以上实验表明:在________ 条件下, 溶液可以与铁片发生反应。
溶液可以与铁片发生反应。
b.为探究 的存在对反应的影响,小组同学将铁片酸洗(用稀硫酸浸泡后洗净)后再进行实验iii,发现铁片表面产生蓝色沉淀。此补充实验表明
的存在对反应的影响,小组同学将铁片酸洗(用稀硫酸浸泡后洗净)后再进行实验iii,发现铁片表面产生蓝色沉淀。此补充实验表明 的作用是
的作用是________ 。
装置 | 分别进行的操作 | 现象 |
| i.连好装置一段时间后,向烧杯中滴加酚酞 | |
ii.连好装置一段时间后,向烧杯中滴加 溶液 溶液 | 铁片表面产生蓝色沉淀 |
①实验i中的现象是
②用电极反应式解释实验i中的现象:
(2)查阅资料:
 具有氧化性。
具有氧化性。①据此有同学认为仅通过ii中现象不能证明铁发生了电化学腐蚀,理由是
②进行下列实验,几分钟后的记录如下:
实验 | 滴管 | 试管 | 现象 |
| 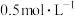  溶液 溶液 | iii.蒸馏水 | 无明显变化 |
iv.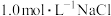 溶液 溶液 | 铁片表面产生大量蓝色沉淀 | ||
v. 溶液 溶液 | 无明显变化 |
 溶液可以与铁片发生反应。
溶液可以与铁片发生反应。b.为探究
 的存在对反应的影响,小组同学将铁片酸洗(用稀硫酸浸泡后洗净)后再进行实验iii,发现铁片表面产生蓝色沉淀。此补充实验表明
的存在对反应的影响,小组同学将铁片酸洗(用稀硫酸浸泡后洗净)后再进行实验iii,发现铁片表面产生蓝色沉淀。此补充实验表明 的作用是
的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】电化学原理在防止金属腐蚀、能量转换等方面应用广泛。
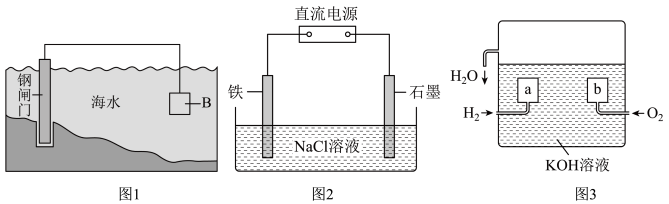
(1)①钢铁在海水中容易发生电化学腐蚀,负极反应式是____________ 。
②图1中,为减缓钢闸门的腐蚀,材料 可以选择
可以选择____________ (填“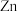 ”或“
”或“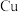 ”)。
”)。
(2)图2为钢铁防护模拟实验装置,则铁做_________ 极,检测钢铁保护效果的方法是:取少量铁电极附近的溶液于试管中,___________ ,则说明保护效果好。
(3)氢氧燃料电池是一种新型的化学电源,其构造如图3所示: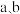 为多孔石墨电极,通入的气体由孔隙中逸出,并在电极表面放电。
为多孔石墨电极,通入的气体由孔隙中逸出,并在电极表面放电。
① 的电极反应式是
的电极反应式是__________________ ;
②若电池共产生 水,则电路中通过了
水,则电路中通过了___________ 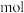 的电子。
的电子。

(1)①钢铁在海水中容易发生电化学腐蚀,负极反应式是
②图1中,为减缓钢闸门的腐蚀,材料
 可以选择
可以选择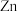 ”或“
”或“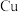 ”)。
”)。(2)图2为钢铁防护模拟实验装置,则铁做
(3)氢氧燃料电池是一种新型的化学电源,其构造如图3所示:
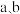 为多孔石墨电极,通入的气体由孔隙中逸出,并在电极表面放电。
为多孔石墨电极,通入的气体由孔隙中逸出,并在电极表面放电。①
 的电极反应式是
的电极反应式是②若电池共产生
 水,则电路中通过了
水,则电路中通过了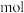 的电子。
的电子。
您最近一年使用:0次
【推荐1】化学实验有助于理解化学知识,提升科学素养。
I.某探究小组用以下右图装置做如下实验。
(1)实验1:同时加入试剂,反应开始阶段可观察到U形管中液面_____ (填编号,下同),反应结束静置一段时间,最终U形管中液面_______ 。
a.左高右低 b.左低右高 c.左右基本持平
(2)实验2:一段时间后观察到U形管中液面左低右高, b管溶液中出现红褐色浑浊物,请解释出现上述现象的原因:________________________________________________ 。
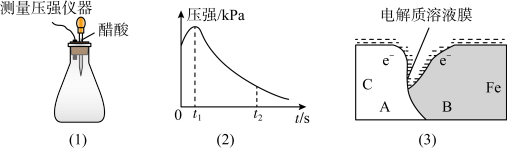
II.某研究小组为探究弱酸性条件下铁的电化学腐蚀类型,将混合均匀的新制铁粉和炭粉置于锥形瓶底部,塞上瓶塞(如图(1)所示)。从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。
(3)请填满表中空格,以完成实验设计:
(4)实验①测得容器中的压强随时间的变化如图(2)所示。该小组得出0~t1时压强增大的主要原因是:___________________________________ 。t2时,容器中压强明显变小的原因是______________ 。请在图(3)中用箭头标出发生该腐蚀时A和B之间的电子移动方向______________ 。
I.某探究小组用以下右图装置做如下实验。
| 实验编号 | a中试剂 | b中试剂 | 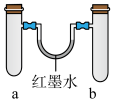 |
| 1 | 0.1克Na、3 mL水 | 0.1克Na、3 mL乙醇 | |
| 2 | 3 mL水 | 3 mL饱和FeSO4溶液 |
a.左高右低 b.左低右高 c.左右基本持平
(2)实验2:一段时间后观察到U形管中液面左低右高, b管溶液中出现红褐色浑浊物,请解释出现上述现象的原因:
II.某研究小组为探究弱酸性条件下铁的电化学腐蚀类型,将混合均匀的新制铁粉和炭粉置于锥形瓶底部,塞上瓶塞(如图(1)所示)。从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。
(3)请填满表中空格,以完成实验设计:
| 编号 | 实验目的 | 炭粉/g | 铁粉/g | 醋酸浓度/mol/L |
| ① | 作参照实验 | 0.5 | 2.0 | 1.0 |
| ② | 探究醋酸浓度对实验的影响 | 0.5 | 0.1 | |
| ③ | 0.2 | 2.0 | 1.0 |

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】研究金属腐蚀和防腐的原理很有现实意义。
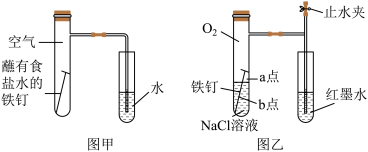
(1)甲图为人教版教材中探究钢铁的吸氧腐蚀的装置。某兴趣小组按该装置实验,导管中液柱的上升缓慢,下列措施可以更快更清晰观察到水柱上升现象的有_______(填序号)。
(2)该小组将甲图装置改进成乙图装置并进行实验,导管中红墨水液柱高度随时间的变化如下表,根据数据判断腐蚀的速率随时间逐渐____ (填“加快”、“不变”、“减慢”),你认为影响因素为____ 。
(3)为探究铁钉腐蚀实验a、b两点所发生的反应,进行以下实验,请完成表格空白:
根据以上实验探究,试判断_______ (填“a”或“b”)为负极,该点腐蚀更严重。
(4)金属阳极钝化是一种电化学防腐方法。将Fe作阳极置于H2SO4溶液中,一定条件下Fe钝化形成致密Fe3O4氧化膜,试写出该阳极电极反应式_______ 。

(1)甲图为人教版教材中探究钢铁的吸氧腐蚀的装置。某兴趣小组按该装置实验,导管中液柱的上升缓慢,下列措施可以更快更清晰观察到水柱上升现象的有_______(填序号)。
| A.用纯氧气代替试管内空气 | B.用酒精灯加热试管提高温度 |
| C.将铁钉换成铁粉和炭粉混合粉末 | D.换成更细的导管,水中滴加红墨水 |
| 时间/min | 1 | 3 | 5 | 7 | 9 |
| 液柱高度/cm | 0.8 | 2.1 | 3.0 | 3.7 | 4.2 |
(3)为探究铁钉腐蚀实验a、b两点所发生的反应,进行以下实验,请完成表格空白:
| 实验操作 | 实验现象 | 实验结论 |
| 向NaCl溶液中滴加2~3滴酚酞指示剂 | a点附近溶液出现红色 | a点电极反应为① |
| 然后再滴加2~3滴K3[Fe(CN)6]溶液 | b点周围出现蓝色沉淀 | b点电极反应为② |
根据以上实验探究,试判断
(4)金属阳极钝化是一种电化学防腐方法。将Fe作阳极置于H2SO4溶液中,一定条件下Fe钝化形成致密Fe3O4氧化膜,试写出该阳极电极反应式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞 (如图1)。
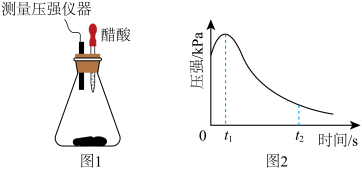
从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。实验测得容器中压强随时间变化如图2。t2时,容器中压强明显小于起始压强,其原因是铁发生了____________ 腐蚀,此时,碳粉表面发生的电极反应式是____________ 。
(2)氢氧燃料电池汽车作为上海世博园中的交通工具之一,下列有关说法不正确 的是______ 。
A.太阳光催化分解水制氢气比电解水制氢气更为科学
B.氢氧燃料电池作为汽车动力更能保护环境
C.以稀H2SO4、KOH溶液为介质的氢氧燃料电池的负极电极反应式相同
D.以稀H2SO4、KOH溶液为介质的氢氧燃料电池的总反应式相同
(3)电动车采用了一种高效耐用的新型可充电电池,该电池的总反应式为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。
①该电池放电时负极电极反应式为_________ ;
②充电时阳极电极反应式为_______ 。
(4)下列描述中,符合生产实际的是( )
A. 电解食盐水制得金属钠 B. 电解熔融氯化铝制取金属铝,用石墨作阳极
C. 一氧化碳高温还原铁矿石制得铁 D.电解熔融氧化镁制取金属镁,用铁作阳极
(5)金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+)( )
A.阴极发生还原反应,其电极反应式:Ni2++2e-=Ni
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D.电解后,电解槽底部的阳极泥中只有Cu和Pt

从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。实验测得容器中压强随时间变化如图2。t2时,容器中压强明显小于起始压强,其原因是铁发生了
(2)氢氧燃料电池汽车作为上海世博园中的交通工具之一,下列有关说法
A.太阳光催化分解水制氢气比电解水制氢气更为科学
B.氢氧燃料电池作为汽车动力更能保护环境
C.以稀H2SO4、KOH溶液为介质的氢氧燃料电池的负极电极反应式相同
D.以稀H2SO4、KOH溶液为介质的氢氧燃料电池的总反应式相同
(3)电动车采用了一种高效耐用的新型可充电电池,该电池的总反应式为:3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。①该电池放电时负极电极反应式为
②充电时阳极电极反应式为
(4)下列描述中,符合生产实际的是
A. 电解食盐水制得金属钠 B. 电解熔融氯化铝制取金属铝,用石墨作阳极
C. 一氧化碳高温还原铁矿石制得铁 D.电解熔融氧化镁制取金属镁,用铁作阳极
(5)金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+)
A.阴极发生还原反应,其电极反应式:Ni2++2e-=Ni
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D.电解后,电解槽底部的阳极泥中只有Cu和Pt
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】以NaCl为主要成分的融雪剂会腐蚀桥梁、铁轨等钢铁设备。某研究小组探究NaCl溶液对钢铁腐蚀的影响。
(1)将滤纸用35%的NaCl溶液润湿,涂上铁粉、碳粉的混合物,贴在表面皿上。在滤纸上加几滴检验试剂,再缓慢加入NaCl溶液至没过滤纸,操作如下所示:

①实验ⅰ的现象说明,得电子的物质是_______ 。
②为了说明NaCl的作用,需要补充的对照实验是_______ 。
(2)向如图所示装置的烧杯a、b中各加入30mL3.5%的NaCl溶液,闭合K,指针未发生偏转。加热烧杯a,指针向右偏转。

①各取a、b中溶液少量,滴加K3[Fe(CN)6]溶液,a中出现蓝色沉淀,b中无变化,b中铁片作_______ 极。
②加热后,指针发生偏转的原因可能是_______ 。
(3)用(2)中图示装置探究不同浓度NaCl溶液对钢铁腐蚀的影响,向烧杯a、b中各加入30mL不同质量分数的NaCl溶液,实验记录如下表所示。
①Ⅱ中,b中电极发生的电极反应是_______ 。
②Ⅲ中,铁在饱和NaCl溶液中不易被腐蚀,查阅资料可知:在饱和NaCl溶液中O2浓度较低,钢铁不易被腐蚀。设计实验证明:_______ 。
(1)将滤纸用35%的NaCl溶液润湿,涂上铁粉、碳粉的混合物,贴在表面皿上。在滤纸上加几滴检验试剂,再缓慢加入NaCl溶液至没过滤纸,操作如下所示:

①实验ⅰ的现象说明,得电子的物质是
②为了说明NaCl的作用,需要补充的对照实验是
(2)向如图所示装置的烧杯a、b中各加入30mL3.5%的NaCl溶液,闭合K,指针未发生偏转。加热烧杯a,指针向右偏转。

①各取a、b中溶液少量,滴加K3[Fe(CN)6]溶液,a中出现蓝色沉淀,b中无变化,b中铁片作
②加热后,指针发生偏转的原因可能是
(3)用(2)中图示装置探究不同浓度NaCl溶液对钢铁腐蚀的影响,向烧杯a、b中各加入30mL不同质量分数的NaCl溶液,实验记录如下表所示。
| 实验 | a | b | 指针偏转方向 |
| Ⅰ | 0.1% | 0.01% | 向右 |
| Ⅱ | 0.1% | 3.5% | 向左 |
| Ⅲ | 3.5% | 饱和溶液 | 向右 |
②Ⅲ中,铁在饱和NaCl溶液中不易被腐蚀,查阅资料可知:在饱和NaCl溶液中O2浓度较低,钢铁不易被腐蚀。设计实验证明:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】如图, 水槽中试管内有一枚铁钉,放置数天观察:

(1)若液面上升,则溶液呈______ 性,发生______ 腐蚀,电极反应式为:负极:______________ ,正极:___________________ 。
(2)若液面下降,则溶液呈________ 性,发生_________ 腐蚀,电极反应式为:负极:______________ ;正极:__________________ 。

(1)若液面上升,则溶液呈
(2)若液面下降,则溶液呈
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】电化学原理在防止金属腐蚀、能最转换、物质合成、环境治理等方面应用广泛。研究金属腐蚀和防腐的原理很有现实意义。
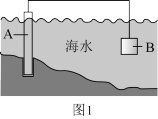
(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择________ (填标号)。
A.碳棒 B.锌板 C.铜板
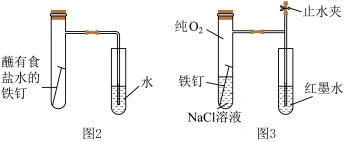
(2)某兴趣小组按图2装置实验,导管中液柱的上升缓慢,下列措施可以更快更清晰观察到水柱上升现象的有 (填序号)。
(3)该小组将图2装置改进成图3装置并进行实验,导管中红墨水液柱高度随时间的变化如下表,根据数据判断腐蚀的速率随时间逐渐________ (填“加快”“不变”或“减慢”),你认为影响因素为________ 。
(4)设计下面装置研究弱酸性环境中腐蚀的主要形式。测定锥形瓶内气压和空气中氧气的体积分数随时间变化见图,从图中可分析,t1~t2之间主要发生________ 腐蚀(填“吸氧”或“析氢”),原因________ 。
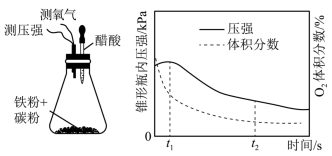
(5)金属阳极钝化是一种电化学防腐方法。将Fe作阳极置于H2SO4溶液中,一定条件下Fe钝化形成致密Fe3O4氧化膜,试写出该阳极电极反应式_____________ 。


(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择
A.碳棒 B.锌板 C.铜板
(2)某兴趣小组按图2装置实验,导管中液柱的上升缓慢,下列措施可以更快更清晰观察到水柱上升现象的有 (填序号)。
| A.用纯氧气代替试管内空气 | B.用酒精灯加热试管提高温度 |
| C.将铁钉换成铁粉和炭粉混合粉末 | D.换成更细的导管,水中滴加红墨水 |
| 时间/min | 1 | 3 | 5 | 7 | 9 |
| 液柱高度/cm | 0.8 | 2.1 | 3.0 | 3.7 | 4.2 |
(4)设计下面装置研究弱酸性环境中腐蚀的主要形式。测定锥形瓶内气压和空气中氧气的体积分数随时间变化见图,从图中可分析,t1~t2之间主要发生

(5)金属阳极钝化是一种电化学防腐方法。将Fe作阳极置于H2SO4溶液中,一定条件下Fe钝化形成致密Fe3O4氧化膜,试写出该阳极电极反应式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学实验小组为了探究氨气的还原性和氧化性设计了如下实验方案。
实验一:探究氨气的还原性
已知:Cu2O粉末呈红色,在酸性溶液中不稳定:Cu2O+H2SO4(稀)=Cu+CuSO4+H2O。
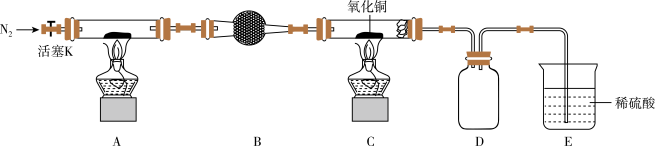
(1)装置A用于制备氨气,硬质玻璃管中所盛试剂通常为____________ ,装置B中所盛放的试剂是____________ 。实验开始前应先通一段时间的N2,其目的是___________________ 。
(2)反应结束后装置C中的氧化铜完全反应生成红色固体,为了探究红色固体的成分,进行了如下实验:取10.4 g红色固体于烧杯中,加入足量稀硫酸充分搅拌、静置、过滤、洗涤、干燥、称重,得固体6.4 g,则红色固体的成分及其物质的量为___________ 。
实验二:探究氨气的氧化性
已知:
①铝可以与氨气发生反应:2Al+2NH3 2AlN+3H2。
2AlN+3H2。
②AlN性质稳定,常温下基本不与水反应,加热时溶于浓碱溶液且可产生氨气。
按如图所示连接好装置,打开装置F中分液漏斗活塞,待装置中空气排尽后再点燃装置H处酒精灯。

(3)装置F中发生反应的化学方程式为_______________________ 。
(4)橡胶管a的作用是________________ ,装置I的作用是_____________ 。
(5)根据已知信息设计实验方案测定所得样品中AlN的纯度,简要写出实验过程:________ 。
实验一:探究氨气的还原性
已知:Cu2O粉末呈红色,在酸性溶液中不稳定:Cu2O+H2SO4(稀)=Cu+CuSO4+H2O。

(1)装置A用于制备氨气,硬质玻璃管中所盛试剂通常为
(2)反应结束后装置C中的氧化铜完全反应生成红色固体,为了探究红色固体的成分,进行了如下实验:取10.4 g红色固体于烧杯中,加入足量稀硫酸充分搅拌、静置、过滤、洗涤、干燥、称重,得固体6.4 g,则红色固体的成分及其物质的量为
实验二:探究氨气的氧化性
已知:
①铝可以与氨气发生反应:2Al+2NH3
 2AlN+3H2。
2AlN+3H2。②AlN性质稳定,常温下基本不与水反应,加热时溶于浓碱溶液且可产生氨气。
按如图所示连接好装置,打开装置F中分液漏斗活塞,待装置中空气排尽后再点燃装置H处酒精灯。

(3)装置F中发生反应的化学方程式为
(4)橡胶管a的作用是
(5)根据已知信息设计实验方案测定所得样品中AlN的纯度,简要写出实验过程:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某课外活动小组设计了下列装置,验证二氧化碳跟过氧化的反应时需要与水接触。
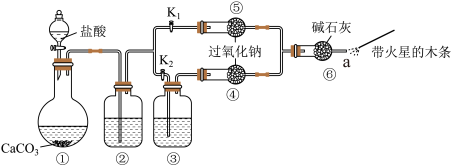
【装置分析】
(1)装置②中的试剂是___________ (填序号);装置③中的试剂是___________ (填序号)。
a.饱和NaHCO3溶液 b.饱和Na2CO3溶液 c.浓H2SO4
【进行实验】
步骤1:打开弹簧夹K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处;
步骤2:打开弹簧夹K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
(2)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是________ 、________ 。
(3)用双线桥表示过氧化钠与二氧化碳反应的电子转移情况___________ 。
【实验反思】
(4)有同学提出质疑:“上述实验不足以证明有水存在时过氧化钠与二氧化碳发生了化学反应。”其理由是___________ 。
(5)需要补充的实验操作是:取⑤中反应后的少量固体后,___________ 。
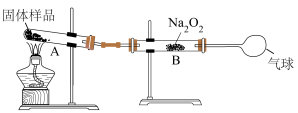
(6)侯氏制碱得到的碳酸钠产品中会含少量碳酸氢钠。某兴趣小组称量10.0g固体样品,利用下图装置测定产品纯度,装置A中生成的CO2和H2O被B中的Na2O2全部吸收后,测得Na2O2增重0.3g,该碳酸钠产品的纯度为___________ %。

【装置分析】
(1)装置②中的试剂是
a.饱和NaHCO3溶液 b.饱和Na2CO3溶液 c.浓H2SO4
【进行实验】
步骤1:打开弹簧夹K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处;
步骤2:打开弹簧夹K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
(2)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是
(3)用双线桥表示过氧化钠与二氧化碳反应的电子转移情况
【实验反思】
(4)有同学提出质疑:“上述实验不足以证明有水存在时过氧化钠与二氧化碳发生了化学反应。”其理由是
(5)需要补充的实验操作是:取⑤中反应后的少量固体后,
(6)侯氏制碱得到的碳酸钠产品中会含少量碳酸氢钠。某兴趣小组称量10.0g固体样品,利用下图装置测定产品纯度,装置A中生成的CO2和H2O被B中的Na2O2全部吸收后,测得Na2O2增重0.3g,该碳酸钠产品的纯度为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】为验证氧化性Cl2>Fe3+>SO2,某小组用下图所示装置进行实验(夹持仪器和A中加热装置已省略,气密性已检验)。

实验过程:
I. 打开弹簧夹K1~K4, 通入一段时间N2, 再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
II.打开活塞a,滴加一定量的浓盐酸,给A加热。
III.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
IV.打开活塞b,使约2 mL的溶液流入D试管中,检验其中的离子。
V.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
VI.更新试管D,重复过程IV,检验B溶液中的离子。
VII.实验结束后,打开弹簧夹K1~K4,再通入一段时间N2,然后拆卸,洗涤,整理仪器。
(1)过程I的目的是___________ 。
(2)棉花中浸润的溶液为___________ ,过程VII的目的是___________ 。
(3)C中发生反应的化学方程式为___________ 。
(4)用70%的硫酸制取SO2,反应速率比用98%的硫酸快,原因是___________ 。
(5)甲、乙、两三位同学分别完成了上述实验,结论如下表所示。他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是___________ (填“甲”、“乙”、“丙”)。
(6)进行实验过程V时,B中溶液颜色由黄色逐渐变为红棕色,停止通气,放置一段时间后溶液颜色变为浅绿色。
查阅资料:Fe2+(aq)+ (aq)
(aq) FeSO3(s)(墨绿色)
FeSO3(s)(墨绿色)
提出假设:FeCl3与SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3 (墨绿色)与FeCl3(黄色)的混合色。
某同学设计如下实验,证实该假设成立:

①溶液E和F分别为___________ 、___________ 。
②请用化学平衡原理解释步骤3中溶液由红棕色变为浅绿色的原因___________ 。

实验过程:
I. 打开弹簧夹K1~K4, 通入一段时间N2, 再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
II.打开活塞a,滴加一定量的浓盐酸,给A加热。
III.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
IV.打开活塞b,使约2 mL的溶液流入D试管中,检验其中的离子。
V.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
VI.更新试管D,重复过程IV,检验B溶液中的离子。
VII.实验结束后,打开弹簧夹K1~K4,再通入一段时间N2,然后拆卸,洗涤,整理仪器。
(1)过程I的目的是
(2)棉花中浸润的溶液为
(3)C中发生反应的化学方程式为
(4)用70%的硫酸制取SO2,反应速率比用98%的硫酸快,原因是
(5)甲、乙、两三位同学分别完成了上述实验,结论如下表所示。他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是
| 过程IV中B溶液中含有的离子 | 过程VI中B溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有 |
| 乙 | 既有Fe3+又有Fe2+ | 有 |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
查阅资料:Fe2+(aq)+
 (aq)
(aq) FeSO3(s)(墨绿色)
FeSO3(s)(墨绿色)提出假设:FeCl3与SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3 (墨绿色)与FeCl3(黄色)的混合色。
某同学设计如下实验,证实该假设成立:

①溶液E和F分别为
②请用化学平衡原理解释步骤3中溶液由红棕色变为浅绿色的原因
您最近一年使用:0次