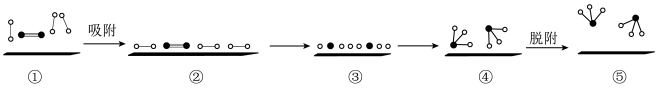
用石灰石硫化床法对燃料脱硫时的部分反应如下:
①CaCO3(s)=CaO(s)+CO2(g);ΔH1=a kJ/mol
②2CaO(s)+2SO2(g)+O2(g)=2CaSO4(s);ΔH2=b kJ/mol
③CaSO4(s)+4CO(g)=CaS(s)+4CO2(g);ΔH3=c kJ/mol
④CaO(s)+SO2(g)+3CO(g)=CaS(s)+3CO2(g);ΔH4=d kJ/mol
下列说法错误的是( )
①CaCO3(s)=CaO(s)+CO2(g);ΔH1=a kJ/mol
②2CaO(s)+2SO2(g)+O2(g)=2CaSO4(s);ΔH2=b kJ/mol
③CaSO4(s)+4CO(g)=CaS(s)+4CO2(g);ΔH3=c kJ/mol
④CaO(s)+SO2(g)+3CO(g)=CaS(s)+3CO2(g);ΔH4=d kJ/mol
下列说法错误的是( )
| A.反应①为放热反应 |
| B.反应②在常温下可自发进行,则该反应的ΔH<0,ΔS<0 |
| C.反应2CaCO3(s)+2SO2(g)+O2(g)= 2CaSO4(s)+2CO2(g)的ΔH=(a+b) kJ/mol |
| D.反应3CaSO4(s)+CaS(s)= 4CaO(s)+4SO2(g)的ΔH=(3c-4d) kJ/mol |
更新时间:2019-05-24 20:00:53
|
相似题推荐
多选题
|
适中
(0.65)
解题方法
【推荐1】CO、H2、C2H5OH三种物质燃烧的热化学方程式如下:
①CO(g)+1/2O2(g)=CO2(g) ΔH1=a kJ/mol
②H2(g)+1/2O2(g)=H2O(g) ΔH2=b kJ/mol
③C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ΔH3=c kJ/mol
下列说法不正确的是
①CO(g)+1/2O2(g)=CO2(g) ΔH1=a kJ/mol
②H2(g)+1/2O2(g)=H2O(g) ΔH2=b kJ/mol
③C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ΔH3=c kJ/mol
下列说法不正确的是
| A.ΔH1<0 |
| B.2CO(g)+4H2(g)=H2O(g)+C2H5OH(l) ΔH=(2a+4b-c) kJ/mol |
| C.CO2与H2合成C2H5OH反应的原子利用率为100% |
| D.2H2O(l)=2H2(g)+O2(g) ΔH=-2b kJ/mol |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】我国学者结合实验与计算机模拟结果,研究了均相NO-CO的反应历程,该反应经历了I、II、III三个过渡态。图中显示的是反应路径中每一阶段内各驻点的能量相对于此阶段内反应物能量的能量之差。下列说法正确的是
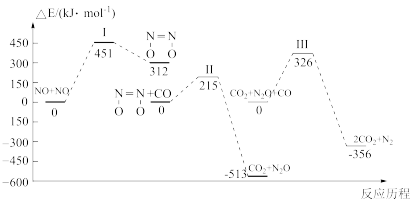

A.N2O比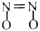 更不容易与CO发生反应 更不容易与CO发生反应 |
| B.整个反应分为三个基元反应阶段,其中第一个反应阶段活化能最大 |
C.2NO(g)+2CO(g) N2(g)+2CO2(g) ∆H>0 N2(g)+2CO2(g) ∆H>0 |
| D.其他条件不变,增大压强或使用催化剂均可以增大反应速率,提高反应物的转化率 |
您最近一年使用:0次
多选题
|
适中
(0.64)
名校
【推荐1】氯气、溴蒸气分别与氢气反应的热化学方程式如下:
H2(g)+Cl2(g)=2HCl(g),生成2 mol HCl放热Q1 kJ
H2(g)+Br2(g)=2HBr(g),生成2 mol HBr放热Q2 kJ
已知Q1>Q2>0。下列说法正确的是
H2(g)+Cl2(g)=2HCl(g),生成2 mol HCl放热Q1 kJ
H2(g)+Br2(g)=2HBr(g),生成2 mol HBr放热Q2 kJ
已知Q1>Q2>0。下列说法正确的是
| A.上述两个反应中反应物的总能量均大于生成物的总能量 |
| B.上述两个反应中反应物的总能量均小于生成物的总能量 |
| C.H2(g)和Cl2(g)反应生成1 mol HCl(g)时放出Q1kJ的热量 |
| D.1 mol HBr(g)具有的能量大于1mol HBr(l)具有的能量 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】废水对自然环境有严重的破坏作用,水污染治理刻不容缓,BMO(Bi2MoO6)是一种高效光催化剂,可用于光催化降解苯酚,原理如图所示。下列说法不正确的是( )
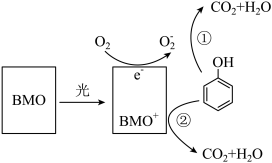

| A.该过程中O2-e-=O2- |
| B.①和②中BMO+和O-都表现较强氧化性 |
| C.催化剂BMO能降低反应的反应热和活化能 |
| D.该过程为放热反应 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】T℃时,在密闭容器甲、乙中分别充入1mol  和3mol
和3mol  ,它们分别在有水分子筛(只允许水分子透过)和无水分子筛条件下仅发生反应1,测得
,它们分别在有水分子筛(只允许水分子透过)和无水分子筛条件下仅发生反应1,测得 平衡转化率与压强关系如图所示。在催化剂A作用下,只发生反应3,该反应的速率方程式为
平衡转化率与压强关系如图所示。在催化剂A作用下,只发生反应3,该反应的速率方程式为 ,
,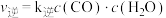 (k为速率常数,只与温度催化剂有关)
(k为速率常数,只与温度催化剂有关)
反应1: ;
;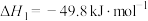
反应2: ;
;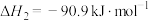
反应3: ;
;
 和3mol
和3mol  ,它们分别在有水分子筛(只允许水分子透过)和无水分子筛条件下仅发生反应1,测得
,它们分别在有水分子筛(只允许水分子透过)和无水分子筛条件下仅发生反应1,测得 平衡转化率与压强关系如图所示。在催化剂A作用下,只发生反应3,该反应的速率方程式为
平衡转化率与压强关系如图所示。在催化剂A作用下,只发生反应3,该反应的速率方程式为 ,
,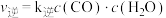 (k为速率常数,只与温度催化剂有关)
(k为速率常数,只与温度催化剂有关)反应1:
 ;
;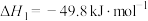
反应2:
 ;
;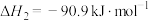
反应3:
 ;
;
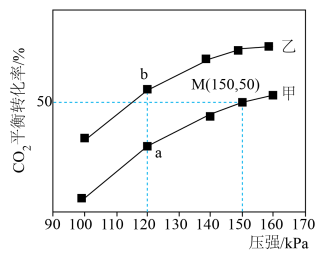
A.催化剂A作用下,830℃时该反应的平衡常数K=1,则900℃时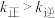 |
| B.使用了水分子筛的容器是甲 |
C.反应1的平衡常数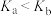 |
D.M点 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】如图是金属镁和卤素单质(X2)反应的能量变化示意图。下列说法正确的是

MgBr2(s)+Cl2(g)=MgCl2(s)+Br2(g),ΔH=-117kJ·mol-1

MgBr2(s)+Cl2(g)=MgCl2(s)+Br2(g),ΔH=-117kJ·mol-1
| A.由MgCl2制取Mg是放热过程 |
| B.热稳定性:MgI2<MgBr2<MgCl2<MgF2 |
| C.常温下氧化性:F2<Cl2<Br2<I2 |
| D.由图可知此温度下MgBr2(s)与Cl2(g)反应的热化学方程式为:MgBr2(s)+Cl2(g)=MgCl2(s)+Br2(g),ΔH=-117kJ·mol-1, |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】已知:CH3OH(g)+ O2(g)=CO2(g)+2H2O(g)△H=akJ·mol﹣1、CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=bkJ·mol﹣1,则下列叙述正确的是
O2(g)=CO2(g)+2H2O(g)△H=akJ·mol﹣1、CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=bkJ·mol﹣1,则下列叙述正确的是
 O2(g)=CO2(g)+2H2O(g)△H=akJ·mol﹣1、CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=bkJ·mol﹣1,则下列叙述正确的是
O2(g)=CO2(g)+2H2O(g)△H=akJ·mol﹣1、CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=bkJ·mol﹣1,则下列叙述正确的是| A.C﹣H键键长小于H﹣H键 |
| B.CH4(g)+2O2=CO2(g)+2H2O(g)△H=bkJ·mol﹣1表示甲烷燃烧热的热化学方程式 |
| C.2CH3OH(g)=2CH4(g)+O2(g)△H=2(a﹣b)kJ·mol﹣1 |
D.当CH3OH(g)和CH4(g)物质的量之比为1:2时,其完全燃烧生成CO2和H2O(g)时,放出的热量为ckJ,则该混合物中CH3OH(g)的物质的量为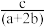 mol mol |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
A.某浓度的氨水加水稀释后 pH 变小,则其中的c(NH3·H2O)/c(NH )的值也减小 )的值也减小 |
| B.向 AgCl 悬浊液中加入少量 KI 溶液,沉淀转化为黄色,说明 Ksp(AgI)>Ksp(AgCl) |
| C.常温下,MgO(s)+C(s)=Mg(s)+CO(g)不能自发进行,则其△H>0 |
| D.室温下,pH=3 的 CH3COOH 溶液与pH=11 的 NaOH 溶液等体积混合,溶液 pH>7 |
您最近一年使用:0次
多选题
|
适中
(0.65)
真题
【推荐2】下列说法不正确的是
| A.铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
B.常温下,反应 不能自发进行,则该反应的 不能自发进行,则该反应的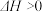 |
| C.一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 |
D.相同条件下,溶液中 、 、 、 、 的氧化性依次减弱 的氧化性依次减弱 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】下列说法正确的是
| A.反应TiO2(s) + 2Cl2(g)=TiCl4(g) + O2(g) ΔH>0能自发进行,其原因是ΔS>0 |
| B.室温下,pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合,溶液pH>7 |
C.CH3COOH溶液加水稀释后,溶液中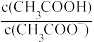 的值减小 的值减小 |
| D.对于乙酸与乙醇的酯化反应(ΔH<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大 |
您最近一年使用:0次

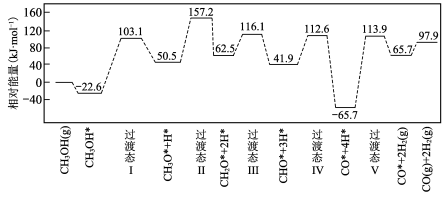
 CO(g)+2H2(g)的
CO(g)+2H2(g)的 分别表示
分别表示 、
、 、
、 及催化剂。
及催化剂。