下表是现行中学化学教科书中元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答问题:
(1)②表示的元素是______ (填元素符号)。
(2)①与⑤两种元素相比较,原子半径较大的是______ (填元素符号),其非金属性较强的是 ______ (填元素符号),其最高正价氧化物水化物酸性较强的酸是_______ (填分子式)。
(3)⑥元素的单质可以用来制取漂白粉,其有效成分是______ (填化学式)。③与⑥两种元素所形成化合物所含化学键是______ (填“共价键”或“离子键”)。
(4)写出元素③的最高价氧化物对应的水化物与元素④的最高价氧化物对应的水化物相互反应的化学方程式:____________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | H | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ① | ② | F | Ne | ||||
| 3 | ③ | Mg | ④ | Si | ⑤ | ⑥ |
(1)②表示的元素是
(2)①与⑤两种元素相比较,原子半径较大的是
(3)⑥元素的单质可以用来制取漂白粉,其有效成分是
(4)写出元素③的最高价氧化物对应的水化物与元素④的最高价氧化物对应的水化物相互反应的化学方程式:
更新时间:2019-06-06 11:33:33
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】A、B、C、D、E、F是六种短周期的主族元素,原子序数依次增大,A是IA族的非金属元素,B元素的最高价氧化物的水化物与其简单气态氢化物可反应生成盐,C是短周期中原子半径最大的元素,D元素原子L层电子数和M层电子数之差等于B元素最外层电子数,E元素最高正价和最低负价代数和等于4,据此回答下列问题:
(1)F元素在周期表中的位置__________ ,C原子结构示意图______________ 。
(2)A、B两元素可形成18电子的分子,该分子的电子式为_______________ 。
(3)A和氧元素形成的简单化合物,其熔沸点高于A和E形成的简单化合物,原因是____________ 。
(4)C、D、F可形成复杂化合物C[DF4],该化合物含有的化学键类型为________________ 。
(5)仅有上述元素形成的化合物或单质间的某些反应,可用以说明E和F两元素非金属性的强弱,写出其中一个离子反应方程式__________________________________ 。
(6)写出C、D两元素最高价氧化物的水化物反应的离子方程式____________________ 。
(1)F元素在周期表中的位置
(2)A、B两元素可形成18电子的分子,该分子的电子式为
(3)A和氧元素形成的简单化合物,其熔沸点高于A和E形成的简单化合物,原因是
(4)C、D、F可形成复杂化合物C[DF4],该化合物含有的化学键类型为
(5)仅有上述元素形成的化合物或单质间的某些反应,可用以说明E和F两元素非金属性的强弱,写出其中一个离子反应方程式
(6)写出C、D两元素最高价氧化物的水化物反应的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】在O、S、Se、Te四种元素中,单质氧化性最强的化学式是__ ,简单阴离子还原性最强的离子符号为___ 。硒元素最高价氧化物的水化物的化学式为__ ,它与足量的氢氧化钠溶液反应的化学方程式为___ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】下表是元素周期表的一部分,针对表中的①〜⑩元素,填写下列空白:
(1)表中所列元素中,属于短周期金属元素的为__________ (填元素符号),其原子半径由大到小的顺序为__________ (用元素符号表示)。
(2)表中不属于主族元素的是__________ (填元素符号),该元素在周期表中的位置是__________ 。
(3)1mol④的单质与足量②的氢化物完全反应产生的气体在标准状况下的体积为__________ 。
| 族 周期 | I A | II A | … | III A | IV A | V A | VI A | VII A | 0 |
| 2 | ① | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑩ | |||
| 4 | ⑨ |
(1)表中所列元素中,属于短周期金属元素的为
(2)表中不属于主族元素的是
(3)1mol④的单质与足量②的氢化物完全反应产生的气体在标准状况下的体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】氧、硫、硒(Se)、碲(Te)、钋(Po)是元素周期表中原子序数依次增大的同主族元素。回答下列问题:
(1)硒在元素周期表中的位置________ 。
(2) Po的中子数为
Po的中子数为________ 。
(3)某温度时,该族单质与H2反应生成气态H2X的热化学方程式如下:
O2(g)+2H2(g)=2H2O(g) △H1=-484 kJ/mol
S(g)+H2(g) H2S(g) △H2=-20 kJ/mol
H2S(g) △H2=-20 kJ/mol
Se(g)+H2(g) H2Se(g) △H3=+81kJ/mol
H2Se(g) △H3=+81kJ/mol
①硫和硒氢化物的热稳定性:H2S________ H2Se(填“>”、“=”或“<”);判断依据是________ 。
②写出O2(g)与H2S(g)反应生成H2O(g)和S(g)的热化学方程式________ 。
(1)硒在元素周期表中的位置
(2)
 Po的中子数为
Po的中子数为(3)某温度时,该族单质与H2反应生成气态H2X的热化学方程式如下:
O2(g)+2H2(g)=2H2O(g) △H1=-484 kJ/mol
S(g)+H2(g)
 H2S(g) △H2=-20 kJ/mol
H2S(g) △H2=-20 kJ/molSe(g)+H2(g)
 H2Se(g) △H3=+81kJ/mol
H2Se(g) △H3=+81kJ/mol①硫和硒氢化物的热稳定性:H2S
②写出O2(g)与H2S(g)反应生成H2O(g)和S(g)的热化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】某小组在研究前18号元素时发现:依据不同的标准和规律,元素周期表有不同的排列形式。如果将它们按原子序数递增的顺序排列,可形成如图所示的“蜗牛”形状,图中每个“●”代表一种元素,其中A代表氢元素。
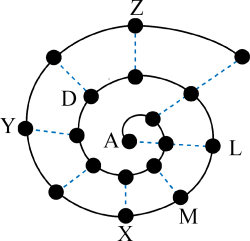
(1)X的元素符号为______ ,I元素在周期表中的位置为______ 。
(2)M与Z两种元素形成的化合物的化学式为______ 。
(3)下列说法正确的是______ (填序号)。
a.I元素形成的单质通入LZ的溶液中可得Z元素形成的单质
b.虚线相连的元素处于同一主族
c.L元素形成的单质在D元素形成的单质中燃烧生成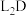
d.X、Y、M元素为同周期元素

(1)X的元素符号为
(2)M与Z两种元素形成的化合物的化学式为
(3)下列说法正确的是
a.I元素形成的单质通入LZ的溶液中可得Z元素形成的单质
b.虚线相连的元素处于同一主族
c.L元素形成的单质在D元素形成的单质中燃烧生成
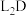
d.X、Y、M元素为同周期元素
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】如表是元素周期表的一部分,根据表中给出的10种元素,按要求使用化学用语填空作答:
(1)地壳中含量最高的元素是___ (填元素符号);金属性最强的元素是___ (填元素符号);单质的化学性质最不活泼的元素是___ (填元素符号)。
(2)最高价氧化物对应水化物酸性最强的是___ (填化合物化学式);最高价氧化物不溶于水,但既溶于稀硫酸又溶于氢氧化钠溶液的是___ (填化合物化学式)。
(3)烧焦羽毛味气体A和臭鸡蛋味气体B相遇可发生反应生成一种单质和水,该反应化学方程式为____ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | H | |||||||
| 2 | C | N | O | Ne | ||||
| 3 | Na | Al | P | S | Cl |
(2)最高价氧化物对应水化物酸性最强的是
(3)烧焦羽毛味气体A和臭鸡蛋味气体B相遇可发生反应生成一种单质和水,该反应化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】2019年是化学元素周期表问世150周年,联合国宣布此年为“国际化学元素周期表年”。元素周期表在学习、研究中有很重要的作用,下表是元素周期表的一部分。
(1)e的元素符号是___ 。
(2)f、g的最高价氧化物对应的水化物中,酸性较强的物质的化学式是___ 。
(3)c的金属性强于d的金属性,用原子结构解释原因:___ ,失电子能力c大于d。
(4)下列对于a及其化合物的推断中,正确的是___ (填序号)。
①a的最高正价和最低负价绝对值相等
②a的氢化物的稳定性强于f的氢化物的稳定性
③单质a比单质b难与氢气反应
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | a | b | ||||||
| 3 | c | d | e | f | g |
(1)e的元素符号是
(2)f、g的最高价氧化物对应的水化物中,酸性较强的物质的化学式是
(3)c的金属性强于d的金属性,用原子结构解释原因:
(4)下列对于a及其化合物的推断中,正确的是
①a的最高正价和最低负价绝对值相等
②a的氢化物的稳定性强于f的氢化物的稳定性
③单质a比单质b难与氢气反应
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:
①元素周期表中,Z与Y相邻,Z与W也相邻;
②Y、Z和W三种元素的原子最外层电子数之和为17。
请填空:
(1)Y、Z和W三种元素是否位于同一周期?(填“是”或“否”)_______ ,理由是_______ ;
(2)Y是_______ ,Z是_______ ,W是_______ 。(填元素符号)
(3)X、Y、Z和W可组成一化合物,其原子个数之比为8∶2∶4∶1.写出该化合物的名称及化学式_______ 。
①元素周期表中,Z与Y相邻,Z与W也相邻;
②Y、Z和W三种元素的原子最外层电子数之和为17。
请填空:
(1)Y、Z和W三种元素是否位于同一周期?(填“是”或“否”)
(2)Y是
(3)X、Y、Z和W可组成一化合物,其原子个数之比为8∶2∶4∶1.写出该化合物的名称及化学式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题:
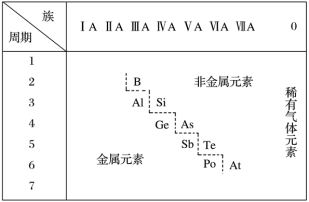
图中从第IIIA族的硼到第VIIA的砹连成一条斜线,即为金属元素和非金属元素的分界线。
问题:分界线附近元素的性质有什么特点____ ?金属性、非金属性最强的元素分别处于元素周期表的什么位置?_____

图中从第IIIA族的硼到第VIIA的砹连成一条斜线,即为金属元素和非金属元素的分界线。
问题:分界线附近元素的性质有什么特点
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】前20号部分元素在周期表中的位置如下表:
回答问题:(均用元素符号表示)
(1)除(1)以外,原子半径最小的是_____ ,(4)(5)(6)(7)元素的简单离子中半径最大的离子是_____ 。
(2)相同物质的量的(4)和(10)的单质分别和(1)的单质化合时放出的热量最多的是_____  。
。
(3)写出(11)离子的结构示意图________ 。
(4)从原子结构角度解释(12)比(13)金属性强的原因:_____________ 。
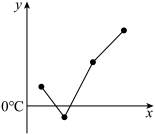
(5)单质沸点可能符合右图(x是原子序数,y是单质沸点)的四个元素是_______ 。
A. (2)(3)(4)(5) B. (8)(9)(10)(11) C. (5)(6)(7)(8) D. (10)(11)(12)(13)
| (1) | ||||||
| (2) | (3) | (4) | (5) | |||
| (6) | (7) | (8) | (9) | (10) | (11) | |
| (12) | (13) | |||||
回答问题:(均用元素符号表示)
(1)除(1)以外,原子半径最小的是
(2)相同物质的量的(4)和(10)的单质分别和(1)的单质化合时放出的热量最多的是
 。
。
(3)写出(11)离子的结构示意图
(4)从原子结构角度解释(12)比(13)金属性强的原因:
(5)单质沸点可能符合右图(x是原子序数,y是单质沸点)的四个元素是
A. (2)(3)(4)(5) B. (8)(9)(10)(11) C. (5)(6)(7)(8) D. (10)(11)(12)(13)
您最近一年使用:0次



