如表是元素周期表的一部分,根据表中给出的10种元素,按要求使用化学用语填空作答:
(1)地壳中含量最高的元素是___ (填元素符号);金属性最强的元素是___ (填元素符号);单质的化学性质最不活泼的元素是___ (填元素符号)。
(2)最高价氧化物对应水化物酸性最强的是___ (填化合物化学式);最高价氧化物不溶于水,但既溶于稀硫酸又溶于氢氧化钠溶液的是___ (填化合物化学式)。
(3)烧焦羽毛味气体A和臭鸡蛋味气体B相遇可发生反应生成一种单质和水,该反应化学方程式为____ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | H | |||||||
| 2 | C | N | O | Ne | ||||
| 3 | Na | Al | P | S | Cl |
(2)最高价氧化物对应水化物酸性最强的是
(3)烧焦羽毛味气体A和臭鸡蛋味气体B相遇可发生反应生成一种单质和水,该反应化学方程式为
更新时间:2021-01-31 13:53:14
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】氧、硫、硒(Se)、碲(Te)、钋(Po)是元素周期表中原子序数依次增大的同主族元素。回答下列问题:
(1)硒在元素周期表中的位置________ 。
(2) Po的中子数为
Po的中子数为________ 。
(3)某温度时,该族单质与H2反应生成气态H2X的热化学方程式如下:
O2(g)+2H2(g)=2H2O(g) △H1=-484 kJ/mol
S(g)+H2(g) H2S(g) △H2=-20 kJ/mol
H2S(g) △H2=-20 kJ/mol
Se(g)+H2(g) H2Se(g) △H3=+81kJ/mol
H2Se(g) △H3=+81kJ/mol
①硫和硒氢化物的热稳定性:H2S________ H2Se(填“>”、“=”或“<”);判断依据是________ 。
②写出O2(g)与H2S(g)反应生成H2O(g)和S(g)的热化学方程式________ 。
(1)硒在元素周期表中的位置
(2)
 Po的中子数为
Po的中子数为(3)某温度时,该族单质与H2反应生成气态H2X的热化学方程式如下:
O2(g)+2H2(g)=2H2O(g) △H1=-484 kJ/mol
S(g)+H2(g)
 H2S(g) △H2=-20 kJ/mol
H2S(g) △H2=-20 kJ/molSe(g)+H2(g)
 H2Se(g) △H3=+81kJ/mol
H2Se(g) △H3=+81kJ/mol①硫和硒氢化物的热稳定性:H2S
②写出O2(g)与H2S(g)反应生成H2O(g)和S(g)的热化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
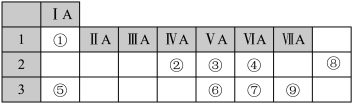
【推荐2】如表是元素周期表的一部分,其中每个数字序号代表一种短周期元素.

请按要求回答下列问题:
(1)元素③的最高价氧化物对应的水化物的化学式为_______________ ;
(2)②、③两元素的原子半径较大的是___________ (填元素符号);
(3)④和⑤两种元素的金属性较强的是____________ (填元素符号);
(4)元素③和元素⑥的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式___________________ .

请按要求回答下列问题:
(1)元素③的最高价氧化物对应的水化物的化学式为
(2)②、③两元素的原子半径较大的是
(3)④和⑤两种元素的金属性较强的是
(4)元素③和元素⑥的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】下表是元素周期表的一部分,回答下列有关问题:
(1)写出①原子结构示意图_______________
(2)在这些元素中,金属性最强的元素是_______ ,(填元素符号)元素⑦与元素⑧相比,非金属性较强的是 _____________ (填元素符号)
(3)⑤的最高价氧化物对应水化物与⑧的最高价氧化物对应水化物反应的离子方程式为:________________
(4)⑤的单质与③的最高价氧化物对应水化物反应的离子方程式为___________________________
(5)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑦形成一种AB2型的化合物,请用电子式表示其形成过程:_____________________________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
4 | ⑩ | ⑪ | ⑫ |
(1)写出①原子结构示意图
(2)在这些元素中,金属性最强的元素是
(3)⑤的最高价氧化物对应水化物与⑧的最高价氧化物对应水化物反应的离子方程式为:
(4)⑤的单质与③的最高价氧化物对应水化物反应的离子方程式为
(5)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑦形成一种AB2型的化合物,请用电子式表示其形成过程:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】在第三周期元素中,除稀有气体元素外:
(1)原子半径最小的元素是________ (填元素符号);
(2)金属性最强的元素是________ (填元素符号);
(3)最高价氧化物对应水化物酸性最强的是________ (用化学式回答,下同);
(4)最不稳定的气态氢化物是________ ;
(5)最高价氧化物对应水化物碱性最强的是________ ;
(6)氧化物中具有两性的是________________ 。
(1)原子半径最小的元素是
(2)金属性最强的元素是
(3)最高价氧化物对应水化物酸性最强的是
(4)最不稳定的气态氢化物是
(5)最高价氧化物对应水化物碱性最强的是
(6)氧化物中具有两性的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】下表为元素周期表的一部分:
回答下列有关问题:
(1)上表中原子半径最小的元素是_______ (填元素符号)。
(2)表中所列元素中,最活泼的金属元素是_______ (填元素符号,下同),最活泼的非金属元素是_______ ,最不活泼的元素是_______ 。
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式,下同),碱性最强的是_______ ,呈两性的是_______ ,最不稳定的气态氢化物是_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
回答下列有关问题:
(1)上表中原子半径最小的元素是
(2)表中所列元素中,最活泼的金属元素是
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】下表是现行中学化学教科书中元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答问题。
(1)②表示的元素是___________ (填元素符号);
(2)①②⑤三种元素的原子半径从大到小排列为:___________ (填元素符号);
(3)③④两种元素的金属性强弱顺序为:③___________ ④(填“<”或“>”);
(4)③与②两种元素所形成化合物的阴阳离子个数比为___________ ;
(5)④和⑥两种元素组成的化合物中含有的化学键为___________ (填“离子键”或“共价键”)。
族 周期 | ⅠA | 0 | |||||||
| 1 | H | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ① | ② | F | Ne | |||||
| 3 | ③ | Mg | ④ | Si | ⑤ | ⑥ | |||
(1)②表示的元素是
(2)①②⑤三种元素的原子半径从大到小排列为:
(3)③④两种元素的金属性强弱顺序为:③
(4)③与②两种元素所形成化合物的阴阳离子个数比为
(5)④和⑥两种元素组成的化合物中含有的化学键为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】用“ > ”或“<”填空:
(1)酸性:H2CO3__________ H2SiO3, H2SiO3__________ H3PO4
(2)碱性:Ca(OH)2__________ Mg(OH)2
(3)气态氢化物稳定性:H2O__________ H2S,
(1)酸性:H2CO3
(2)碱性:Ca(OH)2
(3)气态氢化物稳定性:H2O
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】NaOH被大量用于制皂、造纸和纺织品生产。回答下列问题。
(1)H元素位于元素周期表的第_______ 周期第IA族。
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的_______ (填“大”或“小”)。
(3)NaOH所含的两种非金属元素中,非金属性较强的是_______ (填“H”或“O”)。
(4)Na的最高价氧化物对应的水化物的化学式为_______ 。
(1)H元素位于元素周期表的第
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的
(3)NaOH所含的两种非金属元素中,非金属性较强的是
(4)Na的最高价氧化物对应的水化物的化学式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】完成下列问题。
(1)在元素周期表中位于对角线的元素性质有相似性,如锂和镁。下列关于金属锂的说法不正确的是____ 。
A.金属锂是最轻的金属 B.锂可以和冷水反应放出氢气
C.碳酸锂易溶于水 D.氢氧化钠碱性强于氢氧化锂
(2)下列有关碱金属的说法中,正确的是_______ 。
A.金属锂应保存在煤油中
B.随着核电荷数增加,阳离子的氧化性逐渐减弱
C.它们都能在空气里燃烧生成M2O(M表示碱金属)
D.碱金属单质熔沸点随核电荷数的增大而升高
(3)金属锂是一种重要的储氢材料,吸氢和放氢反应原理如下:
吸氢反应:2Li+H2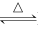 2LiH 放氢反应:LiH+H2O=LiOH+H2↑
2LiH 放氢反应:LiH+H2O=LiOH+H2↑
①放氢反应中的氧化剂是__________ 。
②已知LiH固体密度为0.8g/cm3。用锂吸收112L (标准状况)H2,生成的LiH体积与被吸收的H2体积比为_____ 。由②生成的LiH与H2O作用放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为______ mol。
(1)在元素周期表中位于对角线的元素性质有相似性,如锂和镁。下列关于金属锂的说法不正确的是
A.金属锂是最轻的金属 B.锂可以和冷水反应放出氢气
C.碳酸锂易溶于水 D.氢氧化钠碱性强于氢氧化锂
(2)下列有关碱金属的说法中,正确的是
A.金属锂应保存在煤油中
B.随着核电荷数增加,阳离子的氧化性逐渐减弱
C.它们都能在空气里燃烧生成M2O(M表示碱金属)
D.碱金属单质熔沸点随核电荷数的增大而升高
(3)金属锂是一种重要的储氢材料,吸氢和放氢反应原理如下:
吸氢反应:2Li+H2
 2LiH 放氢反应:LiH+H2O=LiOH+H2↑
2LiH 放氢反应:LiH+H2O=LiOH+H2↑①放氢反应中的氧化剂是
②已知LiH固体密度为0.8g/cm3。用锂吸收112L (标准状况)H2,生成的LiH体积与被吸收的H2体积比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】2019年是化学元素周期表问世150周年,联合国宣布此年为“国际化学元素周期表年”。元素周期表在学习、研究中有很重要的作用,下表是元素周期表的一部分。
(1)e的元素符号是___ 。
(2)f、g的最高价氧化物对应的水化物中,酸性较强的物质的化学式是___ 。
(3)c的金属性强于d的金属性,用原子结构解释原因:___ ,失电子能力c大于d。
(4)下列对于a及其化合物的推断中,正确的是___ (填序号)。
①a的最高正价和最低负价绝对值相等
②a的氢化物的稳定性强于f的氢化物的稳定性
③单质a比单质b难与氢气反应
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | a | b | ||||||
| 3 | c | d | e | f | g |
(1)e的元素符号是
(2)f、g的最高价氧化物对应的水化物中,酸性较强的物质的化学式是
(3)c的金属性强于d的金属性,用原子结构解释原因:
(4)下列对于a及其化合物的推断中,正确的是
①a的最高正价和最低负价绝对值相等
②a的氢化物的稳定性强于f的氢化物的稳定性
③单质a比单质b难与氢气反应
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】下列是部分短周期中第二、第三周期元素的原子半径及主要化合价。
回答下列问题:
(1)⑧在元素周期表中的位置是(周期、族)____________________ 。
(2)8个元素的最高价氧化物的水化物中,酸性最强的是___________________ (填化学式)。
(3)①元素和⑥元素形成化合物的电子式 是 ___________________________ 。
(4)写出④最高价氧化物对应水化物与⑥的氢化物水溶液反应的离子方程式:_______________________________________________ 。
(5)下列叙述正确的是______________ (填字母)。
A.③、④处于不同周期
B.②的阳离子与⑧的阴离子的核外电子数相等
C.⑥在同主族元素中非金属性最强
D.⑤元素与⑦元素两者核电荷数之差是8
E.①与⑧形成的化合物具有两性
| 元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(nm) | 0.186 | 0.160 | 0.152 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
| 主要化合价 | +1 | +2 | +1 | +3 | +5、-3 | +7、-1 | +5、-3 | -2 |
回答下列问题:
(1)⑧在元素周期表中的位置是(周期、族)
(2)8个元素的最高价氧化物的水化物中,酸性最强的是
(3)①元素和⑥元素形成化合物的
(4)写出④最高价氧化物对应水化物与⑥的氢化物水溶液反应的离子方程式:
(5)下列叙述正确的是
A.③、④处于不同周期
B.②的阳离子与⑧的阴离子的核外电子数相等
C.⑥在同主族元素中非金属性最强
D.⑤元素与⑦元素两者核电荷数之差是8
E.①与⑧形成的化合物具有两性
您最近一年使用:0次