71gNa2SO4 含有SO42-________ mol,含有O原子___________ 个,含有S原子______ g;完全溶于水,配成2 L溶液,则所得溶液中Na+的物质的量浓度为___________ 。
11-12高一上·广东深圳·期中 查看更多[1]
(已下线)2011-2012学年广东省深圳市第三高级中学高一上学期期中联考化学试卷
更新时间:2011-11-28 19:41:11
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】完成下列表格
| 物质 | H2 | O2 | NH3 | CO2 |
| 物质的量 | 2mol | 0.5mol | (3) | (6) |
| 体积(标况下) | 44.8L | (1) | (4) | 4.48L |
| 物质的质量 | 4g | 16g | (5) | (7) |
| 原子数 | 2.408x1024 | (2) | 2.408x1024 | (8) |
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】根据物质的量等相关物理量回答下列问题:
(1)_______ mol 所含氢原子数与
所含氢原子数与 所含氢原子数相等。
所含氢原子数相等。
(2)40.5g某金属氯化物 ,含有0.6mol氯离子,则金属R的相对原子质量为
,含有0.6mol氯离子,则金属R的相对原子质量为_______ 。
(3)20gA物质和14gB物质恰好完全反应,生成8.8gC物质、3.6gD物质和0.2molE物质,则E物质的摩尔质量为_______ 。
(4)NO和 可以发生反应
可以发生反应 ,若反应生成
,若反应生成 ,则参加反应的
,则参加反应的 的物质的量为
的物质的量为_______ mol。若有a molNO与b mol 充分反应,则反应后氮原子与氧原子的个数比为
充分反应,则反应后氮原子与氧原子的个数比为_______ (用含a、b的代数式表示)。
(5)36gCO与 的混合气体与足量
的混合气体与足量 充分反应后,将所得气体通入过量的澄清石灰水中,生成白色沉淀的质量为100g,则36gCO与
充分反应后,将所得气体通入过量的澄清石灰水中,生成白色沉淀的质量为100g,则36gCO与 的混合气体的总物质的量为
的混合气体的总物质的量为_______ mol,其中的CO在标准状况下的体积为_______ L。
(1)
 所含氢原子数与
所含氢原子数与 所含氢原子数相等。
所含氢原子数相等。(2)40.5g某金属氯化物
 ,含有0.6mol氯离子,则金属R的相对原子质量为
,含有0.6mol氯离子,则金属R的相对原子质量为(3)20gA物质和14gB物质恰好完全反应,生成8.8gC物质、3.6gD物质和0.2molE物质,则E物质的摩尔质量为
(4)NO和
 可以发生反应
可以发生反应 ,若反应生成
,若反应生成 ,则参加反应的
,则参加反应的 的物质的量为
的物质的量为 充分反应,则反应后氮原子与氧原子的个数比为
充分反应,则反应后氮原子与氧原子的个数比为(5)36gCO与
 的混合气体与足量
的混合气体与足量 充分反应后,将所得气体通入过量的澄清石灰水中,生成白色沉淀的质量为100g,则36gCO与
充分反应后,将所得气体通入过量的澄清石灰水中,生成白色沉淀的质量为100g,则36gCO与 的混合气体的总物质的量为
的混合气体的总物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)3.01×1023个NH4+含有质子的物质的量是______ mol,含有电子的物质的量是______ mol。
(2)200mL 2mol/L的Al2(SO4)3 溶液中SO42-的物质的量浓度为_________ 。
(3)标准状况下36g H2和O2组成的混合气体的体积是67.2L 。求这种混合气体中H2和O2的体积比为____________ 。
(4)同温同压下,质量比为17:48的NH3和CH4两种气体,密度之比为_________ 。
(5)已知1.505×1023个A气体分子质量为31g ,则A气体的摩尔质量是_________ 。
(2)200mL 2mol/L的Al2(SO4)3 溶液中SO42-的物质的量浓度为
(3)标准状况下36g H2和O2组成的混合气体的体积是67.2L 。求这种混合气体中H2和O2的体积比为
(4)同温同压下,质量比为17:48的NH3和CH4两种气体,密度之比为
(5)已知1.505×1023个A气体分子质量为31g ,则A气体的摩尔质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】在20℃时,将5.05 g KNO3溶于10.0g水中,恰好配成密度为1.15g/cm3的饱和溶液,计算:
(1)此饱和溶液中KNO3的物质的量。
(2)此饱和溶液中KNO3的物质的量浓度。
(1)此饱和溶液中KNO3的物质的量。
(2)此饱和溶液中KNO3的物质的量浓度。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】标准状况下,5L乙烯和乙炔的混合气体能与50g溴完全反应,求混合气体中乙烯和乙炔的体积分数_________ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)0.1molAl2(SO4)3中含Al3+_________ 个。
(2)同温同压下,等体积的CO和CO2所含分子个数之比为_________ ,所含氧原子个数之比为______ ,所含原子总数之比为___________ ,所含电子数目之比为___________ ;等质量的CO和CO2所含分子个数之比为____________ ,原子个数之比为____________ ,物质的量之比为____________ 。
(3)34g NH3共有_________ mol原子,0.1molH2S共有_________ 个氢原子;同温同压下,等体积的NH3和H2S气体的质量比为___________ ;等质量的NH3和H2S中分子个数比为_________ ;
(4)在标准状况下,35.5g氯气的体积是_________ L,将其与氢气完全化合需氢气的物质的量是_________ mol,将生成的气体制成1L溶液,溶质的物质的量浓度是_________ mol·L-1,
(2)同温同压下,等体积的CO和CO2所含分子个数之比为
(3)34g NH3共有
(4)在标准状况下,35.5g氯气的体积是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】根据所学知识,回答下列问题:
(1)标准状况下,1.7 g NH3的体积为___ L;它与标准状况下____ L CH4含有的氢原子数目相同。
(2)等质量的CO和N2所含分子数之比为____ 。
(3)将11.7 g NaCl固体配成10 L溶液,从中取出50 mL,这50 mL溶液中NaCl的物质的量浓度为____ mol·L-1
(4)34 g某二价金属的氯化物中含有0.5 mol Cl-,则该金属氯化物的摩尔质量为_____ g·mol-1,该金属的相对原子质量为_____ 。
(5)已知SO2、O2混合气体的质量共11.2 g,在标准状况下的体积为4.48 L,则混合气体中SO2的物质的量为_____ 。
(1)标准状况下,1.7 g NH3的体积为
(2)等质量的CO和N2所含分子数之比为
(3)将11.7 g NaCl固体配成10 L溶液,从中取出50 mL,这50 mL溶液中NaCl的物质的量浓度为
(4)34 g某二价金属的氯化物中含有0.5 mol Cl-,则该金属氯化物的摩尔质量为
(5)已知SO2、O2混合气体的质量共11.2 g,在标准状况下的体积为4.48 L,则混合气体中SO2的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】甲烷 是一种无色无味的气体,是天然气的主要成分。
是一种无色无味的气体,是天然气的主要成分。
(1)现有 ,它的摩尔质量是
,它的摩尔质量是_______ ,要把 完全燃烧,消耗氧气
完全燃烧,消耗氧气_______ g。
(2)标准状况下, 的密度为
的密度为_______ (保留3位有效数字)。如果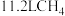 中含有x个氢原子,则阿伏加德罗常数的值为
中含有x个氢原子,则阿伏加德罗常数的值为_______ 。
(3)相同温度和压强下,质量相等的氢气和甲烷,它们的体积之比为_______ ,密度之比为_______ 。若把质量相等的这两种气体混合,则混合气体的平均相对分子质量为_______ (保留2位有效数字)。
(4)某沼气成分是 和
和 。取2L该沼气与
。取2L该沼气与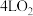 点燃充分反应后,除去水分,剩余气体的体积为3L。该沼气中
点燃充分反应后,除去水分,剩余气体的体积为3L。该沼气中 和
和 的物质的量之比为(气体体积均在同温同压下测定)
的物质的量之比为(气体体积均在同温同压下测定)_______ 。
 是一种无色无味的气体,是天然气的主要成分。
是一种无色无味的气体,是天然气的主要成分。(1)现有
 ,它的摩尔质量是
,它的摩尔质量是 完全燃烧,消耗氧气
完全燃烧,消耗氧气(2)标准状况下,
 的密度为
的密度为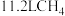 中含有x个氢原子,则阿伏加德罗常数的值为
中含有x个氢原子,则阿伏加德罗常数的值为(3)相同温度和压强下,质量相等的氢气和甲烷,它们的体积之比为
(4)某沼气成分是
 和
和 。取2L该沼气与
。取2L该沼气与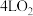 点燃充分反应后,除去水分,剩余气体的体积为3L。该沼气中
点燃充分反应后,除去水分,剩余气体的体积为3L。该沼气中 和
和 的物质的量之比为(气体体积均在同温同压下测定)
的物质的量之比为(气体体积均在同温同压下测定)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】现有m g某X2气体,X2摩尔质量为M g·mol-1,阿伏加德罗常数的值用NA表示,完成下列小题。
(1)该气体的物质的量为_______ mol。
(2)一个X原子的质量为_______ g。
(3)该气体在标准状况下的体积为_______ L。
(4)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为_______ mol·L-1。
(1)该气体的物质的量为
(2)一个X原子的质量为
(3)该气体在标准状况下的体积为
(4)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】现从固体KOH出发配制0.1mol/L 的KOH溶液 500mL,回答下列问题:
(1)配制过程中需要用到的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、___________
(2)如果在定容时仰视操作,则所配得溶液的浓度_______ 0.1mol/L(填> , =" ," <)
(3)若所用的固体KOH中混有NaOH,则所配得溶液的OH-浓度___ 0.1mol/L(填> , =" ," <)
(4)若用250mL的H2SO4溶液恰好能将此500mL 0.1mol/L 的KOH溶液中和,则该硫酸的物质的量浓度为________ mol/L
(1)配制过程中需要用到的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、
(2)如果在定容时仰视操作,则所配得溶液的浓度
(3)若所用的固体KOH中混有NaOH,则所配得溶液的OH-浓度
(4)若用250mL的H2SO4溶液恰好能将此500mL 0.1mol/L 的KOH溶液中和,则该硫酸的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】把2.3 g钠投入足量水中,充分反应后所得溶液用水稀释至100 mL。求:
(1)生成标准状况下的氢气多少升_______ ;
(2)所得的溶液物质的量浓度_______ ?
(1)生成标准状况下的氢气多少升
(2)所得的溶液物质的量浓度
您最近一年使用:0次



