I.有下列物质:①钠 ②金刚石 ③冰 ④Na2O2 ⑤MgCl2 ⑥氯化铵 ⑦水晶 ⑧Cl2
(1)属于原子晶体的是_________ ,属于金属晶体的是_________ 。
(2)既含有离子键又含有共价键的是_________ 。
(3)③熔化时克服作用力的有_________ 。
(4)Na2O2的电子式________________ 。
(5)②、③、⑤、⑦、⑧熔点由低到高的顺序为________________ 。
II.在生产生活以及化学科学研究中,水都有重要的作用。
(1)与H2O分子是等电子体的微粒_________ (阴离子及分子各写一个)。
(2)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是__________ 。
A.微粒的形状发生了改变
B.氧原子的杂化类型发生了改变
C.微粒中的键角发生了改变
D.微粒的化学性质发生了改变
(3)向CuSO4溶液中加入氨水,溶液变成深蓝色,请写出发生此变化的离子方程式______________ 。
(1)属于原子晶体的是
(2)既含有离子键又含有共价键的是
(3)③熔化时克服作用力的有
(4)Na2O2的电子式
(5)②、③、⑤、⑦、⑧熔点由低到高的顺序为
II.在生产生活以及化学科学研究中,水都有重要的作用。
(1)与H2O分子是等电子体的微粒
(2)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是
A.微粒的形状发生了改变
B.氧原子的杂化类型发生了改变
C.微粒中的键角发生了改变
D.微粒的化学性质发生了改变
(3)向CuSO4溶液中加入氨水,溶液变成深蓝色,请写出发生此变化的离子方程式
更新时间:2019-06-26 19:12:37
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】N、Cu、H、O、S、Mg是常见的六种元素。
(1)Mg位于元素周期表第_______ 周期第_______ 族;N与O的基态原子核外未成对电子个数比为_______ ;Cu的基态原子电子排布式为_______ 。
(2)用“>”或“<”填空:
碱性:Mg(OH)2_______ Cu(OH)2
第一电离能:O_______ N
熔点:MgS_______ MgO
稳定性:H2S_______ H2O
(3)Mg在空气中燃烧可微量生产氮化镁(Mg3N2),Mg3N2(S)溶于足量的稀硫酸可得到两种正盐,在25℃、101kPa下,已知该反应每消耗1molH2SO4放热akJ,则该反应的热化学方程式为_______ 。
(4)工业上采取加热条件下用氨气还原氧化铜制取铜,同时得到两种无污染的气体(或蒸汽),写出该反应的化学方程式,并标出电子转移的方向和数目_______ 。
(1)Mg位于元素周期表第
(2)用“>”或“<”填空:
碱性:Mg(OH)2
第一电离能:O
熔点:MgS
稳定性:H2S
(3)Mg在空气中燃烧可微量生产氮化镁(Mg3N2),Mg3N2(S)溶于足量的稀硫酸可得到两种正盐,在25℃、101kPa下,已知该反应每消耗1molH2SO4放热akJ,则该反应的热化学方程式为
(4)工业上采取加热条件下用氨气还原氧化铜制取铜,同时得到两种无污染的气体(或蒸汽),写出该反应的化学方程式,并标出电子转移的方向和数目
您最近一年使用:0次
【推荐2】我国科学家通过测量SiO2中26Al和16Be两种元素的比例确定“北京人”年龄,这种测量方法叫“铝铍测年法”,完成下列填空:
(1)写出Be的核外电子排布式___ ,Be所在的周期中,最外层有2个未成对电子的元素的符号有___ 、___ 。
(2)Al和Be具有相似的化学性质,铝原子核外有___ 种不同运动状态的电子,写出BeCl2水解反应的化学方程式:___ 。
(3)研究表明26Al可以衰变为26Mg。请从原子结构角度解释这两种元素金属性强弱关系___ 。
(4)比较Al3+、S2﹣和Cl﹣半径由大到小的顺序___ ;这3种元素最高价氧化物对应的水化物中酸性最强的是___ (写名称),Al2O3是离子化合物,而AlCl3是共价化合物。工业制铝时,电解Al2O3而不电解AlCl3的原因是___ 。
(1)写出Be的核外电子排布式
(2)Al和Be具有相似的化学性质,铝原子核外有
(3)研究表明26Al可以衰变为26Mg。请从原子结构角度解释这两种元素金属性强弱关系
(4)比较Al3+、S2﹣和Cl﹣半径由大到小的顺序
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】与溶液条件相比,晶体条件下发生的反应有产物选择性高、易于分离提纯等优点。

(1)氟元素在有机晶体化学领域的研究和应用中有重要价值。
①氟元素在元素周期表中的位置为___________ ,六氟苯中碳原子的杂化方式为___________ 。
②苯环上的电子云密度:苯___________ 六氟苯(填“>”或“<”),依据电负性解释其原因:___________ 。
(2)分子间作用力影响晶体中分子的堆积方式,进而影响物质的性质和反应的选择性。
①已知:苯和六氟苯的熔点分别为5.5oC和5.2oC,将二者混合后得到的“混晶”(二者比例为1:1),其熔点上升至23.7oC。
三种晶体中的分子间作用力最大的是___________ (填“苯”、“六氟苯”或“混晶”)。
②已知:紫外光下,两个碳碳双键可加成为四元环(环丁烷)的结构。
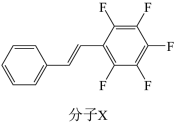
紫外光下,分子X在溶液条件下反应得到2种互为同分异构体的加成产物,在晶体条件下只能生成1种加成产物Z,推测Z的结构简式为___________ (不考虑立体异构)。
(3)A与B经以下两种途径均可获得E。

已知:―N3与―C≡CH在铜盐催化条件下可发生加成反应得到含 结构的分子。E的结构简式为
结构的分子。E的结构简式为___________ 。

(1)氟元素在有机晶体化学领域的研究和应用中有重要价值。
①氟元素在元素周期表中的位置为
②苯环上的电子云密度:苯
(2)分子间作用力影响晶体中分子的堆积方式,进而影响物质的性质和反应的选择性。
①已知:苯和六氟苯的熔点分别为5.5oC和5.2oC,将二者混合后得到的“混晶”(二者比例为1:1),其熔点上升至23.7oC。
三种晶体中的分子间作用力最大的是
②已知:紫外光下,两个碳碳双键可加成为四元环(环丁烷)的结构。
紫外光下,分子X在溶液条件下反应得到2种互为同分异构体的加成产物,在晶体条件下只能生成1种加成产物Z,推测Z的结构简式为

(3)A与B经以下两种途径均可获得E。

已知:―N3与―C≡CH在铜盐催化条件下可发生加成反应得到含
 结构的分子。E的结构简式为
结构的分子。E的结构简式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】乙炔 和丙烯腈
和丙烯腈 是有机合成工业的重要原料。工业上曾用
是有机合成工业的重要原料。工业上曾用 和
和 反应制取乙炔,用乙炔和氢氰酸
反应制取乙炔,用乙炔和氢氰酸 在氯化亚铜等催化作用下生产丙烯腈。
在氯化亚铜等催化作用下生产丙烯腈。
(1) 的基态核外电子排布式为
的基态核外电子排布式为_______ 。 元素在周期表中的位置为
元素在周期表中的位置为_______ 。无水 晶体是白色的,溶于水得蓝色溶液,显蓝色的离子的化学式为
晶体是白色的,溶于水得蓝色溶液,显蓝色的离子的化学式为_______ 。
(2) 的电子式为
的电子式为_______ 。
(3)与 互为等电子体的分子是
互为等电子体的分子是_______ (填常见稳定物质的化学式)。
(4)丙烯腈分子中碳原子的杂化轨道类型是_______ 。
(5) 丙烯腈分子中含
丙烯腈分子中含 键的物质的量为
键的物质的量为_______ mol。
(6)丙烯腈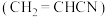 分子中共面的原子数目最多为
分子中共面的原子数目最多为_______ 。
(7) 分子的价电子对分布的几何构型是
分子的价电子对分布的几何构型是_______ ,分子的空间结构是_______ 。水凝结成冰,冰中水分子的配位数是_______ ,冰的密度比水小,原因是_______ 。
 和丙烯腈
和丙烯腈 是有机合成工业的重要原料。工业上曾用
是有机合成工业的重要原料。工业上曾用 和
和 反应制取乙炔,用乙炔和氢氰酸
反应制取乙炔,用乙炔和氢氰酸 在氯化亚铜等催化作用下生产丙烯腈。
在氯化亚铜等催化作用下生产丙烯腈。(1)
 的基态核外电子排布式为
的基态核外电子排布式为 元素在周期表中的位置为
元素在周期表中的位置为 晶体是白色的,溶于水得蓝色溶液,显蓝色的离子的化学式为
晶体是白色的,溶于水得蓝色溶液,显蓝色的离子的化学式为(2)
 的电子式为
的电子式为(3)与
 互为等电子体的分子是
互为等电子体的分子是(4)丙烯腈分子中碳原子的杂化轨道类型是
(5)
 丙烯腈分子中含
丙烯腈分子中含 键的物质的量为
键的物质的量为(6)丙烯腈
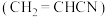 分子中共面的原子数目最多为
分子中共面的原子数目最多为(7)
 分子的价电子对分布的几何构型是
分子的价电子对分布的几何构型是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)Co基态原子核外电子排布式为______ 。元素Mn与O中,第一电离能较大的是________ ,基态原子核外未成对电子数较多的是________________ 。
(2)CO2和CH3OH分子中C原子的杂化形式分别为__________ 和__________ 。
(3)在CO2和H2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为_______ ,原因是_____________ 。
(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在________ 。
(1)Co基态原子核外电子排布式为
(2)CO2和CH3OH分子中C原子的杂化形式分别为
(3)在CO2和H2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为
(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】
(1)分别将O2、KO2、 BaO2 和O2[AsF6]填入与O- O键长相对应的空格中。
(2)在配合物A和B中,O2为配体与中心金属离子配位。A的化学式为[Co2O2(NH3)10]4+,其O- O的键长为147 pm; B的化学式为Co(bzacen)PyO2,其O- O的键长为126 pm, Py 是吡啶(C5H5N),bzacen 是四齿配体[C6H5 -C(O-)=CH -C(CH3) =NCH2- ]2.B具有室温吸氧,加热脱氧的功能,可作为人工载氧体。画出A和B的结构简图(图中必须明确表明O-O与金属离子间的空间关系),并分别指出A和B中Co的氧化态。
(1)分别将O2、KO2、 BaO2 和O2[AsF6]填入与O- O键长相对应的空格中。
| O- O键长 | 112 pm | 121 pm | 128 pm | 149 pm |
| 化学式 |
(2)在配合物A和B中,O2为配体与中心金属离子配位。A的化学式为[Co2O2(NH3)10]4+,其O- O的键长为147 pm; B的化学式为Co(bzacen)PyO2,其O- O的键长为126 pm, Py 是吡啶(C5H5N),bzacen 是四齿配体[C6H5 -C(O-)=CH -C(CH3) =NCH2- ]2.B具有室温吸氧,加热脱氧的功能,可作为人工载氧体。画出A和B的结构简图(图中必须明确表明O-O与金属离子间的空间关系),并分别指出A和B中Co的氧化态。
| 配合物 | a | b |
| 结构简图 | ||
| Co的氧化态 |
您最近一年使用:0次
【推荐2】Ⅰ.无水 与
与 作用会生成
作用会生成 。现有
。现有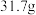 无水
无水 ,吸收
,吸收 后变成
后变成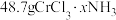 ,试回答下列问题:
,试回答下列问题:
(1) 中
中
______ 。
(2) 为配合物,其中
为配合物,其中 的配位数为6,经测定
的配位数为6,经测定 该配合物和足量
该配合物和足量 溶液反应得到
溶液反应得到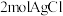 沉淀,则该配合物的化学式可表示为
沉淀,则该配合物的化学式可表示为______ 。
Ⅱ.将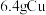 溶于
溶于 过量的硝酸溶液中,假设硝酸的还原产物只有
过量的硝酸溶液中,假设硝酸的还原产物只有 和
和 。反应结束后,将所得的溶液加水稀释至
。反应结束后,将所得的溶液加水稀释至 ,测得
,测得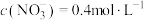 。(假设生成气体完全逸出)。请计算:
。(假设生成气体完全逸出)。请计算:
(3)稀释后溶液中 的物质的量浓度
的物质的量浓度______ 
(4)生成的气体中 物质的量
物质的量______  (用含有
(用含有 的表达式表示)
的表达式表示)
 与
与 作用会生成
作用会生成 。现有
。现有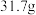 无水
无水 ,吸收
,吸收 后变成
后变成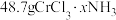 ,试回答下列问题:
,试回答下列问题:(1)
 中
中
(2)
 为配合物,其中
为配合物,其中 的配位数为6,经测定
的配位数为6,经测定 该配合物和足量
该配合物和足量 溶液反应得到
溶液反应得到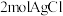 沉淀,则该配合物的化学式可表示为
沉淀,则该配合物的化学式可表示为Ⅱ.将
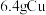 溶于
溶于 过量的硝酸溶液中,假设硝酸的还原产物只有
过量的硝酸溶液中,假设硝酸的还原产物只有 和
和 。反应结束后,将所得的溶液加水稀释至
。反应结束后,将所得的溶液加水稀释至 ,测得
,测得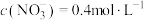 。(假设生成气体完全逸出)。请计算:
。(假设生成气体完全逸出)。请计算:(3)稀释后溶液中
 的物质的量浓度
的物质的量浓度
(4)生成的气体中
 物质的量
物质的量 (用含有
(用含有 的表达式表示)
的表达式表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】有下列八种晶体:
①水晶 ②干冰 ③氟化钠 ④固态氩 ⑤金属铝 ⑥碳化硅 ⑦氢氧化钠 ⑧白磷
试回答:
(1)直接由原子构成的晶体是__ 。
(2)含有共价键的晶体是__ 。
(3)含有阳离子的晶体是__ ,含有阴离子的晶体是__ 。
(4)熔化需克服共价键的晶体是__ ,熔化能导电的晶体是__ 。
①水晶 ②干冰 ③氟化钠 ④固态氩 ⑤金属铝 ⑥碳化硅 ⑦氢氧化钠 ⑧白磷
试回答:
(1)直接由原子构成的晶体是
(2)含有共价键的晶体是
(3)含有阳离子的晶体是
(4)熔化需克服共价键的晶体是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氟在自然界中常以CaF2的形式存在。
(1)下列有关CaF2的表述正确的是___________ 。
a.Ca2+与F-间仅存在静电吸引作用
b.F-的离子半径小于Cl-,则CaF2的熔点高于CaCl2
c.阴阳离子比为2∶1的物质,均与CaF2晶体构型相同
d.CaF2中的化学键为离子键,因此CaF2在熔融状态下能导电
(2)F2通入稀NaOH溶液中可生成OF2,OF2分子构型为___________ ,其中氧原子的杂化方式为___________ 。
(3)单质铜及镍都是由___________ 键形成的晶体:元素铜与镍的第二电离能分别为:ICu=1959kJ/mol,INi=1753kJ/mol,ICu>INi的原因是___________ 。
(1)下列有关CaF2的表述正确的是
a.Ca2+与F-间仅存在静电吸引作用
b.F-的离子半径小于Cl-,则CaF2的熔点高于CaCl2
c.阴阳离子比为2∶1的物质,均与CaF2晶体构型相同
d.CaF2中的化学键为离子键,因此CaF2在熔融状态下能导电
(2)F2通入稀NaOH溶液中可生成OF2,OF2分子构型为
(3)单质铜及镍都是由
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】根据要求回答下列问题:
I. ①H、D、T ②H2O、D2O ③石墨、金刚石 ④ 和
和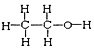
四组微粒或物质中,互为同位素的是_______ ;(填序号,下同) 互为同素异形体的是_____ 。
II.现有①金刚石 ②干冰 ③Na2SO4 ④NH4Cl 四种物质,按下列要求回答:
(1)晶体熔化时需要破坏共价键的是_____ (填序号,下同);
(2)熔点最低的是_______
(3)晶体中只存在一种微粒作用力是_______ ;
(4)属于离子晶体的是________ 。
I. ①H、D、T ②H2O、D2O ③石墨、金刚石 ④
 和
和
四组微粒或物质中,互为同位素的是
II.现有①金刚石 ②干冰 ③Na2SO4 ④NH4Cl 四种物质,按下列要求回答:
(1)晶体熔化时需要破坏共价键的是
(2)熔点最低的是
(3)晶体中只存在一种微粒作用力是
(4)属于离子晶体的是
您最近一年使用:0次

 NH2)沸点高于甲苯(
NH2)沸点高于甲苯( CH3)的主要原因是
CH3)的主要原因是

