已知A,B,C,D,E,F均为周期表中前36号元素,且原子序数依次增大.A,B,C为同一周期的主族元素,B原子p能级电子总数与s能级电子总数相等.A,F原子未成对电子是同周期中最多的,且F基态原子中电子占据三种不同形状的原子轨道.D和E原子的第一至第四电离能如下表所示:
(1)A,B,C三种元素的电负性最大的是__ (填写元素符号),D,E两元素中D的第一电离能较大的原因是__ .
(2)F基态原子的核外电子排布式是__ ;在一定条件下,F原子的核外电子从基态跃迁到激发态产生的光谱属于__ 光谱(填“吸收”或“发射”).
(3)根据等电子原理,写出AB+的电子式:__ .
(4)已知:F3+可形成配位数为6的配合物.组成为FCl3•6H2O的配合物有3种,分别呈紫色、蓝绿色、绿色,为确定这3种配合物的成键情况,分别取等质量的紫色、蓝绿色、绿色3种物质的样品配成溶液,分别向其中滴入过量的AgNO3溶液,均产生白色沉淀且质量比为3:2:1.则绿色配合物的化学式为__ .
A [CrCl(H2O)5]Cl2•H2O B [CrCl2(H2O)4]Cl•2H2O
C [Cr(H2O)6]Cl3 D [CrCl3(H2O)3]•3H2O
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| D | 738 | 1451 | 7733 | 10540 |
| E | 578 | 1817 | 2745 | 11578 |
(2)F基态原子的核外电子排布式是
(3)根据等电子原理,写出AB+的电子式:
(4)已知:F3+可形成配位数为6的配合物.组成为FCl3•6H2O的配合物有3种,分别呈紫色、蓝绿色、绿色,为确定这3种配合物的成键情况,分别取等质量的紫色、蓝绿色、绿色3种物质的样品配成溶液,分别向其中滴入过量的AgNO3溶液,均产生白色沉淀且质量比为3:2:1.则绿色配合物的化学式为
A [CrCl(H2O)5]Cl2•H2O B [CrCl2(H2O)4]Cl•2H2O
C [Cr(H2O)6]Cl3 D [CrCl3(H2O)3]•3H2O
9-10高二下·江苏·期末 查看更多[4]
更新时间:2019-07-03 10:38:17
|
相似题推荐
【推荐1】A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同族,它们原子的最外层电子排布式为ns1。B和D也属同族,它们原子最外层的p能级电子数是s能级电子数的两倍。C原子的最外层电子数等于D原子的最外层电子数的一半。请回答下列问题:
(1)A是____ ,B是____ ,E是____ 。
(2)写出C元素基态原子的电子排布式:________________ 。
(3)用电子排布图表示D元素原子的价电子构型:__________ 。
(4)元素B与D的电负性的大小关系是B____ (填“>”“<”或“=”,下同)D,E与C的第一电离能大小关系是E____ C。
(5)写出元素E和C的最高价氧化物对应的水化物之间反应的离子方程式
_________________________________________ 。
(1)A是
(2)写出C元素基态原子的电子排布式:
(3)用电子排布图表示D元素原子的价电子构型:
(4)元素B与D的电负性的大小关系是B
(5)写出元素E和C的最高价氧化物对应的水化物之间反应的离子方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】氟代硼铍酸钾晶体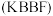 是一种非线性光学晶体材料,能够将激光转化为史无前例的176纳米波长(深紫外)激光,从而可以制造出深紫外固体激光器。回答下列问题:
是一种非线性光学晶体材料,能够将激光转化为史无前例的176纳米波长(深紫外)激光,从而可以制造出深紫外固体激光器。回答下列问题:
(1)基态K原子核外电子排布式为___________ ,在该原子中,原子轨道能量: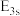
___________ (填“>”或“<”,下同)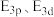
___________ 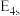 。
。
(2)上述四种元素中,第一电离能最小的是___________ (填元素符号,下同),电负性最大的是___________ 。
(3) 的空间构型为
的空间构型为___________ , 的杂化类型为
的杂化类型为___________ , 的键角比
的键角比 的键角
的键角___________ (填“大”或“小”),用价层电子对互斥理论解释原因为___________ 。
(4)已知晶体硼的熔、沸点及硬度数据和基本结构单元(由硼原子组成的正二十面体如图所示,每个三角形均为正三角形,每个顶点为一个硼原子)如下:
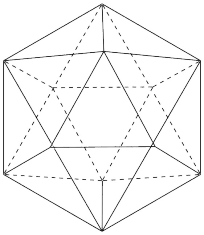
①晶体硼属于___________ 晶体,其理由是___________ 。
②每一个硼基本单元由___________ 个原子组成。
(5)已知 晶体具有
晶体具有 型结构,在
型结构,在 测出
测出 晶体密度为
晶体密度为 。
。 晶胞边长为
晶胞边长为___________  (阿伏加德罗常数用
(阿伏加德罗常数用 表示)。
表示)。
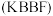 是一种非线性光学晶体材料,能够将激光转化为史无前例的176纳米波长(深紫外)激光,从而可以制造出深紫外固体激光器。回答下列问题:
是一种非线性光学晶体材料,能够将激光转化为史无前例的176纳米波长(深紫外)激光,从而可以制造出深紫外固体激光器。回答下列问题:(1)基态K原子核外电子排布式为
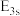
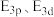
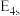 。
。(2)上述四种元素中,第一电离能最小的是
(3)
 的空间构型为
的空间构型为 的杂化类型为
的杂化类型为 的键角比
的键角比 的键角
的键角(4)已知晶体硼的熔、沸点及硬度数据和基本结构单元(由硼原子组成的正二十面体如图所示,每个三角形均为正三角形,每个顶点为一个硼原子)如下:
| 晶体 | 金刚石 | 晶体硅 | 晶体硼 |
| 熔点(K) | 3832 | 1683 | 2573 |
| 沸点(K) | 5100 | 2628 | 3823 |
| 硬度 | 10 | 7.0 | 9.6 |

①晶体硼属于
②每一个硼基本单元由
(5)已知
 晶体具有
晶体具有 型结构,在
型结构,在 测出
测出 晶体密度为
晶体密度为 。
。 晶胞边长为
晶胞边长为 (阿伏加德罗常数用
(阿伏加德罗常数用 表示)。
表示)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】化合物M的结构如图所示,其中X、Y、Z、Q、W为原子序数依次增大的五种短周期元素,Q核外最外层电子数与Y核外电子总数相同,X是元素周期表中原子半径最小的原子。

(1)M的化学键类型有______ ,其阴离子结构简式为______ ,Y的杂化方式为______ 。
(2)Y、Z、Q第一电离能大到小的顺序是______ (用元素符号填空)。
(3)由X、Z形成ZX3分子的空间构型是______ 。
(4)基态Z原子价电子排布图为______ 。
(5)X2Z-ZX2分子中孤电子对与σ键的数目之比为______ ,其相对分子质量与Y2X4分子接近,但沸点远高于Y2X4的原因是______ 。

(1)M的化学键类型有
(2)Y、Z、Q第一电离能大到小的顺序是
(3)由X、Z形成ZX3分子的空间构型是
(4)基态Z原子价电子排布图为
(5)X2Z-ZX2分子中孤电子对与σ键的数目之比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】80%左右的非金属元素在现代技术包括能源、功能材料等领域占有极为重要的地位。
(1)氮及其化合物与人类生产、生活息息相关,基态N原子中电子在2p轨道上的排布遵循的原则是________ ,N2F2分子中N原子的杂化方式是____________ ,1mol N2F2含有______ 个σ键。
(2)高温陶瓷材料Si3N4晶体中键角N—Si—N________ Si—N—Si(填“>”“<”或“=”),原因是_________ 。
金属元素在现代工业中也占据极其重要的地位,钛被称为“未来的钢铁”,具有质轻,抗腐蚀,硬度大特点,是理想化工设备材料。
(3)基态钛原子核外共有________ 种运动状态不相同的电子。金属钛晶胞如下图1所示,为_______ 堆积(填堆积方式)。
(4)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下图2。化合物乙的沸点明显高于化合物甲,主要原因是_______ 。化合物乙中采取sp3杂化的原子的电负性由大到小的顺序为__________ 。


(5)钙钛矿晶体的结构如图3所示。假设把氧离子看做硬球接触模型,钙离子和钛离子填充氧离子的空隙,氧离子形成正八面体,钛离子位于正八面体中心,则一个钛离子被__________ 个氧离子包围。
(1)氮及其化合物与人类生产、生活息息相关,基态N原子中电子在2p轨道上的排布遵循的原则是
(2)高温陶瓷材料Si3N4晶体中键角N—Si—N
金属元素在现代工业中也占据极其重要的地位,钛被称为“未来的钢铁”,具有质轻,抗腐蚀,硬度大特点,是理想化工设备材料。
(3)基态钛原子核外共有
(4)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下图2。化合物乙的沸点明显高于化合物甲,主要原因是


(5)钙钛矿晶体的结构如图3所示。假设把氧离子看做硬球接触模型,钙离子和钛离子填充氧离子的空隙,氧离子形成正八面体,钛离子位于正八面体中心,则一个钛离子被
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】阅读资料,获取信息,回答问题。
(A) A、 B、C、D为四种元素,A原子的1S轨道为半充满;在元素周期表中,B的电负性最大;C的原子序数为24;D2+的电子排布式和Ar相同。
(B)两元素电负性差值大于1. 7,原子间一般形成离子键;小于1. 7,原子间一般形成共价键。
(C)下列是周期表中部分元素的电负性x和第一电离能I1 (KJ·mol-1):

(1).A原子的轨道表示式为_______ ,B原子的价电子排布式为________ ,C原子的电
子排布式为___________ ,D在周期表中的位置为________ 周期________ 族。
(2).电负性最小的元素位于______ 族,第一电离能最大的元素是(填元素符号)______ ;
锂元素的电负性取值范围为____ <x(Li)<_____ ;A12S3属______ 化合物
(3)标出化合物OF2、 LiAlH4中各元素的化合价(写在元素符号上)____ 、____ 。
(A) A、 B、C、D为四种元素,A原子的1S轨道为半充满;在元素周期表中,B的电负性最大;C的原子序数为24;D2+的电子排布式和Ar相同。
(B)两元素电负性差值大于1. 7,原子间一般形成离子键;小于1. 7,原子间一般形成共价键。
(C)下列是周期表中部分元素的电负性x和第一电离能I1 (KJ·mol-1):

(1).A原子的轨道表示式为
子排布式为
(2).电负性最小的元素位于
锂元素的电负性取值范围为
(3)标出化合物OF2、 LiAlH4中各元素的化合价(写在元素符号上)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】砷的化合物应用非常广泛,如有机砷化物、含铁和砷的超导材料(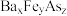 、
、 )等。
)等。
回答下列问题:
(1)基态砷原子处于最高能级的电子云轮廓图为___________ 形。
(2) 的基态核外电子排布式为
的基态核外电子排布式为 ___________
(3) 、As、O、F的电负性从大到小的顺序为
、As、O、F的电负性从大到小的顺序为 ___________  用元素符号填空
用元素符号填空 。
。
(4) 、
、 、
、 是同主族元素的氢化物,其中键角最小的是
是同主族元素的氢化物,其中键角最小的是 ___________ 。
(5)图(a)(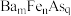 )是从自然界中分离出的一种多砷化合物,该分子中
)是从自然界中分离出的一种多砷化合物,该分子中 的杂化类型为
的杂化类型为 ___________ ,As的杂化类型为 ___________ 。

(6)一种含砷有机物的结构如图(b)所示, 该有机物中含
该有机物中含 键的物质的量为
键的物质的量为 ___________  。
。
(7)一种铁基超导化合物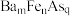 ,的晶胞结构如图(c),则该超导化合物的化学式为
,的晶胞结构如图(c),则该超导化合物的化学式为 ___________ ,已知晶胞边长为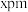 ,高为
,高为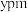 ,该晶体的密度为
,该晶体的密度为 ___________  。
。
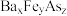 、
、 )等。
)等。回答下列问题:
(1)基态砷原子处于最高能级的电子云轮廓图为
(2)
 的基态核外电子排布式为
的基态核外电子排布式为 (3)
 、As、O、F的电负性从大到小的顺序为
、As、O、F的电负性从大到小的顺序为  用元素符号填空
用元素符号填空 。
。(4)
 、
、 、
、 是同主族元素的氢化物,其中键角最小的是
是同主族元素的氢化物,其中键角最小的是 (5)图(a)(
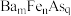 )是从自然界中分离出的一种多砷化合物,该分子中
)是从自然界中分离出的一种多砷化合物,该分子中 的杂化类型为
的杂化类型为 
(6)一种含砷有机物的结构如图(b)所示,
 该有机物中含
该有机物中含 键的物质的量为
键的物质的量为  。
。(7)一种铁基超导化合物
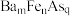 ,的晶胞结构如图(c),则该超导化合物的化学式为
,的晶胞结构如图(c),则该超导化合物的化学式为 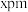 ,高为
,高为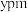 ,该晶体的密度为
,该晶体的密度为  。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】我国科学家利用甲胺盐(CH3NH3I)和PbI2制备太阳能电池材料CH3NH3PbI3,回答下列问题:
(1)基态Pb原子的价层电子排布式为____ 。
(2)CH3NH3I中含有离子键和下列共价键中的____ (填标号);CH3NH 的一种等电子体的分子式为
的一种等电子体的分子式为____ 。
A.σ键 B.π键 C.配位键 D.非极性键
(3)[Pb2(dnob)2(phen)3(H2O)]n是Pb的一种配位聚合物,dnob、phen分别为 、
、 。其中C、N、O的第一电离能由小到大的顺序为
。其中C、N、O的第一电离能由小到大的顺序为____ ;C、N的杂化方式分别为____ 、____ 。
(4)CH3NH3PbI3的晶体属于立方晶系,两个晶胞无隙并置的结构如图所示。其中CH3NH 、Pb2+、I-分别位于晶胞的顶点、体心和面心。
、Pb2+、I-分别位于晶胞的顶点、体心和面心。
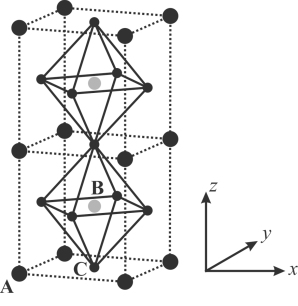
①每个晶胞含有____ 个I-。
②以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子(若为原子团,视为原子处理)的位置,称为原子坐标。在该图中,A点CH3NH 的原子坐标为(0,0,0),B点Pb2+的原子坐标为(
的原子坐标为(0,0,0),B点Pb2+的原子坐标为( ,
, ,
, ),则C点I-的原子坐标为
),则C点I-的原子坐标为____ ;晶体中1个CH3NH 与
与____ 个I-等距离且最近;已知该晶体的密度为ρg·cm-3,AC之间的距离为dpm,则阿伏加德罗常数的值NA=____ mol-1。
(1)基态Pb原子的价层电子排布式为
(2)CH3NH3I中含有离子键和下列共价键中的
 的一种等电子体的分子式为
的一种等电子体的分子式为A.σ键 B.π键 C.配位键 D.非极性键
(3)[Pb2(dnob)2(phen)3(H2O)]n是Pb的一种配位聚合物,dnob、phen分别为
 、
、 。其中C、N、O的第一电离能由小到大的顺序为
。其中C、N、O的第一电离能由小到大的顺序为(4)CH3NH3PbI3的晶体属于立方晶系,两个晶胞无隙并置的结构如图所示。其中CH3NH
 、Pb2+、I-分别位于晶胞的顶点、体心和面心。
、Pb2+、I-分别位于晶胞的顶点、体心和面心。
①每个晶胞含有
②以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子(若为原子团,视为原子处理)的位置,称为原子坐标。在该图中,A点CH3NH
 的原子坐标为(0,0,0),B点Pb2+的原子坐标为(
的原子坐标为(0,0,0),B点Pb2+的原子坐标为( ,
, ,
, ),则C点I-的原子坐标为
),则C点I-的原子坐标为 与
与
您最近一年使用:0次
【推荐2】高氯酸三碳酰肼合镍的化学式为[NiA3](ClO4)2,它是一种新型的起爆药,可由NiO、HClO4及有机物A化合而成,A称为碳酰肼,组成为CO(N2H3)2。请回答下列问题:
(1)Ni在周期表中的位置是________________ ,Ni2+核外有_________ 个未成对电子。
(2)ClO 中氯原子的轨道杂化类型为
中氯原子的轨道杂化类型为_______ ,与Cl 互为等电子体的分子、离子分别是
互为等电子体的分子、离子分别是_________ (填化学式,分子、离子各填一种)。
(3)1.8 g A分子中含有σ键的数目为__________________ 。(用NA表示)
(4)①NiO晶胞结构如图所示,与Ni2+最近且等距离的Ni2+有_____________ 个。已知NiO晶胞的密度为ρ g·cm−3,则晶胞边长为______________ cm。
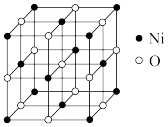
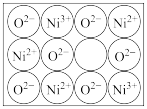
②天然的和绝大部分人工制备的晶体都存在各种缺陷。某种NiO晶体中就存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代,其晶体仍呈电中性,但化合物中Ni和O的个数比却发生了变化,经测定某氧化镍晶体样品中N(Ni2+)∶N(Ni3+)=91∶6,则该晶体中氧元素的质量分数为____________ (保留4位有效数字)。
(1)Ni在周期表中的位置是
(2)ClO
 中氯原子的轨道杂化类型为
中氯原子的轨道杂化类型为 互为等电子体的分子、离子分别是
互为等电子体的分子、离子分别是(3)1.8 g A分子中含有σ键的数目为
(4)①NiO晶胞结构如图所示,与Ni2+最近且等距离的Ni2+有

②天然的和绝大部分人工制备的晶体都存在各种缺陷。某种NiO晶体中就存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代,其晶体仍呈电中性,但化合物中Ni和O的个数比却发生了变化,经测定某氧化镍晶体样品中N(Ni2+)∶N(Ni3+)=91∶6,则该晶体中氧元素的质量分数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
(1)水分子的中心原子价层电子对数为________ ;水分子的空间构型为________ 。
(2)写出与H2O分子互为等电子体的离子___________ (填1种)。
(3)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是___________ 。
A.氧原子的杂化类型发生了改变 B.微粒的形状发生了改变
C.微粒的化学性质发生了改变 D.微粒中的键角发生了改变
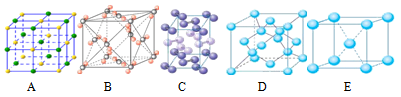
(4)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是___________ (请用相应的编号填写)。
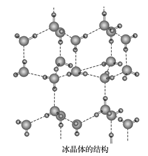
(5)在冰晶体中,每个水分子与相邻的 4个水分子形成氢键(如图所示),已知冰的升华热是 51kJ/mol,除氢键外,水分子间还存在范德华力(11kJ/mol),则冰晶体中氢键的“键能 ” 是___________ kJ/mol;
(6)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子, 请写出生成此配合离子的离子方程式:___________ 。
(1)水分子的中心原子价层电子对数为
(2)写出与H2O分子互为等电子体的离子
(3)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是
A.氧原子的杂化类型发生了改变 B.微粒的形状发生了改变
C.微粒的化学性质发生了改变 D.微粒中的键角发生了改变
(4)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是

(5)在冰晶体中,每个水分子与相邻的 4个水分子形成氢键(如图所示),已知冰的升华热是 51kJ/mol,除氢键外,水分子间还存在范德华力(11kJ/mol),则冰晶体中氢键的“键能 ” 是

(6)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子, 请写出生成此配合离子的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】Al、Cr、Co、Ni的合金及其相关化合物用途非常广泛,如锂离子电池的正极材料为LiCoO2,电解质溶液为LiBF4溶液。
(1)Co2+的基态核外电子排布式为_______ 。
(2)钴元素可形成种类繁多的配合物。三氯五氨合钴的化学式为Co(NH3)5Cl3,是一种典型的维尔纳配合物,具有反磁性。0.01molCo(NH3)5Cl3与足量硝酸银溶液反应时生成2.87g白色沉淀。Co(NH3)5Cl3中Co3+的配位数为_______ ,该配合物中的配位原子为_______ 。
(3)1951年Tsao最早报道了用LiAlH4还原腈:

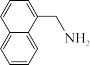 。
。
①LiAlH4中三种元素的电负性从大到小的顺序为_______ (用元素符号表示)。
② 中碳原子的轨道杂化类型为
中碳原子的轨道杂化类型为_______ ,1mol该分子中含σ键的物质的量为_______ 。
(4)全惠斯勒合金CrxCoyAlz的晶胞结构如图甲所示,其化学式为_______ 。
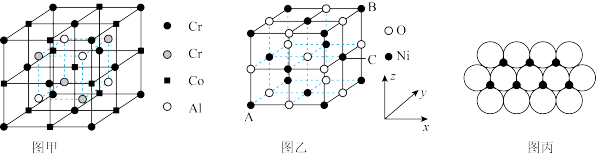
(5)NiO的晶胞结构如图乙所示其中离子坐标参数A为(0,0,0),则C的离子坐标参数为_______ 。一定温度下,NiO晶体可以自发地分散并形成“单分子层”可以认为O2-作密置单层排列,Ni2+填充其中(如图丙),已知O2-的半径为apm,设阿伏加德罗常数的值为NA,每平方米的面积上具有该晶体的质量为_______ g(用含a、NA的代数式表示,Ni的相对原子质量为59)。
(1)Co2+的基态核外电子排布式为
(2)钴元素可形成种类繁多的配合物。三氯五氨合钴的化学式为Co(NH3)5Cl3,是一种典型的维尔纳配合物,具有反磁性。0.01molCo(NH3)5Cl3与足量硝酸银溶液反应时生成2.87g白色沉淀。Co(NH3)5Cl3中Co3+的配位数为
(3)1951年Tsao最早报道了用LiAlH4还原腈:


 。
。①LiAlH4中三种元素的电负性从大到小的顺序为
②
 中碳原子的轨道杂化类型为
中碳原子的轨道杂化类型为(4)全惠斯勒合金CrxCoyAlz的晶胞结构如图甲所示,其化学式为

(5)NiO的晶胞结构如图乙所示其中离子坐标参数A为(0,0,0),则C的离子坐标参数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
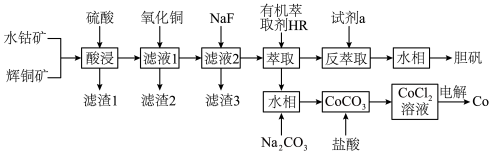
【推荐2】以水钴矿(Co2O3·H2O,含Fe2O3、MgO、CaO)和辉铜矿(Cu2S,含SiO2、Fe2O3)为原料制取胆矾和单质钴。
①常温下,Ksp(MgF2)=6.25×10-9,Ksp(CaSO4)=7.1×10-7,Ksp(CoCO3)=2.4×10-7;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
③萃取Cu2+的反应原理;Cu2++2HR CuR2+2H+;
CuR2+2H+;
④Mg、Ca、Fe、Co均能与强酸反应产生H2。
回答下列问题:
(1)“酸浸”过程硫元素价态变为+6价,写出“酸浸”过程中主要反应的化学方程式:___________ 。
(2)“滤渣1”的主要成分为___________ 。
(3)常温下,“滤液1”中(Fe元素都以Fe3+形式存在)加“氧化铜”调pH不小于___________ 。
(4)常温下,若“滤液2”中c(Mg2+)=0.015mol/L(忽略溶液中极少量的Ca2+),除去2L“滤液2”中的Mg2+,至少需加入NaF固体的质量为___________ g(忽略溶液体积的变化)。
(5)“反萃取”步骤中加入的“试剂a”为___________ 。
(6)采用惰性电极电解CoCl2溶液﹑在无离子交换膜的条件下,不能用CoSO4溶液代替CoCl2溶液的理由是___________ 。
(7)将制得的胆矾配成溶液,先加入足量氨水,得到深蓝色溶液,再通入SO2至弱酸性,生成白色沉淀。经仪器分析:白色沉淀含H、N,O、S、Cu五种元素,且Cu∶N∶S=1∶1∶l;所含Cu离子中无单电子;晶体的部分组成微粒的空间构型分别为三角锥形和正四面体形。则白色沉淀的化学式为___________ 。
①常温下,Ksp(MgF2)=6.25×10-9,Ksp(CaSO4)=7.1×10-7,Ksp(CoCO3)=2.4×10-7;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 金属离子 | Fe3+ | Fe2+ | Co2+ | Cu2+ |
| 开始沉淀时(c=0.01mol/L)的pH | 2.7 | 7.5 | 7.6 | 4.7 |
| 完全沉淀时(c=10-5mol/L)的pH | 3.7 | 9.0 | 9.1 | 6.2 |
 CuR2+2H+;
CuR2+2H+;④Mg、Ca、Fe、Co均能与强酸反应产生H2。
回答下列问题:
(1)“酸浸”过程硫元素价态变为+6价,写出“酸浸”过程中主要反应的化学方程式:
(2)“滤渣1”的主要成分为
(3)常温下,“滤液1”中(Fe元素都以Fe3+形式存在)加“氧化铜”调pH不小于
(4)常温下,若“滤液2”中c(Mg2+)=0.015mol/L(忽略溶液中极少量的Ca2+),除去2L“滤液2”中的Mg2+,至少需加入NaF固体的质量为
(5)“反萃取”步骤中加入的“试剂a”为
(6)采用惰性电极电解CoCl2溶液﹑在无离子交换膜的条件下,不能用CoSO4溶液代替CoCl2溶液的理由是
(7)将制得的胆矾配成溶液,先加入足量氨水,得到深蓝色溶液,再通入SO2至弱酸性,生成白色沉淀。经仪器分析:白色沉淀含H、N,O、S、Cu五种元素,且Cu∶N∶S=1∶1∶l;所含Cu离子中无单电子;晶体的部分组成微粒的空间构型分别为三角锥形和正四面体形。则白色沉淀的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】英国曼彻斯特大学科学家安德烈·海姆和康斯坦丁·诺沃肖洛夫。共同工作多年的二人因“突破性地”用撕裂的方法成功获得超薄材料石墨烯而获奖。制备石墨烯方法有石墨剥离法、化学气相沉积法等。石墨烯的球棍模型示意图如下:
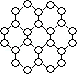
(1)下列有关石墨烯说法正确的是________________ 。
A.键长:石墨烯>金刚石
B.石墨烯分子中所有原子可以处于同一平面
C.12g石墨烯含 键数为NA
键数为NA
D.从石墨剥离得石墨烯需克服石墨层与层之间的分子间作用力
(2)化学气相沉积法是获得大量石墨烯的有效方法之一,催化剂为金、铜、钴等金属或合金,含碳源可以是甲烷、乙炔、苯、乙醇或酞菁等中的一种或任意组合。
①铜原子在基态时,在有电子填充的能级中,能量最高的能级符号为_____________ ;第四周期元素中,最外层电子数与铜相同的元素还有________________________ 。
②乙醇的沸点要高于相对分子质量比它还高的丁烷,请解释原因______________________________ 。
③下列分子属于非极性分子的是__________________ 。
a.甲烷 b.二氯甲烷 c.苯 d.乙醇
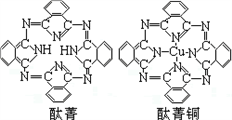
④酞菁与酞菁铜染料分子结构如图,酞菁分子中碳原子采用的杂化方式是__________ ;酞菁铜分子中心原子的配位数为________________ 。
⑤金与铜可形成的金属互化物合金(如图,该晶胞中,Au占据立方体的8个顶点):
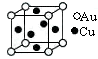
它的化学式可表示为_____ ;在Au周围最近并距离相等的Cu有_____ 个,若2个Cu原子核的最小距离为d pm,该晶体的密度可以表示为___________________ g/cm3。(阿伏伽德罗常数用NA表示)

(1)下列有关石墨烯说法正确的是
A.键长:石墨烯>金刚石
B.石墨烯分子中所有原子可以处于同一平面
C.12g石墨烯含
 键数为NA
键数为NAD.从石墨剥离得石墨烯需克服石墨层与层之间的分子间作用力
(2)化学气相沉积法是获得大量石墨烯的有效方法之一,催化剂为金、铜、钴等金属或合金,含碳源可以是甲烷、乙炔、苯、乙醇或酞菁等中的一种或任意组合。
①铜原子在基态时,在有电子填充的能级中,能量最高的能级符号为
②乙醇的沸点要高于相对分子质量比它还高的丁烷,请解释原因
③下列分子属于非极性分子的是
a.甲烷 b.二氯甲烷 c.苯 d.乙醇
④酞菁与酞菁铜染料分子结构如图,酞菁分子中碳原子采用的杂化方式是

⑤金与铜可形成的金属互化物合金(如图,该晶胞中,Au占据立方体的8个顶点):

它的化学式可表示为
您最近一年使用:0次



