下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白
(用元素符号或化学式回答下列问题)
(1)在这些元素中,化学性质最不活泼的是_______ ,其原子结构示意图是_________ 。
(2)用电子式表示元素④与⑦组成的化合物的形成过程:________ ,该化合物属于_______ (填“共价”或“离子”)化合物。
(3)常温下呈液态的非金属单质是_______ 。
(4)表中能形成两性氢氧化物的元素是_________ ,该元素的单质与⑨的最高价氧化物的水化物反应的化学方程式是___________ 。
(5)①、⑥、⑦三种元素的最高价氧化物对应的水化物中,按酸性增强的顺序排列为_________ 。
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的是
(2)用电子式表示元素④与⑦组成的化合物的形成过程:
(3)常温下呈液态的非金属单质是
(4)表中能形成两性氢氧化物的元素是
(5)①、⑥、⑦三种元素的最高价氧化物对应的水化物中,按酸性增强的顺序排列为
更新时间:2019-07-10 22:57:58
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】请根据题意回答下列问题:
(1)对于数以万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。请利用分类法结合所学知识完成下列各小题:
①现有下列9种微粒: 、
、 、
、 、
、 、
、 、
、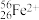 、
、 、
、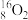 、
、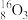 ,其中核素有
,其中核素有_______ 种,涉及到的元素有_______ 种。
②现有以下物质:①稀盐酸 ②Cl2③BaSO4固体④NaOH溶液⑤熔融的NaHSO4 ⑥CO2⑦铝条⑧蔗糖,以上物质中属于电解质的是_______ (填标号,下同),属于非电解质的是_______ 。
(2)2021年2月22日,嫦娥五号采样返回器带回的月壤公开亮相。对月壤中化学元素的分析有助于认识月球表面环境。元素周期表揭示了化学元素间的内在联系,部分元素在周期表中的位置如下:
①月壤中含有大量的g元素,g在周期表中的位置为_______ ;
②g、h、i三种元素的气态氢化物最稳定的是_______ (用化学式表示);
③根据元素周期律,请你试着写出j元素所对应的单质与a和d元素所形成的简单化合物反应的离子方程式:_______ 。
(1)对于数以万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。请利用分类法结合所学知识完成下列各小题:
①现有下列9种微粒:
 、
、 、
、 、
、 、
、 、
、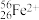 、
、 、
、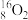 、
、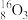 ,其中核素有
,其中核素有②现有以下物质:①稀盐酸 ②Cl2③BaSO4固体④NaOH溶液⑤熔融的NaHSO4 ⑥CO2⑦铝条⑧蔗糖,以上物质中属于电解质的是
(2)2021年2月22日,嫦娥五号采样返回器带回的月壤公开亮相。对月壤中化学元素的分析有助于认识月球表面环境。元素周期表揭示了化学元素间的内在联系,部分元素在周期表中的位置如下:
| a | |||||||||||||||||
| b | c | d | |||||||||||||||
| e | f | g | h | i | |||||||||||||
| j |
②g、h、i三种元素的气态氢化物最稳定的是
③根据元素周期律,请你试着写出j元素所对应的单质与a和d元素所形成的简单化合物反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.按要求回答下列问题:
(1)某粒子有1个原子核、核中有17个质子、20个中子,核外有18个电子,该粒子的化学符号是___________ 。
(2)写出下列物质的电子式:
NaOH___________ Cl2 ___________ NH4I ___________ 。
(3)用电子式表示下列化合物的形成过程:
Na2S___________ 。
H2O___________ 。
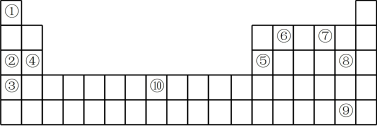
Ⅱ. 如图为元素周期表的一部分,列出了10种元素在元素周期表中的位置,试回答下列问题:___________ 。(填化学式)。
(5)10种元素中,原子半径最小的是___________ (填序号)。
(6)元素⑦的简单氢化物与元素⑧的单质反应的离子方程式为___________ 。
(7)元素②和⑤的最高价氧化物对应水化物相互反应的化学方程式为___________ 。
(8)元素⑩的原子序数为___________ 。
(9)元素⑨的单质易溶于元素⑥与⑧形成的化合物中,所得溶液颜色为___________ 色。
(1)某粒子有1个原子核、核中有17个质子、20个中子,核外有18个电子,该粒子的化学符号是
(2)写出下列物质的电子式:
NaOH
(3)用电子式表示下列化合物的形成过程:
Na2S
H2O
Ⅱ. 如图为元素周期表的一部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
(5)10种元素中,原子半径最小的是
(6)元素⑦的简单氢化物与元素⑧的单质反应的离子方程式为
(7)元素②和⑤的最高价氧化物对应水化物相互反应的化学方程式为
(8)元素⑩的原子序数为
(9)元素⑨的单质易溶于元素⑥与⑧形成的化合物中,所得溶液颜色为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】1.短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示,其中A为地壳中含量最高的金属元素。
请用化学用语回答下列问题:
1.(1)A. D、E元素简单离子半径由大到小的顺序为______ >______ >______ (填粒子符号)
(1)F与D同主族且相邻二者气态氢化物稳定性的大小关系为________ >________ (填粒子符号)
(2)用高能射线照射含有10电子的D元素氢化物分子时,一个分子能释放出一个电子,同时产生一种
具有较强氧化性的阳离子,试写出该阳离子的电子式:______________ 。 该阳离子中存在的化学键有_________ 。
(3)由C、E两种元素组成的化合物甲,常温下为易挥发的淡黄色液体,甲分子构型为三角锥形,且分子中C、E两种原子最外层均达到8个电子的稳定结构。甲遇水蒸气可形成一种常见的漂白性物质。写出甲遇水蒸气的化学方程式__________ 。
| B | C | D | ||
| A | E |
1.(1)A. D、E元素简单离子半径由大到小的顺序为
(1)F与D同主族且相邻二者气态氢化物稳定性的大小关系为
(2)用高能射线照射含有10电子的D元素氢化物分子时,一个分子能释放出一个电子,同时产生一种
具有较强氧化性的阳离子,试写出该阳离子的电子式:
(3)由C、E两种元素组成的化合物甲,常温下为易挥发的淡黄色液体,甲分子构型为三角锥形,且分子中C、E两种原子最外层均达到8个电子的稳定结构。甲遇水蒸气可形成一种常见的漂白性物质。写出甲遇水蒸气的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】动手实践:某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究____________ 元素性质递变规律。
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlC13溶液,NaOH溶液,酚酞溶液等。仪器:①__________ ,②__________ ,试管,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等。
(3)实验内容:(填写与实验步骤对应实验现象的编号和②的化学方程式及此实验的结论)__________
①_____________________________________ ,
②_____________________________________ ,
此实验的结论:_______________________________________________________ 。
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色 |
| ②向新制得的Na2S溶液中满加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体 |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体 |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉锭 |
(1)实验目的:研究
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlC13溶液,NaOH溶液,酚酞溶液等。仪器:①
(3)实验内容:(填写与实验步骤对应实验现象的编号和②的化学方程式及此实验的结论)
| 实验内容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A~F) |
②
此实验的结论:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D 同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性。回答下列问题:
(1)五种元素中,原子半径最大的是_________ ,非金属性最强的是_________ (填元素符号);
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是___________ (用化学式表示);
(3)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为______________ ,其中存在的化学键类型为_______________ ;
(4)比较D、E最高价氧化物的水化物的酸性大小关系_____________________ ; (用化学式表示)
(5)单质E与水反应的离子方程式为_________________________ ;
(6)C最高价氧化物对应水化物与E最高价氧化物对应水化物反应的离子方程式____________ 。
(1)五种元素中,原子半径最大的是
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是
(3)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为
(4)比较D、E最高价氧化物的水化物的酸性大小关系
(5)单质E与水反应的离子方程式为
(6)C最高价氧化物对应水化物与E最高价氧化物对应水化物反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下表为九种主族元素在周期表中的位置:
请回答下列问题:
(1)I元素的位置是第________ 周期,第______ 族。
(2)C、B、D 三种元素的金属性由强到弱的顺序为_______ (填元素符号)。
(3)E、F两种元素对应的最简单氢化物的稳定性:________________ (填化学式)。
(4)C的单质与水反应的离子方程式为_______ 。
(5)用电子式表示A和G形成化合物的过程:____ 。
| A | |||||||
| E | F | ||||||
| B | D | I | G | ||||
| C | H | ||||||
请回答下列问题:
(1)I元素的位置是第
(2)C、B、D 三种元素的金属性由强到弱的顺序为
(3)E、F两种元素对应的最简单氢化物的稳定性:
(4)C的单质与水反应的离子方程式为
(5)用电子式表示A和G形成化合物的过程:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某小组探究卤素参与的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
(1)浓盐酸与MnO2混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和MnO2。
①反应的离子方程式是__ 。
②电极反应式:i.还原反应:MnO2+2e-+4H+=Mn2++2H2O;ii.氧化反应:__ 。
③根据电极反应式,分析A中仍存在盐酸和MnO2的原因。
i.随c(H+)降低或c(Mn2+)浓度升高,MnO2氧化性减弱。ii.随c(Cl-)降低,__ 。
④补充实验证实了③中的分析。
a是__ ,b是__ 。
(2)利用c(H+)浓度对MnO2氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能与MnO2反应所需的最低c(H+)最小的是__ ,从原子结构角度说明理由__ 。
(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高Br2的氧化性,将Mn2+氧化为MnO2。经实验证实了推测,该化合物是__ 。
(4)总结:物质氧化性和还原性随反应物和生成物浓度变化的一般规律是:氧化剂(还原剂)的浓度越大,其氧化性(还原性)越___ (选填“强”或“弱”,下同),还原产物(氧化产物)的浓度越大,对应的氧化剂(还原剂)的氧化性(还原性)越___ 。
(1)浓盐酸与MnO2混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和MnO2。
①反应的离子方程式是
②电极反应式:i.还原反应:MnO2+2e-+4H+=Mn2++2H2O;ii.氧化反应:
③根据电极反应式,分析A中仍存在盐酸和MnO2的原因。
i.随c(H+)降低或c(Mn2+)浓度升高,MnO2氧化性减弱。ii.随c(Cl-)降低,
④补充实验证实了③中的分析。
| 实验操作 | 试剂 | 产物检测 | |
| I | 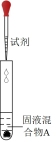 | 较浓H2SO4 | 有Cl2 |
| II | a | 有Cl2 | |
| III | a+b | 无Cl2 |
(2)利用c(H+)浓度对MnO2氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能与MnO2反应所需的最低c(H+)最小的是
(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高Br2的氧化性,将Mn2+氧化为MnO2。经实验证实了推测,该化合物是
(4)总结:物质氧化性和还原性随反应物和生成物浓度变化的一般规律是:氧化剂(还原剂)的浓度越大,其氧化性(还原性)越
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】有四种短周期元素,相关信息如下表。
请根据表中信息回答:
(1)A在周期表中位于第_______ 周期第_______ 族。
(2)用电子式表示B与C形成化合物的过程:_______ 。
(3)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是_______ (填化学式)。
(4)已知硒(Se)与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是_______ 。
a.其单质在常温下呈固态
b. 既有氧化性又有还原性
既有氧化性又有还原性
c.最高价氧化物对应的水化物的化学式为
d.非金属性比Cl元素的强
| 元素 | 相关信息 |
| A | 气态氢化物极易溶于水,且其水溶液显碱性 |
| B | 单质在焰色试验中显黄色 |
| C | 单质是淡黄绿色气体,可用于自来水消毒 |
| D | -2价阴离子的电子层结构与Ar原子相同 |
(1)A在周期表中位于第
(2)用电子式表示B与C形成化合物的过程:
(3)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是
(4)已知硒(Se)与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是
a.其单质在常温下呈固态
b.
 既有氧化性又有还原性
既有氧化性又有还原性c.最高价氧化物对应的水化物的化学式为

d.非金属性比Cl元素的强
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】微型实验具有设计简单、节约药品等优点。某化学活动小组利用所学知识设计氯气的制备和性质检验实验回答下列问题:
(1)若实验室用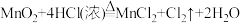 制取少量氯气,则反应的最佳装置是
制取少量氯气,则反应的最佳装置是___________ (填标号)。

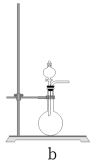

(2)利用如图装置收集纯净的氯气,其链节顺序为发生装置→___________ (按气流方向,用字母表示)。
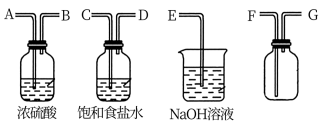
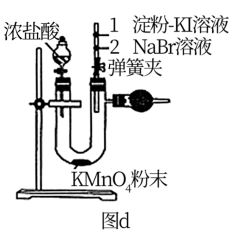
(3)通过图d装置(1,2两处为蘸有溶液的棉球)可检验卤素单质的氧化性强弱,干燥管中装的试剂为碱石灰其作用为___________ ;2处反应的离子方程式为___________ 。
(4)仔细观察图d,欲利用该装置证明溴单质的氧化性大于碘单质的。其操作为打开2下方的弹簧夹,使氯气缓慢上升到2的位置,待观察到___________ 立即夹住弹簧夹,不使氯气上升。然后取下上节玻璃管在2处微微加热即看到红棕色的物质扩散到1处,此时___________ ,则证明氧化性Br2>I2.反应的化学方程式为___________ 。
(1)若实验室用
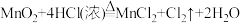 制取少量氯气,则反应的最佳装置是
制取少量氯气,则反应的最佳装置是


(2)利用如图装置收集纯净的氯气,其链节顺序为发生装置→

(3)通过图d装置(1,2两处为蘸有溶液的棉球)可检验卤素单质的氧化性强弱,干燥管中装的试剂为碱石灰其作用为
(4)仔细观察图d,欲利用该装置证明溴单质的氧化性大于碘单质的。其操作为打开2下方的弹簧夹,使氯气缓慢上升到2的位置,待观察到

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】联合国大会将2019年定为“化学元素周期表国际年”,高度体现了元素周期表的重要性。部分元素在周期表中的位置如图:
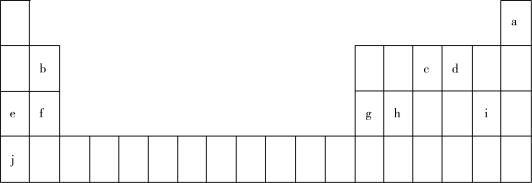
(1)2021年2月22日,嫦娥五号采样返回器带回的月壤公开亮相,对月壤中化学元素的分析有助于认识月球表面环境。
①月壤中含有较丰富的质量数为3的a,它可以作为未来核聚变的重要原料之一,a的这种核素表示为_______ 。
②经分析,月壤中含有大量的元素d和h,原子半径d_______ h(填“>”、“<”或“=”),元素h在周期表中的位置为_______ 。
(2)e和f的单质都是化学家戴维通过电解的方法首次制得。e的单质与水反应的化学方程式为_______ ,用电子式表示f原子与i原子形成化合物的形成过程:_______ 。
(3)d和i两种元素的简单氢化物中,熔沸点较高的氢化物的电子式为_______ 。
(4)《天工开物》记载,“凡火药,以硝石、硫磺为主,草木灰为辅”,由c、d、j三种元素组成的化合物是硝石的主要成分,化学式为_______ 。实验室按照如图操作配制该溶液,所得溶液浓度_______ (填“偏大”或“偏小”)。
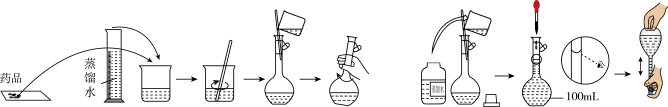
(5)元素b与g的性质相似,可以预测b与g的单质或化合物也可能具有相似的性质。请写出b的最高价氧化物对应水化物与e的最高价氧化物对应水化物反应的化学方程式_______ 。

(1)2021年2月22日,嫦娥五号采样返回器带回的月壤公开亮相,对月壤中化学元素的分析有助于认识月球表面环境。
①月壤中含有较丰富的质量数为3的a,它可以作为未来核聚变的重要原料之一,a的这种核素表示为
②经分析,月壤中含有大量的元素d和h,原子半径d
(2)e和f的单质都是化学家戴维通过电解的方法首次制得。e的单质与水反应的化学方程式为
(3)d和i两种元素的简单氢化物中,熔沸点较高的氢化物的电子式为
(4)《天工开物》记载,“凡火药,以硝石、硫磺为主,草木灰为辅”,由c、d、j三种元素组成的化合物是硝石的主要成分,化学式为

(5)元素b与g的性质相似,可以预测b与g的单质或化合物也可能具有相似的性质。请写出b的最高价氧化物对应水化物与e的最高价氧化物对应水化物反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】 、
、 、
、 、
、 、
、 为原子序数依次增大的短周期主族元素,分别位于三个周期。
为原子序数依次增大的短周期主族元素,分别位于三个周期。 元素原子的最外层电子数是次外层的三倍,
元素原子的最外层电子数是次外层的三倍, 元素与
元素与 、
、 元素均能形成两种常见的二元化合物,其中与
元素均能形成两种常见的二元化合物,其中与 形成的化合物分别为
形成的化合物分别为 和
和 ,
, 可以用来杀菌消毒:
可以用来杀菌消毒: 、
、 、
、 元素原子的最外层电子数之和为
元素原子的最外层电子数之和为 元素原子所含质子数的一半。据此回答下列问题。
元素原子所含质子数的一半。据此回答下列问题。
(1)画出 元素简单离子的离子结构示意图
元素简单离子的离子结构示意图___________ ,元素 在周期表中的位置为
在周期表中的位置为___________ 。
(2) 分子的空间结构为
分子的空间结构为___________ , 的电子式为
的电子式为___________ , 与
与 所形成的简单化合物中含有的化学键类型为
所形成的简单化合物中含有的化学键类型为___________ 。
(3)请写出 的最高价氧化物对应水化物与
的最高价氧化物对应水化物与 的最高价氧化物对应水化物反应的离子方程式
的最高价氧化物对应水化物反应的离子方程式___________ 。
(4) 的单质与
的单质与 的单质能反应生成一种气体,将集满该气体的试管倒立于水槽中,产生的现象是
的单质能反应生成一种气体,将集满该气体的试管倒立于水槽中,产生的现象是___________ 。
a.试管中液面略有上升 b.液体几乎充满试管
c.液面升至距管口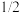 处 d.无现显现象
处 d.无现显现象
(5) 与
与 组成的
组成的 电子带电微粒不能在强碱性溶液中大量共存,请写出反应的离子方程式
电子带电微粒不能在强碱性溶液中大量共存,请写出反应的离子方程式___________ 。
 、
、 、
、 、
、 、
、 为原子序数依次增大的短周期主族元素,分别位于三个周期。
为原子序数依次增大的短周期主族元素,分别位于三个周期。 元素原子的最外层电子数是次外层的三倍,
元素原子的最外层电子数是次外层的三倍, 元素与
元素与 、
、 元素均能形成两种常见的二元化合物,其中与
元素均能形成两种常见的二元化合物,其中与 形成的化合物分别为
形成的化合物分别为 和
和 ,
, 可以用来杀菌消毒:
可以用来杀菌消毒: 、
、 、
、 元素原子的最外层电子数之和为
元素原子的最外层电子数之和为 元素原子所含质子数的一半。据此回答下列问题。
元素原子所含质子数的一半。据此回答下列问题。(1)画出
 元素简单离子的离子结构示意图
元素简单离子的离子结构示意图 在周期表中的位置为
在周期表中的位置为(2)
 分子的空间结构为
分子的空间结构为 的电子式为
的电子式为 与
与 所形成的简单化合物中含有的化学键类型为
所形成的简单化合物中含有的化学键类型为(3)请写出
 的最高价氧化物对应水化物与
的最高价氧化物对应水化物与 的最高价氧化物对应水化物反应的离子方程式
的最高价氧化物对应水化物反应的离子方程式(4)
 的单质与
的单质与 的单质能反应生成一种气体,将集满该气体的试管倒立于水槽中,产生的现象是
的单质能反应生成一种气体,将集满该气体的试管倒立于水槽中,产生的现象是a.试管中液面略有上升 b.液体几乎充满试管
c.液面升至距管口
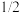 处 d.无现显现象
处 d.无现显现象(5)
 与
与 组成的
组成的 电子带电微粒不能在强碱性溶液中大量共存,请写出反应的离子方程式
电子带电微粒不能在强碱性溶液中大量共存,请写出反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下表列出了①~⑩十种元素,回答下列问题:
(1)①、④按原子个数比1:1组成的分子的电子式为____ ;由②、④两种元素组成的一种无毒化合物的结构式为_______
(2)这10种元素中,化学性质最不活泼的元素是________ (填元素符号,下同),得电子能力最强的原子是_________ 失电子能力最强的单质与水反应的化学方程式是___________
(3)用化学方程式表示②和⑨两种元素的非金属性强弱:_________
(4)元素③的气态氢化物和元素⑧的气态氢化物中,易于制备的是______ (填化学式)
(5)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应,其离子方程式为____________
(6)元素①、④、⑤两两之间可以形成两种类型的化合物,写出一种共价化合物的化学式:_________ ;写出一种离子化合物的化学式:___________
(7)写出⑥的单质置换出②的单质的化学方程式:__________________
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ④ | ⑩ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ③ | ⑧ | ⑨ |
(2)这10种元素中,化学性质最不活泼的元素是
(3)用化学方程式表示②和⑨两种元素的非金属性强弱:
(4)元素③的气态氢化物和元素⑧的气态氢化物中,易于制备的是
(5)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应,其离子方程式为
(6)元素①、④、⑤两两之间可以形成两种类型的化合物,写出一种共价化合物的化学式:
(7)写出⑥的单质置换出②的单质的化学方程式:
您最近一年使用:0次



