I.写出下列热化学反应方程式
(1)N2 (g)与H2(g)反应生成1molNH3(g),放出46.1kJ热量。_______
(2)1molC2H5OH(l)完全燃烧生成CO2(g)和H2O(l),放出1366.8kJ热量。_______
(3)1molC(石墨)与适量H2O(g)反应吸收131.3kJ热量________
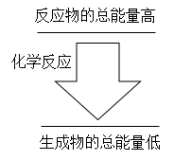
II.(1)化学反应中均伴随着能量的变化,化学键的断裂和形成是发生能量变化的主要原因。生成物中化学键形成时会______ 能量(填“放出”或“吸收”);如果一个化学反应,化学键断裂时的能量变化大于化学键形成时的能量变化,则该反应属于______ 反应;如果一个化学反应,反应物的总能量和生成物的总能量有如图所示的关系,则该反应属于_______ 反应。
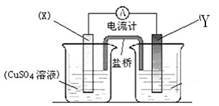
(2)不同形式的能量可以相互转换,如:化学能和电能、热能之间的相互转换。如图是一个原电池工作原理的示意图。试回答:
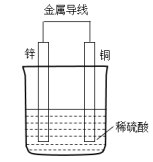
①从能量角度看,它属于________ 能转化为________ 能;
②装置中Zn为________ 极。
(1)N2 (g)与H2(g)反应生成1molNH3(g),放出46.1kJ热量。
(2)1molC2H5OH(l)完全燃烧生成CO2(g)和H2O(l),放出1366.8kJ热量。
(3)1molC(石墨)与适量H2O(g)反应吸收131.3kJ热量
II.(1)化学反应中均伴随着能量的变化,化学键的断裂和形成是发生能量变化的主要原因。生成物中化学键形成时会

(2)不同形式的能量可以相互转换,如:化学能和电能、热能之间的相互转换。如图是一个原电池工作原理的示意图。试回答:

①从能量角度看,它属于
②装置中Zn为
11-12高二上·山东·期中 查看更多[2]
更新时间:2016-12-08 18:27:29
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是___________ 。
(2)已知:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
CO(g)+ O2(g)=CO2(g) ΔH=-283 kJ·mol-1
O2(g)=CO2(g) ΔH=-283 kJ·mol-1
某H2和CO的混合气体完全燃烧时放出113.76 kJ热量,同时生成3.6 g液态水,则原混合气体中H2和CO的物质的量分别为___________ 。
(1)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是
(2)已知:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
CO(g)+
 O2(g)=CO2(g) ΔH=-283 kJ·mol-1
O2(g)=CO2(g) ΔH=-283 kJ·mol-1某H2和CO的混合气体完全燃烧时放出113.76 kJ热量,同时生成3.6 g液态水,则原混合气体中H2和CO的物质的量分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)实验测得,1g乙醇在氧气中充分燃烧生成二氧化碳和液态水释放出29.7kJ的热量,试写出乙醇燃烧的热化学方程式:___________ 。
(2)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行理论推算。试依据下列热化学方程式,计算反应 的焓变为
的焓变为___________ 。
①

②

③

(3)某实验小组用0.5mol/L NaOH溶液和0.5mol/L硫酸溶液进行中和热的测定。
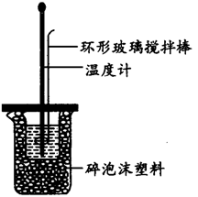
①环形玻璃搅拌棒___________ (填“能”或“不能”)改为环形金属(如铜)棒,其原因是___________ 。
②碎泡沫的作用是___________ 。
③测定稀硫酸和稀氢氧化钠中和热的实验装置如上图所示。取50mL NaOH溶液和30mL硫酸溶液进行实验,三次测定温度差的平均值为4.0℃,若近似认为0.5mol/L NaOH溶液和0.5mol/L硫酸溶液的密度都是1 ,中和后生成溶液的比热容
,中和后生成溶液的比热容 。则中和热
。则中和热
___________ (取小数点后一位)。
④上述实验数值结果与57.3 有偏差,产生偏差的原因可能是
有偏差,产生偏差的原因可能是___________ (填字母)。
a.反应时未用搅拌器搅拌
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
(1)实验测得,1g乙醇在氧气中充分燃烧生成二氧化碳和液态水释放出29.7kJ的热量,试写出乙醇燃烧的热化学方程式:
(2)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行理论推算。试依据下列热化学方程式,计算反应
 的焓变为
的焓变为①


②


③


(3)某实验小组用0.5mol/L NaOH溶液和0.5mol/L硫酸溶液进行中和热的测定。

①环形玻璃搅拌棒
②碎泡沫的作用是
③测定稀硫酸和稀氢氧化钠中和热的实验装置如上图所示。取50mL NaOH溶液和30mL硫酸溶液进行实验,三次测定温度差的平均值为4.0℃,若近似认为0.5mol/L NaOH溶液和0.5mol/L硫酸溶液的密度都是1
 ,中和后生成溶液的比热容
,中和后生成溶液的比热容 。则中和热
。则中和热
④上述实验数值结果与57.3
 有偏差,产生偏差的原因可能是
有偏差,产生偏差的原因可能是a.反应时未用搅拌器搅拌
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学在能源开发与利用中起着十分关键的作用。
(1)蕴藏在海底的“可燃冰”是高压下形成的外观像冰的甲烷水合物固体。甲烷气体氧化和水汽化的热化学方程式分别为:①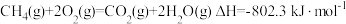 ,②
,②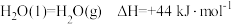 。则
。则 “可燃冰”(分子式为
“可燃冰”(分子式为 )释放的甲烷气体完全氧化生成二氧化碳气体和液态水时放出的热量为
)释放的甲烷气体完全氧化生成二氧化碳气体和液态水时放出的热量为_______ 。
(2) 的气态高能燃料乙硼烷(
的气态高能燃料乙硼烷( )在氧气中氧化生成固态三氧化二硼和液态水时放出
)在氧气中氧化生成固态三氧化二硼和液态水时放出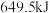 热量,其热化学方程式为
热量,其热化学方程式为_______ 。
(3)家用液化气的主要成分之一是丁烷( )。常温常压条件下,
)。常温常压条件下, 丁烷完全氧化生成
丁烷完全氧化生成 气体和液态水时放出热量
气体和液态水时放出热量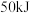 ,则表示丁烷摩尔燃烧焓的热化学方程式为
,则表示丁烷摩尔燃烧焓的热化学方程式为_______ 。
(4)下列制氢气方法中最节能的是_______(填序号)。
(5)已知:2Al(s)+3∕2O2(g)=Al2O3(s) △H=-1644.3kJ•mol-1
2Fe(s)+ O2(g)=Fe2O3(s) △H=-815.88kJ•mol-1
O2(g)=Fe2O3(s) △H=-815.88kJ•mol-1
试写出铝粉与氧化铁粉末发生铝热反应的热化学方程式_______ 。
(1)蕴藏在海底的“可燃冰”是高压下形成的外观像冰的甲烷水合物固体。甲烷气体氧化和水汽化的热化学方程式分别为:①
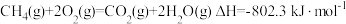 ,②
,②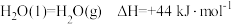 。则
。则 “可燃冰”(分子式为
“可燃冰”(分子式为 )释放的甲烷气体完全氧化生成二氧化碳气体和液态水时放出的热量为
)释放的甲烷气体完全氧化生成二氧化碳气体和液态水时放出的热量为(2)
 的气态高能燃料乙硼烷(
的气态高能燃料乙硼烷( )在氧气中氧化生成固态三氧化二硼和液态水时放出
)在氧气中氧化生成固态三氧化二硼和液态水时放出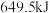 热量,其热化学方程式为
热量,其热化学方程式为(3)家用液化气的主要成分之一是丁烷(
 )。常温常压条件下,
)。常温常压条件下, 丁烷完全氧化生成
丁烷完全氧化生成 气体和液态水时放出热量
气体和液态水时放出热量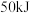 ,则表示丁烷摩尔燃烧焓的热化学方程式为
,则表示丁烷摩尔燃烧焓的热化学方程式为(4)下列制氢气方法中最节能的是_______(填序号)。
A.电解水制氢气: |
B.高温使水分解制氢气: |
C.太阳光催化分解水制氢气: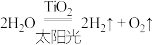 |
D.天然气制氢气: |
2Fe(s)+
 O2(g)=Fe2O3(s) △H=-815.88kJ•mol-1
O2(g)=Fe2O3(s) △H=-815.88kJ•mol-1试写出铝粉与氧化铁粉末发生铝热反应的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)某反应A(g)+B(g)= C(g)+D(g)过程中的能量变化如图所示,回答问题。
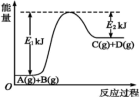
①该反应是_______ (填“吸热”或“放热”)反应,反应的ΔH=_______ kJ· mol-1(用含E1、E2的代数式表示)。
②该反应过程中,断裂旧化学键吸收的总能量_______ (填“>”“ <”或“=”)形成新化学键释放的总能量。
(2)已知:①C4H10(g)+ O2(g)= C4H8(g)+H2O(g) ΔH1=-119 kJ·mol-1
O2(g)= C4H8(g)+H2O(g) ΔH1=-119 kJ·mol-1
② H2(g)+ O2(g) = H2O(g) ΔH2=-242 kJ·mol-1
O2(g) = H2O(g) ΔH2=-242 kJ·mol-1
则:C4H10(g)= C4H8(g)+H2(g) ΔH3=_______ kJ·mol-1。
(3)已知拆开1 mol H-Cl键、1 mol H-H键、1 mol Cl-Cl键分别需要的能量是431 kJ、436 kJ、243 kJ,则2 mol HCl气体分解生成1molCl2与1 molH2的热化学方程式为_______ 。
(4)已知:101 kPa时,C(s)+O2(g)═CO(g) ΔH=﹣110.5kJ/mol,则碳的燃烧热数值_______ 110.5 kJ/mol(填>,<,=)。
(1)某反应A(g)+B(g)= C(g)+D(g)过程中的能量变化如图所示,回答问题。

①该反应是
②该反应过程中,断裂旧化学键吸收的总能量
(2)已知:①C4H10(g)+
 O2(g)= C4H8(g)+H2O(g) ΔH1=-119 kJ·mol-1
O2(g)= C4H8(g)+H2O(g) ΔH1=-119 kJ·mol-1 ② H2(g)+
 O2(g) = H2O(g) ΔH2=-242 kJ·mol-1
O2(g) = H2O(g) ΔH2=-242 kJ·mol-1则:C4H10(g)= C4H8(g)+H2(g) ΔH3=
(3)已知拆开1 mol H-Cl键、1 mol H-H键、1 mol Cl-Cl键分别需要的能量是431 kJ、436 kJ、243 kJ,则2 mol HCl气体分解生成1molCl2与1 molH2的热化学方程式为
(4)已知:101 kPa时,C(s)+O2(g)═CO(g) ΔH=﹣110.5kJ/mol,则碳的燃烧热数值
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知化学反应N2+3H2 NH3的能量变化如图所示:
NH3的能量变化如图所示:
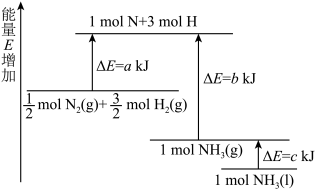
(1)1 mol N和3 mol H生成 1 mol NH3(g)是________ 能量的过程(填“吸收”或“释放”)。
(2)由 mol N2(g)和
mol N2(g)和 mol N2(g)生成1 mol NH3(g)过程
mol N2(g)生成1 mol NH3(g)过程________ (填“吸收”或“释放”)________ kJ能量。
 NH3的能量变化如图所示:
NH3的能量变化如图所示:
(1)1 mol N和3 mol H生成 1 mol NH3(g)是
(2)由
 mol N2(g)和
mol N2(g)和 mol N2(g)生成1 mol NH3(g)过程
mol N2(g)生成1 mol NH3(g)过程
您最近一年使用:0次
【推荐3】(1)下列各组物质:①O2和O3;②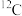
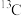
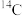 ;③H2O、D2O、T2O;④C16H34和(CH3)2CHCH2CH3;⑤CH3(CH2)3CH3和
;③H2O、D2O、T2O;④C16H34和(CH3)2CHCH2CH3;⑤CH3(CH2)3CH3和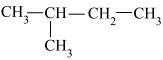 ;⑥2-甲基丁烷、异戊烷。
;⑥2-甲基丁烷、异戊烷。
其中互为同位素的是_______ ;互为同素异形体的是_______ ;互为同系物的是_______ ;互为同分异构体的是_______ ;属于同种物质的是_______ 。(用序号填空,下同)
(2)为了研究化学反应A+B===C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:
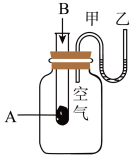
①该反应为______ 反应(填“放热”或“吸热”)。
②A和B的总能量比C和D的总能量___ (填“高”或“低”)。
③物质中的化学能通过______ 转化成______ 释放出来。
④反应物化学键断裂吸收的能量________ (填“高”或“低”)于生成物化学键形成放出的能量。
⑤写出一个符合题中条件的化学方程式 :___________ 。
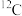
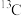
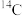 ;③H2O、D2O、T2O;④C16H34和(CH3)2CHCH2CH3;⑤CH3(CH2)3CH3和
;③H2O、D2O、T2O;④C16H34和(CH3)2CHCH2CH3;⑤CH3(CH2)3CH3和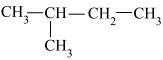 ;⑥2-甲基丁烷、异戊烷。
;⑥2-甲基丁烷、异戊烷。其中互为同位素的是
(2)为了研究化学反应A+B===C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:

①该反应为
②A和B的总能量比C和D的总能量
③物质中的化学能通过
④反应物化学键断裂吸收的能量
⑤写出一个符合题中条件的
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)下列反应中,属于放热反应的是_____________ ,属于吸热反应的是___________ .
①煅烧石灰石 ②木炭燃烧 ③炸药爆炸 ④酸碱中和 ⑤生石灰与水作用制熟石灰 ⑥食物因氧化而腐败
(2)用铜、银与硝酸银设计一个原电池,此电池的负极是__________ ,负极的电极反应式是_________ .
(3)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片的质量减少了3.25g,铜表面析出了氢气________ L(标准状况),导线中通过______ mol电子.
(4)某化学反应,设反应物的总能量为E1,生成物的总能量为E2,若E1>E2,则该反应为___________ 热反应,该反应过程可以看成________________ .
中和反应都是___________ 热反应,其实质是___________ (用化学语言填空)
①煅烧石灰石 ②木炭燃烧 ③炸药爆炸 ④酸碱中和 ⑤生石灰与水作用制熟石灰 ⑥食物因氧化而腐败
(2)用铜、银与硝酸银设计一个原电池,此电池的负极是
(3)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片的质量减少了3.25g,铜表面析出了氢气
(4)某化学反应,设反应物的总能量为E1,生成物的总能量为E2,若E1>E2,则该反应为
中和反应都是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】钠及其化合物具有独特的性质和广泛的用途。
I.
(1)下图为钠与水反应的实验示意图。
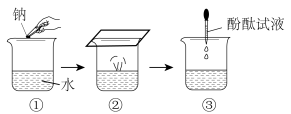
i.②中现象说明钠的密度比水___________ (“大”或“小”)。
ii.实验中观察到钠融成小球,下列能量变化示意图中能解释该现象的是___________ 。
a.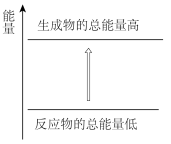 B.
B.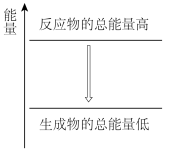
iii.③中加入酚酞试液后的现象是___________ 。
(2)用化学方程式表示由氯化钠制取金属钠的原理。___________
(3)将一定量的 通入
通入 溶液中。所得溶液转移至Y形管的一侧,并放入小磁子;向Y形管另一侧支管中加入
溶液中。所得溶液转移至Y形管的一侧,并放入小磁子;向Y形管另一侧支管中加入 盐酸,Y形管上端连接压强传感器。将Y形管倾斜,使两支管中的溶液混合,启动磁力搅拌器,采集压强数据。当数据变化平缓时,停止采集数据,得到如图所示的实验结果:
盐酸,Y形管上端连接压强传感器。将Y形管倾斜,使两支管中的溶液混合,启动磁力搅拌器,采集压强数据。当数据变化平缓时,停止采集数据,得到如图所示的实验结果:
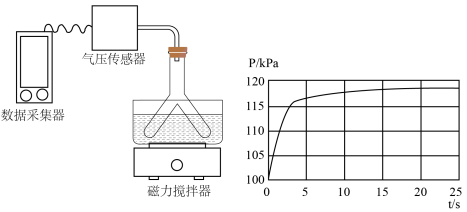
其中0~5s发生反应的离子方程式为___________ 。20s时溶液中的溶质是___________ (不考虑气体在水中的溶解)。
II.过碳酸钠( ),俗名固态双氧水,具有去污杀菌等功效。其制备原理为:
),俗名固态双氧水,具有去污杀菌等功效。其制备原理为: (反应放热)
(反应放热)
(4)结合 和
和 的性质,推测制备过碳酸钠的原料中,
的性质,推测制备过碳酸钠的原料中, 与
与 的物质的量之比应
的物质的量之比应___________  。
。
A.大于 B.等于 C.小于
向 中加入
中加入 溶液的速度不能过快,原因是
溶液的速度不能过快,原因是___________ 。
(5)在过碳酸钠的生产过程中需要加入稳定剂,以得到稳定性好的过碳酸钠产品,保证其在一定贮存期内仍具有高活性的氧含量。以不同种类的稳定剂制备过碳酸钠产品,测得其活性氧质量分数随时间的变化如图所示:
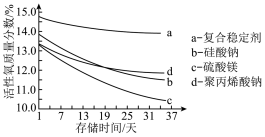
由图可知,制备过碳酸钠时应选择的稳定剂是___________ ,理由是___________ 。
A.a B.b C.c D.d
I.
(1)下图为钠与水反应的实验示意图。

i.②中现象说明钠的密度比水
ii.实验中观察到钠融成小球,下列能量变化示意图中能解释该现象的是
a.
 B.
B.
iii.③中加入酚酞试液后的现象是
(2)用化学方程式表示由氯化钠制取金属钠的原理。
(3)将一定量的
 通入
通入 溶液中。所得溶液转移至Y形管的一侧,并放入小磁子;向Y形管另一侧支管中加入
溶液中。所得溶液转移至Y形管的一侧,并放入小磁子;向Y形管另一侧支管中加入 盐酸,Y形管上端连接压强传感器。将Y形管倾斜,使两支管中的溶液混合,启动磁力搅拌器,采集压强数据。当数据变化平缓时,停止采集数据,得到如图所示的实验结果:
盐酸,Y形管上端连接压强传感器。将Y形管倾斜,使两支管中的溶液混合,启动磁力搅拌器,采集压强数据。当数据变化平缓时,停止采集数据,得到如图所示的实验结果:
其中0~5s发生反应的离子方程式为
II.过碳酸钠(
 ),俗名固态双氧水,具有去污杀菌等功效。其制备原理为:
),俗名固态双氧水,具有去污杀菌等功效。其制备原理为: (反应放热)
(反应放热)(4)结合
 和
和 的性质,推测制备过碳酸钠的原料中,
的性质,推测制备过碳酸钠的原料中, 与
与 的物质的量之比应
的物质的量之比应 。
。A.大于 B.等于 C.小于
向
 中加入
中加入 溶液的速度不能过快,原因是
溶液的速度不能过快,原因是(5)在过碳酸钠的生产过程中需要加入稳定剂,以得到稳定性好的过碳酸钠产品,保证其在一定贮存期内仍具有高活性的氧含量。以不同种类的稳定剂制备过碳酸钠产品,测得其活性氧质量分数随时间的变化如图所示:

由图可知,制备过碳酸钠时应选择的稳定剂是
A.a B.b C.c D.d
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)以下反应:①木炭与水制备水煤气,②氯酸钾分解,③炸药爆炸,④酸与碱的中和反应,⑤生石灰与水作用制熟石灰,⑥Ba(OH)2•H2O 与 NH4Cl ,⑦浓硫酸溶于水, 属于放热反应__________ .(填序号)
(2)Mg-Al-NaOH 电池中的负极反应:___________ .
(3)FeCl3 溶液常用于腐蚀印刷电路铜板,发生 2FeCl3+Cu=2FeCl2+CuCl2,若将 此反应设计成原电池,则负极所用电极材料为___________ ,当线路中转移 0.2mol 电 子时,则被腐蚀铜的质量为___________ g.
(4)已知拆开 1mol H-H 键、1mol N≡N、1mol N-H 键分别需要吸收的能量为 436kJ、946k J、391k J.则由 N2 和 H2 反应生成 1mol NH3 需要放出___________ 的热量。
(5)用序号回答:①HCl ②NaOH ③Cl2 ④H2O ⑤NH4Cl ⑥P4 ⑦NH3•H2O ⑧Na2O2 ⑨HClO⑩CaO⑪HF⑫MgCl2
属于共价化合物的是___________ ,存在非极性键的是___________ 。
(2)Mg-Al-NaOH 电池中的负极反应:
(3)FeCl3 溶液常用于腐蚀印刷电路铜板,发生 2FeCl3+Cu=2FeCl2+CuCl2,若将 此反应设计成原电池,则负极所用电极材料为
(4)已知拆开 1mol H-H 键、1mol N≡N、1mol N-H 键分别需要吸收的能量为 436kJ、946k J、391k J.则由 N2 和 H2 反应生成 1mol NH3 需要放出
(5)用序号回答:①HCl ②NaOH ③Cl2 ④H2O ⑤NH4Cl ⑥P4 ⑦NH3•H2O ⑧Na2O2 ⑨HClO⑩CaO⑪HF⑫MgCl2
属于共价化合物的是
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
名校
【推荐1】金属冶炼和处理常涉及氧化还原反应。
(1)由下列物质冶炼相应金属时采用电解法的是_________ 。
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)辉铜矿(Cu2S)可发生反应2Cu2S+2H2SO4+5O2=4CuSO4+2H2O,该反应的还原剂是________ ,当1mol O2发生反应时,还原剂所失电子的物质的量为___ mol;向CuSO4溶液中加入镁条时有气体生成,该气体是_________ 。
(3)下图为电解精炼银的示意图,______ (填“a”或“b”)极为含有杂质的粗银,若b极 有少量红棕色气体产生,则生成该气体的电极反应式为________________ 。
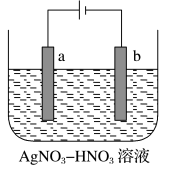
(4)为处理银器表面的黑斑(Ag2S),将银器置于铝制容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为____________________________________ 。
(1)由下列物质冶炼相应金属时采用电解法的是
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)辉铜矿(Cu2S)可发生反应2Cu2S+2H2SO4+5O2=4CuSO4+2H2O,该反应的还原剂是
(3)下图为电解精炼银的示意图,

(4)为处理银器表面的黑斑(Ag2S),将银器置于铝制容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】电解原理和原电池原理是电化学的两个重要内容。某兴趣小组做如下探究实验:
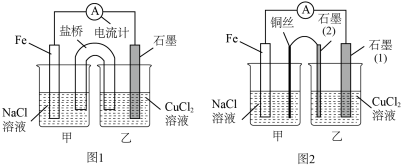
(1)如上图 1 为某实验小组依据氧化还原反应设计的原电池装置,若盐桥中装有饱和的 KNO3溶液和琼胶制成的胶冻,则 NO 移向
移向_____ 装置(填写“甲或乙”)。其他条件不变,若将 CuCl2溶液换为 NH4Cl溶液,发现生成无色无味的单质气体,则石墨上电极反应式_____ 。
(2)如图 2,其他条件不变,若将盐桥换成弯铜导线与石墨相连成 n 型,则甲装置是_____ (填 “原电池或电解池”),乙装置中石墨(2)为_____ 极,乙装置中与铁线相连的石墨(1)电极上发生的反应式为_____ ,甲装置中铜丝电极反应式为_____ 。
(3)在图 2 乙装置中改为加入 CuSO4溶液,一段时间后,若某一电极质量增重 1.28 g,则另一电极生成________ mL(标况下)气体。

(1)如上图 1 为某实验小组依据氧化还原反应设计的原电池装置,若盐桥中装有饱和的 KNO3溶液和琼胶制成的胶冻,则 NO
 移向
移向(2)如图 2,其他条件不变,若将盐桥换成弯铜导线与石墨相连成 n 型,则甲装置是
(3)在图 2 乙装置中改为加入 CuSO4溶液,一段时间后,若某一电极质量增重 1.28 g,则另一电极生成
您最近一年使用:0次