根据所学知识回答下列有关问题。
(1)下列说法正确的是________ (填序号)。
A 漂白粉久置在空气中容易失效的原因是Ca(ClO)2不稳定、易分解
B 次氯酸和过氧化钠都有漂白作用,但漂白原理不同
C Ca(ClO)2中含有氯离子
D 漂白粉与84消毒液的消毒原理相同
(2)工业上将氯气通入石灰乳[主要成分为Ca(OH)2]制取漂白粉,反应的化学方程式为___________________________________________________________ ;
湿润的Cl2也具有漂白性,但人们常将Cl2制成漂白粉使用,其主要目的是____________________________________________________________ 。
(3)漂白粉与空气中的CO2和H2O作用,即可产生具有漂白、杀菌作用的次氯酸,反应的化学方程式为______________________________________________________________ 。
(1)下列说法正确的是
A 漂白粉久置在空气中容易失效的原因是Ca(ClO)2不稳定、易分解
B 次氯酸和过氧化钠都有漂白作用,但漂白原理不同
C Ca(ClO)2中含有氯离子
D 漂白粉与84消毒液的消毒原理相同
(2)工业上将氯气通入石灰乳[主要成分为Ca(OH)2]制取漂白粉,反应的化学方程式为
湿润的Cl2也具有漂白性,但人们常将Cl2制成漂白粉使用,其主要目的是
(3)漂白粉与空气中的CO2和H2O作用,即可产生具有漂白、杀菌作用的次氯酸,反应的化学方程式为
19-20高一·全国·课时练习 查看更多[3]
鲁科版(2019)新教材化学同步1.2.2研究物质的基本程序练习题(已下线)1.2.2研究物质的基本程序 练习(2)——《高中新教材同步备课》(鲁科版 必修第一册)鲁科版(2019)高一必修第一册第一章第2节 研究物质性质的方法和程序 课时2 研究物质性质的基本程序
更新时间:2020-09-13 14:01:19
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】利用氯元素价类二维图,可以从不同角度研究含氯物质的性质及其转化关系。回答下列问题:
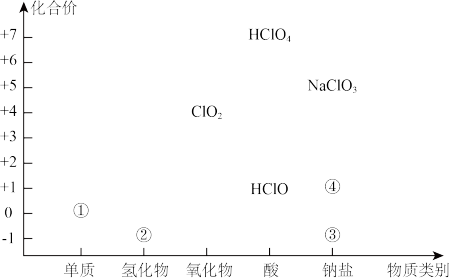
(1)②为_______ (写化学式),写出③的一种用途:_______ 。
(2)常温下,①可与NaOH溶液反应生成③和④,请写出该反应的化学方程式:_______ ,该反应也是漂白液的制备原理,漂白液的有效成分为_______ 。
(3)控制温度,①可与NaOH溶液反应生成 :
: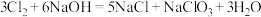 ,被氧化的氯原子与被还原的氯原子的物质的量之比为
,被氧化的氯原子与被还原的氯原子的物质的量之比为_______ 。
(4)已知 是一元强酸,则它与NaOH反应的离子方程式为
是一元强酸,则它与NaOH反应的离子方程式为_______ 。
(5)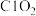 可用于自来水消毒,检验自来水中是否含有
可用于自来水消毒,检验自来水中是否含有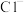 的试剂为
的试剂为_______ , 还可将水中的
还可将水中的 转化为
转化为 ,
, 再生成
再生成 胶体,说明
胶体,说明 具有
具有_______ 性,检验有胶体生成的简便方法为_______ 。

(1)②为
(2)常温下,①可与NaOH溶液反应生成③和④,请写出该反应的化学方程式:
(3)控制温度,①可与NaOH溶液反应生成
 :
: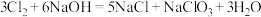 ,被氧化的氯原子与被还原的氯原子的物质的量之比为
,被氧化的氯原子与被还原的氯原子的物质的量之比为(4)已知
 是一元强酸,则它与NaOH反应的离子方程式为
是一元强酸,则它与NaOH反应的离子方程式为(5)
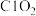 可用于自来水消毒,检验自来水中是否含有
可用于自来水消毒,检验自来水中是否含有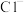 的试剂为
的试剂为 还可将水中的
还可将水中的 转化为
转化为 ,
, 再生成
再生成 胶体,说明
胶体,说明 具有
具有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】实验室制取氯气的化学方程式为MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。结合氯气的物理性质,判断下列叙述中不正确的是
MnCl2+Cl2↑+2H2O。结合氯气的物理性质,判断下列叙述中不正确的是________________ (填序号)。
①加热盛有二氧化锰、浓盐酸的烧瓶,瓶内充满黄绿色气体。
②氯气的密度比空气大,常用向上排空气法收集氯气。
③闻氯气气味时,用手轻轻在集气瓶口扇动,使极少量氯气飘进鼻孔。
④在充满氯气的集气瓶内加水,盖严后振荡,瓶内气体颜色变浅,液体变为黄绿色。
⑤氯气易液化,在低温和加压的条件下可以转变为液态(液氯)和固态。
⑥氯气、氯水、液氯是同一种物质,只是状态不同,都属于纯净物。
 MnCl2+Cl2↑+2H2O。结合氯气的物理性质,判断下列叙述中不正确的是
MnCl2+Cl2↑+2H2O。结合氯气的物理性质,判断下列叙述中不正确的是①加热盛有二氧化锰、浓盐酸的烧瓶,瓶内充满黄绿色气体。
②氯气的密度比空气大,常用向上排空气法收集氯气。
③闻氯气气味时,用手轻轻在集气瓶口扇动,使极少量氯气飘进鼻孔。
④在充满氯气的集气瓶内加水,盖严后振荡,瓶内气体颜色变浅,液体变为黄绿色。
⑤氯气易液化,在低温和加压的条件下可以转变为液态(液氯)和固态。
⑥氯气、氯水、液氯是同一种物质,只是状态不同,都属于纯净物。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】化学与人类生活密切相关。请按要求,回答下列问题:
(1)春秋末期工艺官书《考工记》中记载有“涑帛”的方法,即利用含有碳酸钠的水溶液来洗涤丝帛。请写出碳酸钠水溶液中通入CO2气体的化学方程式____ ,将54.8g Na2CO3和NaHCO3 的混合物分成等量的两份,一份溶于水后加入足量盐酸,收集到气体V L,另一份直接加热至恒重,生成气体2.24L(所有气体体积均在标准状况下测定),则原固体混合物中Na2CO3的物质的量:n(Na2CO3)=____ ,气体V=____ 。
(2)“84”消毒液在生活中使用广泛,其有效成分是次氯酸钠。可在常温下将氯气通入NaOH溶液制得,该反应的离子方程式为____ ,若有2mol氯气参与该反应,则此时转移的电子数为____ NA。
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为____ 。
(4)长石是地表岩石最重要的造岩矿物。某种长石的化学组成KAlSi3O8则将其改写成氧化物的组合形式为____ 。
(5)葡萄糖(分子式C6H12O6)是人体活细胞的能量来源。已知1mol等于1000mmol,某体检单的一些指标如图,则每升该样品中含葡萄糖的质量为____ g(请保留两位小数)。
(1)春秋末期工艺官书《考工记》中记载有“涑帛”的方法,即利用含有碳酸钠的水溶液来洗涤丝帛。请写出碳酸钠水溶液中通入CO2气体的化学方程式
(2)“84”消毒液在生活中使用广泛,其有效成分是次氯酸钠。可在常温下将氯气通入NaOH溶液制得,该反应的离子方程式为
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为
(4)长石是地表岩石最重要的造岩矿物。某种长石的化学组成KAlSi3O8则将其改写成氧化物的组合形式为
(5)葡萄糖(分子式C6H12O6)是人体活细胞的能量来源。已知1mol等于1000mmol,某体检单的一些指标如图,则每升该样品中含葡萄糖的质量为
| 9 | 白球比 | 1.6 | |
| 10 | 乳酸脱氢酶 | 161 | U/L |
| 11 | 磷酸肌酸激酶 | 56 | U/L |
| 12 | 甘油三酯 | 0.52 | mmol/L |
| 13 | 总胆固醇 | 4.27 | mmol/L |
| 14 | 高密度脂蛋白胆固醇 | 1.57 | mmol/L |
| 15 | 低密度脂蛋白胆固醇 | 1.40 | mmol/L |
| 16 | 葡萄糖 | 4.94 | mmol/L |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】漂白粉的有效成分是______ ,制取漂白粉的反应方程式为______ ,漂白粉漂白和消毒的主要原因是:_______ (文字表述),漂白粉在空气中长时间放置失效的原因是:__________ (用化学方程式表示)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】防治环境污染,改善生态环境已成为全球共识。
①2013年,全国多个省市出现严重的雾霾天气。导致雾霾形成的主要污染物是____________ (填字母);
A.O2 B.CO2 C.PM2.5
②采用焚烧处理垃圾进行发电已在江苏投入使用。下列是生活中的常见垃圾.
A.废电池 B.易拉罐 C.玻璃瓶
在焚烧处理前,除废电池外,还有__________ (填字母)应剔除并回收。
③漂白粉可用于生活用水的杀菌消毒,工业上利用氯气和石灰乳制取漂白粉的化学反应方程式是____________ 。
①2013年,全国多个省市出现严重的雾霾天气。导致雾霾形成的主要污染物是
A.O2 B.CO2 C.PM2.5
②采用焚烧处理垃圾进行发电已在江苏投入使用。下列是生活中的常见垃圾.
A.废电池 B.易拉罐 C.玻璃瓶
在焚烧处理前,除废电池外,还有
③漂白粉可用于生活用水的杀菌消毒,工业上利用氯气和石灰乳制取漂白粉的化学反应方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)根据题意选择以下四种物质的字母序号填空:
A.Si B.Na2SiO3 C.Ca(ClO)2 D.KAl(SO4)2·12H2O
①漂白粉的有效成分是_______ 。
②可用于制备硅胶和木材防火剂的是_______ 。
③可用于制计算机芯片的是_______ 。
④可用于作净水剂的是_______ 。
(2)物质的量是化学中常用的物理量,请完成以下有关计算:
①标准状况下,含有相同氧原子数的CO和CO2的体积之比为_______ 。
②100 mL硫酸钠溶液中n(Na+)=0.20 mol,则其中c( )=
)=_______ 。
③配制1.0 mol/L硫酸溶液250 mL ,需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为_______ mL(计算结果保留一位小数)。如果实验室有15 mL、20 mL、50 mL量筒,应选用_______ mL的量筒最好。若定容时仰视刻度线,所配溶液浓度_______ 。(填偏大、偏小或无影响)
A.Si B.Na2SiO3 C.Ca(ClO)2 D.KAl(SO4)2·12H2O
①漂白粉的有效成分是
②可用于制备硅胶和木材防火剂的是
③可用于制计算机芯片的是
④可用于作净水剂的是
(2)物质的量是化学中常用的物理量,请完成以下有关计算:
①标准状况下,含有相同氧原子数的CO和CO2的体积之比为
②100 mL硫酸钠溶液中n(Na+)=0.20 mol,则其中c(
 )=
)=③配制1.0 mol/L硫酸溶液250 mL ,需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】“化学一我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请回答下列问题:
(1)云、雾属于胶体,鉴别胶体和溶液的方法是____ ,胶体和溶液的本质区别是____ 。
(2)钠的焰色试验的焰色为____ 色,该色的光射程远,透雾力强,据此原理制作的高压钠灯广泛应用于道路和广场的照明。焰色试验属于____ (填“物理”或“化学”)变化。
(3)将新鲜的有色花瓣放入干燥的氯气中,可观察到的现象是____ ,原因是____ 。
(4)漂白粉暴露在空气中易变质,若向暴露在空气中的漂白粉中加入浓盐酸,可能收集到的气体除了挥发的HCl和水蒸气,还可能有____ (填化学式)。
(1)云、雾属于胶体,鉴别胶体和溶液的方法是
(2)钠的焰色试验的焰色为
(3)将新鲜的有色花瓣放入干燥的氯气中,可观察到的现象是
(4)漂白粉暴露在空气中易变质,若向暴露在空气中的漂白粉中加入浓盐酸,可能收集到的气体除了挥发的HCl和水蒸气,还可能有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】漂白粉的主要成分是次氯酸钙和氯化钙。请回答下列问题:
(1)漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式(若涉及氧化还原反应,请标注电子转移情况):____________________________ 。
(2)某化学小组将完全变质后的漂白粉溶于水,向其中加入足量稀硝酸,共收集到标准状况下448mL气体,则该漂白粉中所含有效成份的质量为_____________ (假设漂白粉中的其它成份不与硝酸反应)。
(1)漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式(若涉及氧化还原反应,请标注电子转移情况):
(2)某化学小组将完全变质后的漂白粉溶于水,向其中加入足量稀硝酸,共收集到标准状况下448mL气体,则该漂白粉中所含有效成份的质量为
您最近一年使用:0次



